ОРИГИНАЛЬНЫЕ ПУБЛИКАЦИИ
Что уже известно об этой теме?
► Нозокомиальная пневмония – одно из самых распространенных инфекционных заболеваний в медицинских учреждениях
► Антибактериальная резистентность возбудителей госпитальных инфекций значительно осложняет выбор терапии и зачастую вынуждает применять большое количество антибактериальных препаратов (АБП) с широким спектром действия
► Актуальная клинико-экономическая оценка применения системных АБП в условиях реальной клинической практики за счет сложности ее выполнения представлена крайне немногочисленными данными
Что нового дает статья?
► Оценена клинико-экономическая эффективность применения АБП в качестве терапии нозокомиальной пневмонии в условиях стационара
► На основании данных реальной практики проведен анализ прямых медицинских затрат, ассоциированных с патогенами группы ESKAPE
Как это может повлиять на клиническую практику в обозримом будущем?
► Полученные данные могут быть использованы для рационализации антибиотикотерапии и планирования больничного формуляра антимикробных препаратов
► Результаты исследования помогут оптимизировать расходы медицинской организации, учитывая высокую стоимость системной антибактериальной терапии и микробиологического мониторинга инфекционных патогенов
Цель: клинико-экономический анализ применения антибактериальной терапии нозокомиальной пневмонии тяжелого течения в условиях реальной клинической практики многопрофильного стационара г. Москвы.
Материал и методы. Проведено ретроспективное исследование медицинских карт пациентов, поступивших в многопрофильный стационар ГБУЗ «ГКБ им. С.С. Юдина ДЗМ» в г. Москве в 2019–2021 гг. В рамках фармакоэпидемиологического анализа изучены структура назначений антибактериальных препаратов (АБП), особенности эмпирической и этиотропной терапии, длительность применения АБП и другие параметры. Для анализа отобрано 110 случаев нозокомиальной пневмонии тяжелого течения, вызванной патогенами группы ESKAPE. Выполнено сравнение эффективности затрат некоторых режимов эмпирической антибактериальной терапии. Рассчитаны прямые медицинские затраты, коэффициенты «затраты – эффективность» на основании данных реальной клинической практики.
Результаты. Установлено, что нозокомиальная пневмония – это наиболее часто возникающее осложнение среди госпитализированных пациентов стационара. K. pneumoniae, A. Baumanii и P. aeruginosa – основные возбудители нозокомиальной пневмонии в отделении реанимации и интенсивной терапии (ОРИТ). АБП в стационаре были представлены 31 международными непатентованными наименованиями группы J01 Антибактериальные препараты системного действия. Прямые медицинские затраты на эмпирическую антибактериальную терапию составили в среднем 9367 руб. (2118 руб. [1462; 3525]). Сравнительный анализ эффективности затрат на применение АБП выполнен на основании суррогатных и конечных точек. Показано, что прямые медицинские затраты, ассоциированные с патогенами группы ESKAPE, составляют около 70% бюджетных средств установленного тарифа на оплату медицинской помощи программы обязательного медицинского страхования по пребыванию пациента в ОРИТ.
Заключение. Затраты на антибактериальную терапию нозокомиальной пневмонии значительно увеличивают общую стоимость пребывания пациента в стационаре. С учетом ограниченных ресурсов здравоохранения результаты клинико-экономической оценки применения АБП позволяют оптимизировать расходы на терапию, а также помогают специалистам в формировании больничного формуляра антимикробных препаратов.
Что уже известно об этой теме?
► Лекарственные препараты (ЛП) для лечения редких заболеваний характеризуются высоким уровнем неопределенности в отношении их клинической эффективности
► Для принятия решений о возмещении ЛП, предназначенных для лечения детей с тяжелыми жизнеугрожающими, в т.ч. редкими, заболеваниями, необходим учет различных клинических, экономических и социальных факторов
Что нового дает статья?
► Выполнен анализ ЛП и заболеваний, в отношении которых была проведена оценка технологий здравоохранения для их включения в перечни Фонда «Круг добра» в период с 1 февраля 2021 г. по 31 декабря 2024 г.
► Включенные в перечни Фонда «Круг добра» пары «ЛП – заболевание» характеризуются высокой неудовлетворенной медицинской потребностью (отсутствием альтернативных методов лечения), а также, более чем в половине случаев, соответствующим орфанным статусом в ЕС и/или США
► В исследованиях клинической эффективности ЛП отмечены: преимущественное использование суррогатных исходов, временной горизонт оценки исходов, в среднем равный 12 мес от начала терапии, а также отсутствие сравнительных данных в трети случаев
Как это может повлиять на клиническую практику в обозримом будущем?
► Включение ЛП в перечни для закупок Фонда «Круг добра» и анализ соответствующих закономерностей способствуют повышению качества оказания медицинской помощи детям
► Оценка технологий здравоохранения и финансирование, в частности, незарегистрированных ЛП позволяют пациентам раньше получать инновационные препараты, увеличивая продолжительность и качество их жизни
Актуальность. В 2021 г. для дополнительного финансового обеспечения детей с тяжелыми жизнеугрожающими и хроническими заболеваниями необходимым лечением, в частности дорогостоящими лекарственными препаратами (ЛП), был создан Фонд поддержки детей с тяжелыми жизнеугрожающими и хроническими заболеваниями, в т.ч. редкими (орфанными) заболеваниями, «Круг добра» (далее – Фонд «Круг добра»). При этом преобладающая часть обеспечиваемых ЛП предназначена для терапии редких заболеваний. Методологической поддержкой при принятии решений о включении заболеваний в перечень заболеваний и ЛП в перечни для закупок Фонда «Круг добра» является оценка технологий здравоохранения (комплексная оценка), проводимая ФГБУ «Центр экспертизы и контроля качества медицинской помощи» Минздрава России.
Цель: анализ характеристик ЛП, в отношении которых была проведена комплексная оценка за четыре года работы Фонда «Круг добра», в зависимости от их статуса включения в перечни для закупок, а также обзор доказательной базы, подтверждающей клиническую эффективность рассмотренных ЛП.
Материал и методы. Проанализированы 187 пар «ЛП – заболевание», по которым была проведена комплексная оценка, по следующим характеристикам: статус регистрации ЛП на территории Российской Федерации, Соединенных штатов Америки (США) и Европейского союза (ЕС) и данные о наличии орфанного статуса у зарегистрированных технологий, факт наличия неудовлетворенной терапевтической потребности в данном ЛП (отсутствия альтернативных опций терапии) и данные о наличии воспроизведенных ЛП. Характеристики опубликованных исследований о клинической эффективности ЛП, включенных в анализ, содержали данные о дизайне исследования, использованных конечных точках (суррогатные или «конечные» исходы), медиане наблюдения, группе контроля, а также факте наличия сравнительных исследований для каждой пары «ЛП – заболевание».
Результаты. Установлено, что ЛП, включенные в перечни для закупок, по сравнению с рассмотренными невключенными ЛП, характеризовались большей частотой получения орфанного статуса в США (84,6% против 67,8%) и ЕС (65,7% против с 38,8%), а также отсутствием альтернативных опций терапии (50,6% против 32,0%). Использование только суррогатных исходов отмечено в 56% опубликованных исследований о клинической эффективности ЛП, медиана временного горизонта оценки исходов составила 12,00 мес (межквартильный интервал 5,52–35,94), а среди дизайнов преобладали рандомизированные контролируемые испытания и несравнительные исследования (36,7% и 30,9% соответственно). Опубликованные данные о результатах сравнительных исследований отсутствовали для 36,8% всех проанализированных пар «ЛП – заболевание».
Заключение. Включенные в перечни Фонда «Круг добра» пары «ЛП – заболевание» характеризуются высокой неудовлетворенной медицинской потребностью (отсутствием альтернативных методов лечения), а также (более чем в половине случаев) соответствующим орфанным статусом в ЕС и/или США. Полученные результаты также соответствуют данным отечественных и зарубежных авторов о преимущественном использовании суррогатных исходов и распространенности применения несравнительных дизайнов исследований, обосновывающих эффективность орфанных ЛП. Это подчеркивает актуальность и целесообразность проведения комплексной оценки ЛП с высокой неопределенностью в отношении их эффективности, которая, с одной стороны, позволяет учитывать ограничения доказательности их клинических исследований, а с другой – обобщает данные о прочих значимых характеристиках ЛП и редкого заболевания.
Что уже известно об этой теме?
► Стоимость противоопухолевой лекарственной терапии (ПОЛТ) создает беспрецедентное финансовое давление на системы здравоохранения во всем мире
► Современные исследования демонстрируют, что высокая стоимость инновационных противоопухолевых препаратов не всегда коррелирует с достижением значимых клинических результатов
► Комбинированный ABC/VEN-анализ как метод клинико-экономического анализа служит эффективным инструментом комплексной оценки финансовой нагрузки (ABC) и клинической значимости (VEN) схем ПОЛТ
Что нового дает статья?
► Выявлены диспропорции в структуре финансирования ПОЛТ, характерные для современных систем лекарственного обеспечения с акцентом на финансирование таргетных опций терапии
► Включение препаратов одного вида в разные категории при проведении ABC-анализа может свидетельствовать о существовании «бюджетных» аналогов и недостаточном использовании более доступных и эквивалентных препаратов при их наличии, в т.ч. дженериков и биосимиляров
► Примерный перечень ВОЗ для классификации препаратов по группам VEN включает только те средства, которые показали значительные преимущества в выживаемости или достигли установленного ВОЗ порога эффективности, что ограничило оценку препаратов, не продемонстрировавших такие приоритеты
Как это может повлиять на клиническую практику в обозримом будущем?
► Полученные результаты подчеркивают необходимость разработки адаптивной системы лекарственного обеспечения, которая учитывала бы как клиническую значимость препаратов, так и экономическую эффективность их применения
► Сохранение полного доступа пациентов к эффективному лечению является неоспоримым приоритетом онкологической практики, требующим при этом строгой оценки объективных показателей улучшения качества и продолжительности жизни
► Одним из возможных решений является мультикритериальная система оценки противоопухолевых препаратов с учетом клинической эффективности, социальной значимости, фармакоэкономических параметров и иных факторов, влияющих на систему здравоохранения в целом
Актуальность. Современная онкология столкнулась с парадоксальной ситуацией: стремительный рост стоимости противоопухолевой терапии не всегда сопровождается пропорциональным увеличением ее эффективности. Это создает серьезные экономические барьеры для систем здравоохранения по всему миру. В условиях ограниченных ресурсов особую актуальность приобретают методы рационального распределения лекарственного бюджета. Комбинированный ABC/VEN-анализ представляет собой эффективный инструмент для решения этой задачи. Такой подход особенно важен при анализе современных пероральных противоопухолевых препаратов, занимающих все более значимое место в терапии онкологических заболеваний.
Цель: оценить структуру затрат на пероральную противоопухолевую терапию методами ABC/VEN- и частотного анализа.
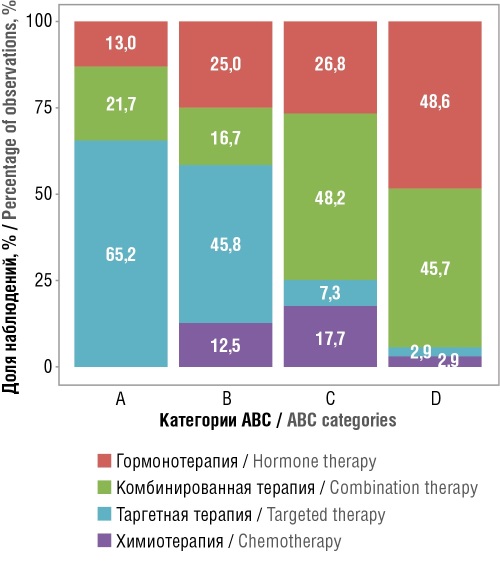
Материал и методы. Распределение по АВС-категориям осуществлялось согласно общепринятой методологии. В группу А (наиболее затратные препараты) вошли схемы, общая стоимость которых составила 80% от всех затраченных средств, группу С (наименее затратные) составили схемы с не более 5% всех затрат. Остальные схемы включены в группу В (менее затратные), на осуществление терапии которыми израсходовано 15% всех средств. Итоговые затраты определялись исходя из стоимости лекарственной терапии по схеме в условиях дневного стационара и количества случаев оказания медицинской помощи по данной схеме за 2022 г. Формальная методология VEN-анализа заключалась в распределении схем в соответствии с наличием содержащихся в них препаратов из Примерного перечня Всемирной организации здравоохранения основных лекарственных средств. Отдельно в части как АВС, так и VEN проанализированы данные в разрезе групп химиотерапии, гормональной терапии, таргетной терапии или комбинированной схемы лечения. Частотный анализ проведен с учетом количества госпитализаций пациентов, получивших ту или иную схему противоопухолевой терапии по данным реальной практики деперсонифицированных реестров структуры госпитализаций.
Результаты. Анализ распределения ресурсов подтвердил действие принципа Парето, при котором 80% финансовых затрат пришлось на 9,3% (95% ДИ 6,0–13,7) терапевтических схем (23 схемы), составивших высокозатратную группу А. В группу С (не более 5% затрат) вошли 164 схемы (66,7%; 95% ДИ 60,4–72,5). Остальные препараты оказались в группе В (15% затрат) – 24 схемы (9,8%; 95% ДИ 6,4–14,2). При этом 35 схем (14,2%; 95% ДИ 10,1–19,2) в 2022 г. не использовались. Распределение схем по группам VEN также было сопоставимо с рекомендуемым: 149 схем (60,6%; 95% ДИ 54,2–66,7) для группы V, 63 схемы (25,6%; 95% ДИ 20,3–31,5) для группы E и 34 схемы (13,8%; 95% ДИ 9,8–18,8) для группы N. Объединенный ABC/VEN-анализ продемонстрировал, что группа А преимущественно включает препараты группы V (52,2%). Однако в части ABC/VEN-анализа также выявлены диспропорции: обнаруженная значительная доля (39,1%) препаратов категории N в группе А требует особого внимания и указывает на необходимость создания механизмов регулирования назначений высокозатратных препаратов.
Заключение. Полученные результаты создают основу для разработки сбалансированных подходов к лекарственному обеспечению в онкологии, сочетающих принципы клинической целесообразности и экономической эффективности. Исследование обосновывает необходимость распределения средств, гарантирующих приоритетное обеспечение доказательно эффективных схем лечения в условиях ресурсных ограничений.
Что уже известно об этой теме?
► В структуре потребления антигипертензивных лекарственных препаратов (АГЛП) в Российской Федерации (РФ) преобладают монопрепараты, а применение статинов населением находится на низком уровне
► Объемы и структура аптечной реализации АГЛП и статинов в течение 6 последних лет в масштабах 83 из 89 регионов РФ ранее не изучались
Что нового дает статья?
► Представлен материал по структуре продаж в 5200 аптечных организациях основных сердечно-сосудистых препаратов (АГЛП и статинов), репрезентативный для 7 федеральных округов и для РФ в целом
► Выявлены низкая доля фиксированных комбинаций (ФК) АГЛП и статинов в структуре потребления основных сердечно-сосудистых препаратов населением и отсутствие их значимого прироста в последние годы
► Показано, что низкая стоимость монопрепаратов является главным фактором их преимущественного использования населением
Как это может повлиять на клиническую практику в обозримом будущем?
► Представленные данные являются надежной основой для изучения динамики аптечных продаж рассматриваемых препаратов в РФ
► Требуются усилия, направленные на большее потребление статинов и АГЛП как основных трендов в кардиологии
► Полученные результаты указывают на необходимость снижения стоимости ФК АГЛП
Актуальность. В современной популяции в структуре неинфекционных заболеваний превалируют болезни сердечно-сосудистой системы, ассоциированные с артериальной гипертензией и дислипидемией, что обосновывает потребность долговременной фармакотерапии антигипертензивными и гиполипидемическими препаратами.
Цель: изучение профиля потребления населением Российской Федерации (РФ) антигипертензивных и гиполипидемических лекарственных препаратов, которые могут быть рассмотрены как основные сердечно-сосудистые средства.
Материал и методы. Проведено многолетнее ретроспективное фармакоэпидемиологическое исследование. Изучена статистика аптечных продаж данных групп как в качестве монопрепаратов, так и в виде фиксированных комбинаций (ФК) с 2017 по 2022 гг. в 5221 аптечной организации 83 регионов РФ из 70 400 аптечных организаций, зарегистрированных в РФ в 2022 г.
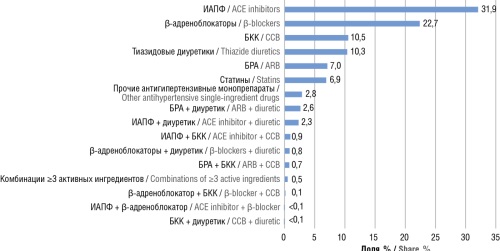
Результаты. Установлено, что преобладает потребление монопрепаратов: ингибиторов ангиотензин-превращающего фермента (31,9%), β-блокаторов (22,7%), блокаторов кальциевых каналов (10,5%) и диуретиков (10,3%). Среди монопрепаратов лидирующие позиции занимают амлодипин (13,6%), эналаприл (11,6%), индапамид (9,7%). Среди ФК наиболее распространены «лозартан + гидрохлоротиазид» (20,6%), «периндоприл + индапамид» (15,4%), «амлодипин + индапамид + периндоприл» (9,1%). Средняя стоимость 1 установленной суточной дозы (англ. defined daily dose, DDD) для диуретиков – 2,8 руб., для блокаторов кальциевых каналов – 3,2 руб., для ингибиторов ангиотензинпревращающего фермента – 4,0 руб., для сартанов – 8 руб., для β-блокаторов – 10 руб., для статинов – 9 руб. Стоимость 1 DDD для ФК существенно выше – 15–40 руб., что может быть основным фактором их чрезвычайно низкого потребления (ФК антигипертензивных препаратов – 7,1%, статинов – 6,9%), не соответствующего требованиям современных клинических рекомендаций.
Заключение. Структура аптечной реализации основных кардиологических лекарственных средств в 2017–2022 гг. консервативна с преобладанием монопрепаратов и не соответствует трендам современной кардиологии на расширенное потребление ФК и статинов. До сих пор на рынке РФ нет ни одного отечественного препарата полипилл, включающего антигипертензивное средство и статин, а доля продаж импортных мультитаргетных препаратов полипилл крайне мала.
Что уже известно об этой теме?
► Исторически в Российской Федерации наблюдается несоответствие между теоретической потребностью в применении ингибиторов ангиогенеза и их фактическим уровнем потребления у пациентов с возрастной макулярной дегенерацией
► Последние данные о применении ингибиторов ангиогенеза относятся к 2019 г., что обосновывает необходимость актуализации информации о текущем состоянии их применения системой здравоохранения
Что нового дает статья?
► Актуализированы данные об ассортименте, предельных отпускных и фактических ценах на ингибиторы ангиогенеза, объемах закупок и потребления за период с 2018 по 2024 гг. включительно
► Выявлена положительная динамика в обеспечении данной группой лекарственных препаратов. Наблюдался общий рост закупок, включая показатели дорогих представителей группы
► Расчеты указывают на использование одного флакона препарата ингибитора ангиогенеза у нескольких пациентов, что не соответствует их инструкциям по медицинскому применению
Как это может повлиять на клиническую практику в обозримом будущем?
► Результаты исследования могут быть использованы для совершенствования системы лекарственной помощи пациентам с возрастной макулярной дегенерацией
► Полученные данные могут служить основанием для производителей и поставщиков ингибиторов ангиогенеза для наращивания предложения данной группы препаратов
► Показана необходимость урегулирования ситуации с использованием одного флакона ингибитора ангиогенеза у нескольких пациентов
Актуальность. Исследования лекарственного обеспечения неоваскулярной возрастной макулярной дегенерации ингибиторами ангиогенеза в Российской Федерации неоднократно указывали на несоответствие между уровнем потребления и реальной потребностью в них, что позволяет считать актуальным дальнейшее изучения данного вопроса посредством маркетингового анализа.
Цель: провести маркетинговый анализ рынка ингибиторов ангиогенеза для лечения неоваскулярной возрастной макулярной дегенерации, включающий оценку ассортимента, динамики цен, спроса и потребления, а также индексный анализ за период 2018–2024 гг.
Материал и методы. Исследование основано на открытых данных о закупках ингибиторов ангиогенеза в государственном сегменте, ценовых характеристиках, сведениях о потреблении в сфере обязательного медицинского страхования (круглосуточные и дневные стационары, высокотехнологичная медицинская помощь). Научно-методический аппарат составили методы анализа продаж лекарственных препаратов (ЛП) из группы ингибиторов ангиогенеза, зарегистрированных к медицинскому применению на территории Российской Федерации, а также методические инструменты для расчетов ряда цепных индексов (индекса средневзвешенных цен, индекса цен, индекса структурных сдвигов, индекса изменения натуральных объемов продаж, модифицированного индекса Герфиндаля–Хиршмана). Использованы методики анализа жизненного цикла рассмотренных ЛП и сравнения объемов их закупок и потребления.
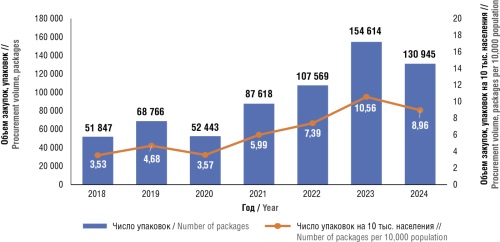
Результаты. В течение рассматриваемого периода наблюдался заметный рост спроса на ингибиторы ангиогенеза и их потребления: закупки в натуральном выражении выросли в 2,53 раза, в денежном – в 1,62 раза. Положительная динамика рынка исследуемой группы ЛП сопровождалась ростом средневзвешенных цен и доли более дорогостоящих ЛП в структуре закупок. В период с 2021 по 2023 гг. выявлен неравномерный рост объемов закупок в натуральном выражении и числа госпитализаций для применения рассматриваемых ЛП. Соотношение объемов госпитализаций и закупок за период составило 1,21, 1,46 и 1,47 соответственно, что указывает на применение одного флакона ЛП для нескольких пациентов. Диспропорция между объемами закупок и числом госпитализаций свидетельствует о наличии значительного дополнительного потенциального спроса на ингибиторы ангиогенеза. Сложившаяся конъюнктура рынка позволяет характеризовать его как привлекательный для производителей и поставщиков.
Заключение. Установлено, что рынок ингибиторов ангиогенеза характеризуется тенденциями качественного и количественного роста с сохранением положительной динамики развития. Выявленные особенности закупок и потребления указывают на необходимость дальнейших исследований в целях выработки оптимальных решений в сфере лекарственного обеспечения потребителей ингибиторами ангиогенеза в необходимом ассортименте и достаточных объемах.
Что уже известно об этой теме?
► Омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК) изучены как кардиопротективные, противовоспалительные и гепатопротективные агенты, широко применяются в фармакологии и нутрициологии для профилактики и терапии хронических заболеваний
► Жирнокислотный состав зависит от источника: морская рыба богата эйкозапентаеновой кислотой (ЭПК) и докозагексаеновой кислотой (ДГК), растительные масла содержат альфа-липоевую кислоту, водоросли – устойчивый источник ДГК
► Препараты различаются по концентрации ПНЖК, степени этерификации (триглицериды или этиловые эфиры), уровню очистки и наличию дополнительных антиоксидантов, влияющих на стабильность
Что нового дает статья?
► Проведено исследование жирнокислотного состава 16 препаратов ω3-ПНЖК, включившее количественное хроматографическое определение более 50 жирных кислот, их производных и других соединений
► Подтверждены полученные ранее и получены новые фармакомаркеры жирнокислотного состава, позволяющие с высокой достоверностью отделять препараты с высокой степенью стандартизации по ω3-ПНЖК
► Предложены новые, более эффективные критерии оценки качества жирнокислотного состава препаратов ω3-ПНЖК. В частности, выполнимость критериев «ω11<3%», «ЭПК+ДГК>55%» соответствует более стандартизированным препаратам с лучшим качеством очистки
Как это может повлиять на клиническую практику в обозримом будущем?
► Используя полученные в исследовании данные, врачи смогут выбирать более стандартизированные препараты ω3-ПНЖК с доказанным составом и стабильностью
► Улучшится персонализированный подбор ω3-препаратов для пациентов с различными патологиями
► Появится основа для включения новых критериев качества в фармакопейные статьи и рекомендации
Актуальность. Омега-3 полиненасыщенные жирные кислоты (ω3-ПНЖК) – важный фактор соматического и репродуктивного здоровья. Микронутриентные и фармацевтические препараты на основе ω3-ПНЖК широко используются для кардиопротекции (профилактика атеросклероза, эндотелиальной дисфункции, хронического воспаления, избыточного тромбообразования), поддержки репродуктивной функции во время беременности и улучшения неврологического развития детей. Эффективность препаратов ω3-ПНЖК определяется их жирнокислотным составом: количествами эйкозапентаеновой кислоты (ЭПК), докозагексаеновой кислоты (ДГК) и других видов ненасыщенных и насыщенных жирных кислот.
Цель: провести анализ жирнокислотного состава микронутриентных и фармацевтических препаратов ω3-ПНЖК.
Материал и методы. Проведено исследование жирнокислотного состава 16 препаратов ω3-ПНЖК. Использован метод количественного хроматографического определения более 50 жирных кислот, их производных и других соединений.
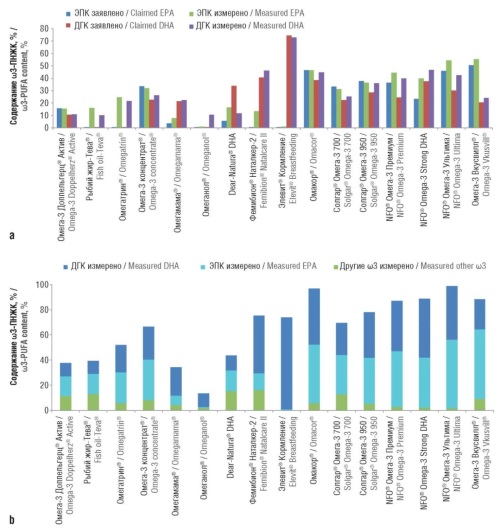
Результаты. Подтверждены полученные ранее и получены новые фармакомаркеры жирнокислотного состава, позволяющие с высокой достоверностью отделять препараты с высокой степенью стандартизации по ω3-ПНЖК (Омакор®, NFO® Омега-3 Премиум, NFO® Omega-3 Strong DHA, NFO® Омега-3 Ультима и др.) от менее стандартизированных (Рыбий жир-Тева®, Омеганол® и др.). Предложены новые, более эффективные критерии оценки качества жирнокислотного состава препаратов ω3-ПНЖК. В частности, выполнимость критериев «ω11<3%», «ЭПК+ДГК>55%» соответствует более стандартизированным препаратам с лучшим качеством очистки. Подтверждена полезность предлагаемого нами коэффициента стандартизации препаратов, оценивающего соответствие измеренных уровней ω3-ПНЖК содержанию, заявленному производителем.
Заключение. Выполнимость критериев «ω11<3%», «ЭПК+ДГК>55%» соответствует более стандартизированным препаратам. Выделение высокостандартизированных составов позволяет врачам и пациентам делать информированный выбор при необходимости приема препаратов ω3-ПНЖК.
Что уже известно об этой теме?
► Ценностно-ориентированное здравоохранение (ЦОЗ) – это модель оказания медицинской помощи, оценивающая соотношение клинических результатов, значимых для пациента исходов и экономических затрат
► Эффективное внедрение ЦОЗ требует строгой стандартизации показателей, поскольку ее отсутствие препятствует объективному анализу и улучшению качества помощи
► Для стандартизации оценки медицинской помощи Консорциум ICHOM разрабатывает унифицированные наборы показателей, интегрирующие результаты, важные для ЦОЗ, однако низкая осведомленность исследователей об этом ресурсе ограничивает его применение в научных работах
Что нового дает статья?
► Структурирован процесс внедрения ЦОЗ путем систематизации методологических подходов к сбору и анализу данных согласно рекомендациям ICHOM
► Результаты подтверждают, что разработанная структура данных отвечает критериям ЦОЗ, позволяя проводить комплексный анализ медицинской помощи на основе клинических исходов и показателей, сообщаемых пациентами
► Унификация подходов к сбору данных через международные стандарты обеспечивает объективное измерение эффективности медицинской помощи и создает единую концептуальную основу для всех участников системы здравоохранения
Как это может повлиять на клиническую практику в обозримом будущем?
► Полученные данные имеют большое практическое значение для внедрения принципов ЦОЗ в клиническую практику, обеспечивая методологическую основу для стандартизированной оценки эффективности медицинской помощи
► Следующим этапом работы в данном направлении должна стать адаптация сбора данных по конкретным сетам с учетом национальных особенностей и возможностей проведения исследований ЦОЗ в России
Актуальность. Ценностно-ориентированное здравоохранение (ЦОЗ) – это модель медицинской помощи, основанная на анализе результатов лечения с учетом значимых для пациента результатов (ценности), клинической эффективности и экономических затрат. Несмотря на существование стандартизированных систем оценки (например, разработанной Международным консорциумом по оценке клинических исходов (англ. International Consortium for Health Outcomes Measurement, ICHOM)), их практическое применение остается ограниченным, что замедляет внедрение ЦОЗ. Отсутствие унифицированных методик снижает сопоставимость данных между медицинскими организациями, выявление наилучших практик и в итоге препятствует практической реализации ЦОЗ.
Цель: анализ и адаптация стандартизированных подходов к оценке параметров ЦОЗ и методологии их сбора на основе наборов показателей ICHOM.
Материал и методы. Проведен комплексный анализ 49 стандартизированных наборов ICHOM и 43 связанных публикаций в рецензируемых журналах. Выполнено структурированное изучение объектов исследования с выделением основных характеристик сбора данных. Сформирован перечень ключевой информации для сбора, выявлены возможные препятствия при внедрении медицинскими организациями методик сбора данных. Применены методы качественного контент-анализа и сравнительного анализа данных.
Результаты. В статье представлена унифицированная структура показателей для оценки ЦОЗ. Особое внимание уделено трем ключевым компонентам оценки исходов: пациентоориентированным исходам – результатам, сообщаемым пациентами, клиническим исходам и показателям использования ресурсов здравоохранения. Выявлены стандартизированные подходы к сбору данных, каждый из которых имеет свои ограничения. Определены оптимальные временные точки мониторинга (таймлайны), варьирующиеся в зависимости от типа нозологии. Полученные результаты демонстрируют, что стандарты ICHOM обеспечивают комплексную основу для оценки ценностно-ориентированной медицинской помощи, однако требуют адаптации к конкретным организационным условиям. Разработанная категоризация данных и представленные выводы создают предпосылки для того, чтобы медицинские учреждения начали процесс внедрения ценностно-ориентированного подхода, уделяя особое внимание исходам, значимым для пациентов.
Заключение. Выполненный анализ обосновывает необходимость проведения исследований ЦОЗ в соответствии с унифицированными стандартами ICHOM. Единая методология может обеспечить комплексную и объективную оценку эффективности помощи и сформировать общее понимание концепции всеми участниками. Подобный подход позволит перейти от теории к глобальной практике оценки ценности в медицине. Следующим этапом работы в данном направлении должна стать адаптация сбора данных по конкретным наборам с учетом национальных особенностей и возможностей в России.
Что уже известно об этой теме?
► Косметические средства являются товарной группой на фармацевтическом рынке в рамках аптечных продаж, которая характеризуется менее строгим государственным регулированием, чем обращение лекарственных средств
► При продаже в аптеках косметические средства позиционируются как качественные и безопасные. Объем реализации косметики в аптеках в 2022 г. составил рекордные 50 млрд руб., что делает данную товарную группу значимой в структуре продаж аптечных сетей
► С введением антироссийских санкций сократились поставки зарубежной косметики, что открывает возможности для роста отечественных брендов
Что нового дает статья?
► Проведена оценка присутствия доминирующих групп в трех сегментах косметических средств в рамках аптечных продаж на основе матрицы «сила/разнообразие»
► Сегмент селективной косметики, характеризующийся наиболее дорогими товарами, является самым концентрированным. Доминирующая группа, состоящая из зарубежных брендов, попадает в квадрант «естественная олигополия»
► Рынки масс-маркет и активной косметики являются конкурентными, т.к. доминирующая группа в последние годы не выявлена. Отмечено значительное усиление позиций некоторых отечественных брендов
Как это может повлиять на клиническую практику в обозримом будущем?
► В сегментах, где успешно растут отечественные бренды, будет заметно замещение зарубежных косметических средств более доступными российскими аналогами
► На рынке селективной косметики, где доминируют зарубежные бренды, товары будут менее доступными для приобретения, что может привести к увеличению стоимости дерматологической помощи
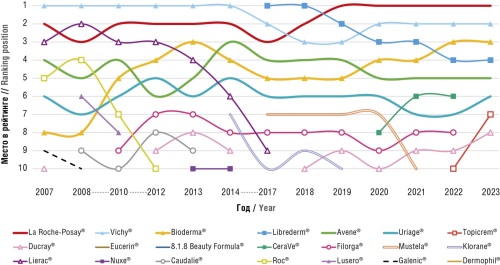
Цель: анализ конкуренции и уровня доминирования на рынке косметических средств в рамках аптечных продаж, выявление трендов в трех ключевых сегментах: селективной, масс-маркет и активной (лечебной) косметики.
Материал и методы. В качестве материалов были взяты ежегодные отчеты о российском фармацевтическом рынке компании DSM Group. Для анализа были применены индексы Линда и Герфиндаля–Хиршмана, а также матрица «сила/разнообразие» (англ. strength/variety, SV), включающая коэффициенты концентрации и модифицированный индекс Холла–Тайдмана. Оценена степень концентрации на рынке, определено наличие доминирующих групп, проведен анализ структуры рынка и динамики рейтинга крупных игроков.
Результаты. На российском рынке косметических средств в рамках аптечных продаж наблюдаются как сходства, так и существенные различия между сегментами. В сегменте селективной косметики, где доминируют иностранные игроки (кроме отечественного Librederm®), произошла трансформация от высокой дифференциации брендов к состоянию, близкому к естественной олигополии. Эта тенденция сопровождается усилением позиций российских брендов после 2014 г. В отличие от данного сегмента, рынок косметики масс-маркет, характеризующийся высокой динамичностью и конкуренцией, демонстрирует низкую концентрацию и более размытые лидерские позиции, при этом неоднозначность динамики международных игроков после 2014 г. сопровождается усилением позиций отечественных брендов, например Мое солнышко®, что свидетельствует о влиянии геополитики не только на сегмент селективной косметики, но и на масс-маркет косметику. Сегмент активной (лечебной) косметики, где лидируют российские производители, отличается относительной стабильностью отдельных брендов, таких как Alerana®, на фоне высокой изменчивости рынка. Отсутствие доминирующего ядра подтверждает высокий уровень конкуренции.
Заключение. Существуют различия в развитии сегментов косметических средств в рамках аптечных продаж: самым концентрированным является сегмент селективной косметики, в отличие от сегментов масс-маркет и активной (лечебной) косметики, характеризующихся высоким уровнем конкуренции. Значимость отечественных брендов после введения санкций возросла.
Что уже известно об этой теме?
► Для эффективной фармакотерапии воспаления и боли используются нестероидные противовоспалительные препараты (НПВП). Однако длительная терапия НПВП и/или их неадекватное применение могут привести к повреждениям желудочно-кишечного тракта
► Комплекс диклофенака с цинком оказывает те же противовоспалительные и антиноцицептивные эффекты, но вызывает меньшую частоту поражений желудка по сравнению с диклофенаком
► Комбинация «цинк + НПВП» является донором эссенциального микроэлемента цинка, который проявляет противовоспалительные, ранозаживляющие и иммуномодулирующие свойства
Что нового дает статья?
► Хемореактомный анализ показал, что цинкосодержащее соединение пилим-1 (бис-(1-винилимидазол)цинкдиацетат) – перспективная молекула с противовоспалительной активностью, лишенная ульцерогенного эффекта
► Противовоспалительное действие пилима-1 реализуется через модуляцию активности цитокинов, метаболизма простагландинов и лейкотриенов, анальгетический эффект основан на ингибировании кининовых и гистаминовых рецепторов
► Пилим-1 отличается нейтральностью по отношению к обмену витаминов при противовоспалительном действии, сопоставимом по силе с цинкосодержащими производными НПВП
Как это может повлиять на клиническую практику в обозримом будущем?
► Перспективно создание на основе пилима-1 лекарственного препарата с выраженными противовоспалительными и анальгезирующими свойствами, не обладающего ульцерогенным действием
► При суточной потребности в цинке порядка 15–20 мг пилим-1 и исследованные цинк-НПВП являются существенными источниками элементного цинка
Актуальность. Гастроэнтерологические побочные эффекты (эрозии пищевода, желудка и кишечника) при использовании лекарственных средств из группы нестероидных противовоспалительных препаратов (НПВП) диктуют необходимость изучения новых молекул-кандидатов со сниженным ульцерогенным действием. Цинкосодержащая молекула-кандидат пилим-1 потенциально может проявлять противовоспалительный эффект и улучшать регенеративные свойства слизистой желудка.
Цель: изучить противовоспалительные, ульцерогенные, анальгетические и антивитаминные эффекты молекулы пилим-1 методами хемореактомики.
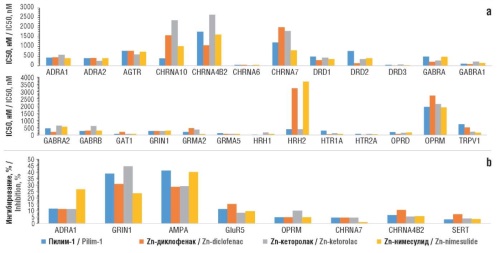
Материал и методы. Проведена хемореактомная оценка фармакологических свойств пилима-1 и цинковых производных известных НПВП (кеторолак, диклофенак и нимесулид) посредством методов хемоинформационного анализа молекул, развиваемых в научной школе академика Ю.И. Журавлёва.
Результаты. Пилим-1 обладает отчетливым противовоспалительным действием, реализующимся через модуляцию активности цитокинов, метаболизма простагландинов и лейкотриенов. Важнейшим отличием молекулы пилим-1 является нейтральность по отношению к обмену витаминов при сопоставимости по силе противовоспалительного действия с цинкосодержащими производными НПВП. Анальгетическое действие пилима-1 основывается на ингибировании кининовых и гистаминовых рецепторов. Рецептор ноцицептина ORL1 может ингибироваться пилимом-1 более эффективно (IC50 198–214 нМ), чем цинк-НПВП (IC50 361–1093 нМ). В фенилхиноновом противоболевом тесте у крыс пилим-1 продемонстрировал немного больший процент анальгезии (44%; цинк-НПВП: 21–43%). Частота возникновения язв желудка при приеме в дозе 100 мг/кг перорально оценена в 35% (остальные молекулы – 75%). По сравнению с другими цинковыми производными НПВП пилим-1 минимально вмешивается в обмен витаминов и минералов.
Заключение. Хемореактомный анализ пилима-1 указывает на перспективы его применения как противовоспалительного препарата.
Что уже известно об этой теме?
► С 2014 г. в мире наблюдается рост числа программ искусственного интеллекта (ИИ) для смартфонов для раннего выявления злокачественных новообразований (ЗНО) кожи
► Отмечается высокая сменяемость таких программ ИИ для смартфонов из-за их недостаточной диагностической точности
► В России программы для смартфонов с использованием ИИ для диагностики опухолей кожи представлены недостаточно, а указания на их диагностическую и клиническую точность ограниченны или отсутствуют
Что нового дает статья?
► Программа ИИ Derma Onko Check для смартфона может быть использована при оказании первичной медико-санитарной помощи для дифференциальной диагностики доброкачественных новообразований (ДНО) и ЗНО кожи врачами общей практики и специалистами, не имеющими достаточных специальных знаний по дерматовенерологии и онкологии
► Программа Derma Onko Check является эффективным инструментом для дифференциальной диагностики между ДНО и ЗНО кожи различной тканевой принадлежности с высокими показателями диагностической точности (96%), чувствительности (98%) и специфичности (96%)
Как это может повлиять на клиническую практику в обозримом будущем?
► Врачи общей практики или другие специалисты, используя программы для ЭВМ (для смартфонов) с использованием ИИ, могут с высокой вероятностью проводить дифференциальную диагностику между ДНО и ЗНО кожи. Это улучшит качество ранней диагностики ЗНО кожи и ускорит направление таких пациентов к врачам-онкологам
Цель: оценить эффективность предварительной дифференциальной диагностики доброкачественных и злокачественных опухолей кожи на первичном врачебном приеме при оказании первичной медико-санитарной помощи с применением программы искусственного интеллекта (ИИ) Derma Onko Check для электронных вычислительных машин (приложение для смартфона).
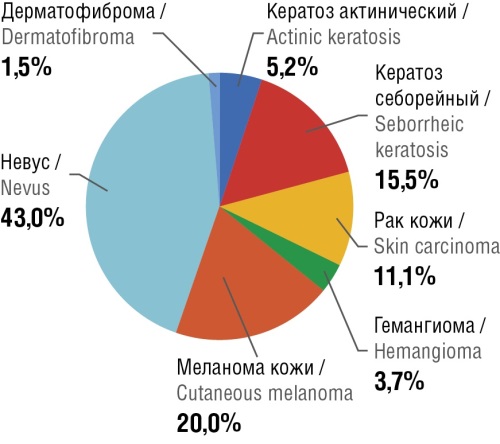
Материал и методы. Эффективность программы Derma Onko Check для визуальной идентификации доброкачественных и злокачественных опухолей кожи оценили у 135 пациентов в возрасте от 22 до 78 лет, которые имели различные образования кожи, визуально подозрительные на злокачественные. Заключение программы сравнивали с результатами дерматоскопического и морфологического методов исследования.
Результаты. Диагностическая точность программы Derma Onko Check при определении вероятности наличия у пациента доброкачественной или злокачественной опухоли кожи составила 96%, чувствительность – 98%, специфичность – 96%, доля ложноположительных результатов – 4,3%, доля ложноотрицательных результатов – 2,4%.
Заключение. Использование современных программ для электронных вычислительных машин на основе технологий ИИ дает возможность раннего выявления злокачественных опухолей кожи на первичном осмотре при оказании первичной медико-санитарной помощи, что особенно актуально в медицинских организациях и регионах с недостатком или отсутствием врачей-дерматологов и врачей-онкологов.
Что уже известно об этой теме?
► Биоимпеданс – это маркер морфологической конституции, своего рода «зеркало» обменных процессов в организме при различных патологиях
► Оценка биоимпеданса в клинической практике направлена на раннюю коррекцию неблагоприятных изменений состава тела
► Избыток жировой ткани, особенно висцеральной, потеря мышечной массы, негативные изменения водного баланса, снижение плотности костной ткани характерны для заболеваний почек
Что нового дает статья?
► Пациенты с хронической патологией почек (ХПП) характеризуются более пожилым возрастом, избыточной массой тела (что подтверждается показателями биоимпеданса и биохимического анализа крови), имеют более высокое артериальное давление и полиорганную патологию
► Показатель «тощая масса, кг» монотонно возрастает с ростом, массой тела, окружностью талии, внутриклеточной жидкостью, основным обменом, общей жидкостью и, наоборот, монотонно снижается с повышением активного сопротивления на частотах 5 и 50 кГц, реактивного сопротивления на 50 кГц
Как это может повлиять на клиническую практику в обозримом будущем?
► Перспективно изучить более подробно информативность и силу предикторов ХПП
► Важно проводить комплексную оценку эффективности различной терапии патологии почек в подгруппах пациентов с ХПП разной тяжести с учетом влияния на показатели импеданса
► Необходимо оценить эффективность различных подходов к терапии, роль физической нагрузки и обеспеченности микронутриентами (при наличии соответствующих данных)
Цель: на основании анализа взаимосвязей соматометрических (включая показатели биоимпеданса), биохимических и клинических показателей состояния пациентов с хронической патологией почек (ХПП) выявить потенциальные предикторы ХПП.
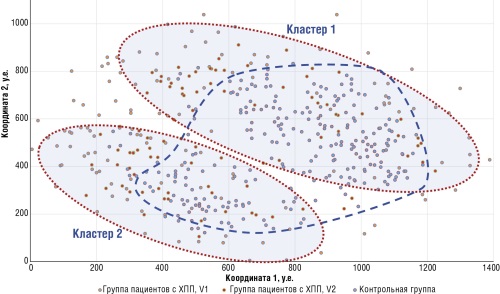
Материал и методы. Собраны значения 58 показателей, описывающих состояние 357 участников: 128 пациентов с ХПП и 229 участников контрольной группы (без патологии почек). Исследованы демографические, антропометрические, анамнестические данные (всего 19 диагнозов по Международной классификации болезней 10-го пересмотра), значения биоимпеданса, результаты общего и биохимического анализа крови (всего 19 показателей), показатели диеты по опроснику CINDI. Использованы новые математические подходы для установления интервалов информативных значений численных показателей, нахождения метрических сгущений в пространстве показателей биомедицинского исследования и построения метрических карт.
Результаты. В группе пациентов ХПП (основная группа) установлено преобладание более пожилых пациентов (средний возраст 54,1±13,1 года) по сравнению с контрольной группой (48,78±9,75 года), а также людей с избыточной массой тела (82,18±19 против 74,7±17,45 кг). У пациентов с ХПП наблюдаются нарушения обмена жировой ткани, снижение активного и реактивного сопротивления биоимпеданса, высокие значения систолического артериального давления, наличие полиорганной патологии.
Заключение. Анализ кластера взаимодействий показателей позволил сформулировать перспективные направления для дальнейших исследований: необходимо изучить более подробно информативность и «силу» предикторов ХПП, провести комплексную оценку эффективности терапии, выявить различия между подгруппами пациентов с различными нозологиями и стадиями ХПП, оценить эффективность различных подходов к терапии, а также роль физической нагрузки и обеспеченности микронутриентами.
ОБЗОРНЫЕ ПУБЛИКАЦИИ
Что уже известно об этой теме?
► Генитоуринарный синдром менопаузы (ГСМ) – термин, предложенный для обозначения ряда генитальных и мочевых симптомов, которые могут возникать во время и после менопаузы. Симптомы ГСМ могут появиться и раньше из-за противораковой терапии или двусторонней овариэктомии
► Симптомы ГСМ встречаются часто и включают сухость влагалища или вульвовагинальную атрофию (ВВА), дискомфорт и диспареунию, жжение и зуд, а также учащенное и неотложное мочеиспускание
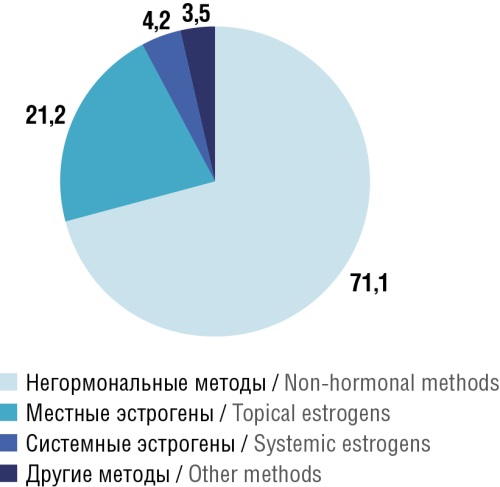
► Лечение первой линии состоит из негормональных методов (лубрикантов/увлажнителей). «Золотым стандартом» считается вагинальная терапия эстрогенами в минимальной эффективной дозе, однако существует ряд опасений по поводу лечения эстрогенами, начиная от неудобства вагинального введения и заканчивая развитием новообразований
Что нового дает статья?
► Несмотря на то что гормональная терапия является «золотым стандартом» лечения ГСМ, в лечении ВВА она обычно неэффективна – отчасти из-за симптоматического действия, в результате которого процесс инволюции возобновляется, как только прекращается введение гормонов
► Селективные модуляторы эстрогеновых рецепторов, такие как лазофоксифен и оспемифен, а также введение в схему лечения лактобактерий, витаминов D и E продемонстрировали положительное влияние на вагинальную ткань у женщин с симптомами ВВА
► Появляются такие перспективные методы лечения, как вагинальный дегидроэпиандростендион, вагинальный тестостерон и тканевые селективные эстрогеновые комплексы. В качестве альтернативных вариантов можно использовать новые терапевтические подходы с использованием лазерной терапии и инъекционных процедур в периуретральную область и стенки влагалища
Как это может повлиять на клиническую практику в обозримом будущем?
► Применение инъекционных материалов (аутологичная богатая тромбоцитами плазма, гиалуроновая кислота (ГК), препараты на основе несшитой ГК и гидроксиапатита кальция, микрофрагментированная жировая ткань, гибридные кооперативные комплексы гиалуронана, сшитая ГК, микрожировая и наножировая трансплантация) является эффективным методом лечения ГСМ
► У женщин с онкологическим анамнезом новые методы лечения (лазерная терапия, вагинальные инъекции) показывают многообещающие результаты с минимальными побочными эффектами и гормононезависимыми механизмами. Лечение должно быть индивидуальным на основе соотношения риска и пользы для каждой пациентки
► В отдельных случаях (при гормононезависимом РМЖ или при гормонозависимых опухолях, после завершения антигормональной адъювантной терапии) можно рассмотреть возможность использования вагинальных эстрогенов, которые следует назначать локально, в минимальной дозе и на ограниченный период времени до улучшения симптомов
Актуальность. Лечение вульвовагинальной атрофии (ВВА) у женщин с диагнозом гинекологического рака или рака молочных желез (РМЖ) является сложной задачей. Методы лечения ВВА как генитального проявления генитоуринарного синдрома менопаузы (ГСМ) обычно отражают подходы, используемые при естественной менопаузе, однако данные об эффективности и безопасности, характерные для этой группы пациенток, ограниченны из-за исключения их из клинических испытаний.
Цель: провести анализ литературных данных о новых подходах к терапии ВВА как проявления ГСМ у женщин с гинекологическим раком или РМЖ.
Материал и методы. Проведен поиск в базах данных PubMed/MEDLINE, Web of Science, eLibrary, Google Scholar, Scopus с использованием ключевых словосочетаний «вульвовагинальная атрофия», «вульварная атрофия после рака», «лечение вульварной атрофии у женщин с раком», «терапия низкими дозами эстрогенов», «лазерное лечение вульвовагинальной атрофии» на русском и английском языках. Также поиск выполняли по ключевым ссылкам из библиографий соответствующих исследований. В обзор включали оригинальные и обзорные статьи, содержащие указанные ключевые слова и опубликованные с 1996 г. по март 2025 г.
Результаты. У женщин с анамнезом гинекологического рака или РМЖ лечение ВВА должно быть индивидуализировано. Негормональные методы, а именно лубриканты при сексуальной активности и регулярное использование вагинальных увлажнителей длительного действия, обычно являются первой линией терапии. Фракционная лазерная терапия с применением CO2 представляет собой эффективный и безопасный метод для пациенток, переживших гинекологический рак, улучшая сексуальную функцию и качество жизни. Также в этой популяции использование гиалуроновой кислоты вместе с витаминами А и Е продемонстрировало положительный эффект, приводя к уменьшению сухости влагалища и диспареунии. Применение местной гормональной терапии может быть вариантом для пациенток, у которых нефармакологические и негормональные средства оказались неэффективны, после обсуждения рисков и преимуществ, а также консультации с онкологом.
Заключение. Не все доступные варианты лечения подходят для женщин с онкологическим анамнезом из-за опасности рецидива гормонозависимого рака, связанного с терапией эстрогенами. В данной популяции новые методы лечения, такие как лазерная терапия и вагинальные инъекции, показывают многообещающие результаты с минимальными побочными эффектами и гормононезависимыми механизмами.
Что уже известно об этой теме?
► IgA-нефропатия (IgA-Н) характеризуется неоднородным риском прогрессирования, который зависит от многих факторов. Несмотря на большое количество исследований, универсальные подходы к лечению IgA-Н с учетом риска ее прогрессирования не разработаны
► Высокий риск прогрессирования IgA-Н определяется как стойкая протеинурия (>1 г/сут ) несмотря на проведение оптимальной поддерживающей терапии на протяжении 3 мес
Что нового дает статья?
► Установлено, что наиболее значимыми предикторами прогрессирования IgA-Н являются протеинурия и артериальная гипертензия с учетом исходной функции почек
► Анализ гистологических изменений отдельных структур в пределах площади нефробиоптата в соответствии с классификацией MEST-C и сопоставление с клиническими данными повышают точность индивидуальной оценки риска прогрессирования IgA-Н
Как это может повлиять на клиническую практику в обозримом будущем?
► Разработка инструмента для оценки индивидуального риска прогрессирования IgA-Н с учетом клинических, гистологических данных и других маркеров-предикторов даст возможность определять изменяющийся риск для конкретного пациента на разных стадиях заболевания
► Создание общепринятой системы стратификации риска прогрессирования IgA-Н поможет оптимизировать и персонализировать лечение на ранних стадиях заболевания и улучшить долгосрочный прогноз
Иммуноглобулин А-нефропатия (англ. immunoglobulin A, IgA) является наиболее распространенной формой хронического гломерулонефрита и одной из ведущих причин терминальной почечной недостаточности. В настоящее время возможности точного прогнозирования риска прогрессирования данной патологии на уровне отдельных пациентов ограничены. В статье проведен анализ научной литературы, содержащей результаты исследований, посвященных определению независимых предикторов риска про грессирования IgA-нефропатии. Согласно результатам большинства исследований такие переменные, как протеинурия, артериальная гипертензия и исходная функция почек, имеют устойчивую и независимую связь с ухудшением почечного прогноза. Гистологические изменения в нефробиоптате выступают как отдельные предикторы. Сочетание морфологических и клинических данных позволяет повысить точность прогнозирования. Для улучшения результатов лечения и отдаленных исходов необходимы дальнейшие исследования, включая поиск новых биомаркеров и разработку общепринятой системы стратификации риска.

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.
ISSN 2070-4933 (Online)