Перейти к:
Принципы разработки стандартов медицинской помощи на основе клинических рекомендаций
https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.160
Аннотация
Цель: провести обзор законодательных и нормативных правовых актов, а также иных документов и рассмотреть изменение требований к разработке стандартов медицинской помощи и сложившуюся форму стандарта, определить ключевые принципы и методологию разработки стандартов медицинской помощи на основе клинических рекомендаций. Материал и методы. Рассмотрены положения Федерального закона от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», устанавливающие требования к разработке стандартов медицинской помощи. Проведен обзор порядка разработки стандартов (приказы Минздрава России (МЗ РФ) от 8 февраля 2018 г. № 53н и от 22 февраля 2022 г. № 103н). На примере стандартов медицинской помощи, утвержденных в 2021–2022 гг., рассмотрена форма стандарта. Выполнен обзор методических материалов, регламентирующих разработку стандартов медицинской помощи на основе клинических рекомендаций. Результаты. Порядок разработки стандартов медицинской помощи впервые был урегулирован в 2018 г. В настоящее время определены участники процесса (департаменты МЗ РФ, главные внештатные специалисты МЗ РФ, ФГБУ «Центр экспертизы и контроля качества медицинской помощи» МЗ РФ), их функции, а также регламентированы этапы и сроки разработки. Методология разработки стандартов медицинской помощи на основе клинических рекомендаций предусматривает формирование стандартизированных модулей медицинской помощи и математической модели. Заключение. В настоящее время процесс разработки стандартов медицинской помощи на основе клинических рекомендаций нормативно урегулирован и методология определена. Однако сохраняются вопросы, требующие дополнительного нормативного регулирования, такие как форма стандарта, методология проведения медико-экономической оценки. |
Ключевые слова
Для цитирования:
Ледовских Ю.А., Тишкина С.Н., Пирова Г.И., Семакова Е.В., Омельяновский В.В. Принципы разработки стандартов медицинской помощи на основе клинических рекомендаций. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023;16(1):5–16. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.160
For citation:
Ledovskikh Yu.A., Tishkina S.N., Pirova G.I., Semakova E.V., Omelyanovskiy V.V. Principles of medical care standards development based on clinical guidelines. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023;16(1):5–16. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.160
ВВЕДЕНИЕ / INTRODUCTION
Стандарты медицинской помощи и клинические рекомендации в соответствии с законодательством в сфере охраны здоровья граждан на сегодняшний день являются одними из основных документов, регулирующих вопросы организации и финансирования медицинской помощи [1].
Вопросы, связанные с местом и ролью стандартов в системе здравоохранения Российской Федерации (РФ), активно обсуждались в медицинском сообществе начиная с 2011 г. Дискуссия была обусловлена закреплением стандартов в качестве нормативных правовых актов [2] и последующими изменениями Федерального закона от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (далее – ФЗ-323), направленными на усиление роли клинических рекомендаций как основы для организации и оказания медицинской помощи в РФ [3]. При этом стандарты медицинской помощи в системе здравоохранения РФ сохраняют свою функцию экономического инструмента, позволяющего оценивать финансовую потребность на оказание медицинской помощи, в т.ч. в рамках Программы государственных гарантий бесплатного оказания гражданам медицинской помощи (ПГГ) [4].
Несмотря на то что начиная с 2012 г. стандарты являются нормативными правовыми актами, которые утверждаются приказами Министерства здравоохранения РФ (МЗ РФ) и проходят регистрацию в Министерстве юстиции РФ, процесс их разработки долгое время не был урегулирован, что тоже вызывало вопросы в медицинском сообществе [1][5]. Закрепление в ФЗ-323 законодательной нормы права о разработке стандартов медицинской помощи на основе клинических рекомендаций повысило актуальность конкретизации принципов разработки стандартов с учетом новых требований.
Цель – провести обзор законодательных и нормативных правовых актов, а также иных документов и рассмотреть изменение требований к разработке стандартов медицинской помощи и сложившуюся форму стандарта, определить ключевые принципы и методологию разработки стандартов медицинской помощи на основе клинических рекомендаций.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
В обзор законодательных и нормативных правовых актов включены ФЗ-323, приказы МЗ РФ от 8 февраля 2018 г. № 53н (далее – приказ № 53н) и от 22 февраля 2022 г. № 103н (далее – приказ № 103н) «Об утверждении порядка разработки стандартов медицинской помощи», стандарты медицинской помощи, утвержденные приказами МЗ РФ в 2021–2022 гг. и размещенные на официальном интернет-портале правовой информации1.
Проведен анализ методических материалов, размещенных на сайте ФГБУ «Центр экспертизы и контроля качества медицинской помощи» Минздрава России (ФГБУ «ЦЭККМП» МЗ РФ). Использованы методы сравнительного анализа, научного обобщения, контент-анализа.
РЕЗУЛЬТАТЫ / RESULTS
Изменения требований к разработке стандартов медицинской помощи / Changes in the requirements for the development of medical care standards
В 2011 г. с принятием ФЗ-323 были обозначены компоненты стандарта медицинской помощи (медицинские услуги, лекарственные препараты, медицинские изделия, имплантируемые в организм человека, компоненты крови, виды лечебного питания, включая специализированные продукты лечебного питания, иное) с указанием усредненных показателей частоты предоставления и кратности применения. Также в ФЗ-323 были установлены дополнительные требования для включения медицинских услуг и лекарственных препаратов. Для медицинских услуг дополнительным требованием является наличие в номенклатуре медицинских услуг [6]. Требованиями к препаратам являются наличие регистрации на территории РФ, соответствие инструкции по медицинскому применению препарата, соответствие фармакотерапевтической группе по анатомо-терапевтическо-химической классификации (АТХ), рекомендованной Всемирной организацией здравоохранения. Данные положения не изменялись и сохраняются в действующей редакции ФЗ-323.
С начала действия ФЗ-323 порядок разработки стандартов медицинской помощи долгое время не был урегулирован. Появлению в 2018 г. нормативного документа предшествовало внесение в ФЗ-323 дополнения о разработке стандартов медицинской помощи в установленном порядке [7]. После этого приказом № 53н был утвержден подзаконный нормативный правовой акт – порядок разработки стандартов медицинской помощи [8]. В дополнение к нормам ФЗ-323 о компонентах стандарта документ зафиксировал, что стандарт медицинской помощи состоит из паспортной и основной частей, а включение медицинских услуг, лекарственных препаратов и другого осуществляется с учетом наличия в клинических рекомендациях (протоколах лечения). Последующие изменения порядка разработки стандартов также были синхронизированы с изменениями ФЗ-323 (табл. 1).
Таблица 1. Изменения законодательных актов, регулирующих порядок разработки стандартов медицинской помощи
Table 1. Changes in legislative acts regulating the development of medical care standards
|
Законодательный акт / Legislative act |
Год / Year |
||
|
2018 |
2019 |
2022 |
|
|
Федеральный закон от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» / Federal Law of November 21, 2011, No. 323-FZ “On fundamentals of health care in the Russian Federation” |
Вступление в силу нормы о разработке стандартов медицинской помощи в соответствии с порядком, утвержденным уполномоченным органом исполнительной власти / Entry into force of the norm on the development of medical care standards in accordance with the procedure approved by the authorized executive body |
Вступление в силу нормы о разработке стандартов медицинской помощи на основе клинических рекомендаций / Entry into force of the norm on the development of medical care standards based on clinical guidelines |
Вступление в силу нормы, допускающей включение в стандарты медицинской помощи детям лекарственных препаратов, применяемых вне инструкции (офф-лейбл) / Entry into force of the norm allowing the inclusion of off-label medications into the medical care standards for children |
|
Порядок разработки стандартов медицинской помощи / Procedure for the development of medical care standards |
Издание приказа МЗ РФ № 53н «Об утверждении порядка разработки стандартов медицинской помощи» / Publication of the Order of the MH RF No. 53n "On approval of the procedure for medical care standards development” |
Внесение соответствующих изменений в порядок разработки стандартов / Introduction of appropriate amendments to the procedure for standards development |
Издание приказа МЗ РФ № 103н «Об утверждении порядка разработки стандартов медицинской помощи» / Publication of the Order of the MH RF No. 103n “On approval of the order of medical care standards development” |
Примечание. МЗ РФ – Министерство здравоохранения Российской Федерации.
Note. MH RF – Ministry of Health of the Russian Federation.
Так, с 1 января 2019 г. вступили в силу изменения в ФЗ-323, в которых содержалось прямое указание на разработку стандартов медицинской помощи на основе клинических рекомендаций, что было обусловлено законодательным определением клинических рекомендаций и их роли в системе здравоохранения РФ. В том же году данное положение было зафиксировано и в порядке разработки стандартов [9]. В 2022 г. вступила в силу ч. 14.1 ст. 37 ФЗ-323, допускающая включение в стандарты медицинской помощи детям лекарственных препаратов, применяющихся вне инструкции (офф-лейбл). Также в 2022 г. приказом № 103н был актуализирован и переутвержден порядок разработки стандартов [10].
С учетом произошедших изменений действующий порядок разработки стандартов (приказ № 103н) повторяет требования ФЗ-323 к разработке стандартов медицинской помощи, а также содержит положения, которые детализируют или дополняют федеральный закон. По сравнению с документом 2018 г. актуализированы требования к содержанию паспортной части стандарта, составу разработчиков и срокам разработки (табл. 2).
Таблица 2. Изменение требований порядка разработки стандартов медицинской помощи
Table 2. Changes in the requirements of the medical care standards development procedure
|
Порядок разработки стандартов, утвержденный приказом МЗ РФ № 53н / Standards development procedure approved by Order of the MH RF No. 53n |
Порядок разработки стандартов, утвержденный приказом МЗ РФ № 103н – действующий / Standards development procedure approved by Order of the MH RF No. 103n – valid |
Описание изменения / Description of changes |
|
Содержание паспортной части / Contents of the passport part |
||
|
– возрастная категория пациента / patient's age category – пол пациента / patient's gender – вид МП / type of MC – условия оказания МП / terms of MC – форма оказания МП / form of MC – фаза течения заболевания (состояния) / phase of the disease (condition) – стадия (или) степень тяжести заболевания (состояния) / stage (or) degree of severity of the disease (condition) – осложнение (при наличии) / complication (if any) – средняя продолжительность лечения законченного случая (количество дней) / average duration of treatment of a completed case (number of days) – нозологические единицы с указанием кода в соответствии с МКБ-10 / nosological entities with code according to ICD-10 |
– возрастная категория пациента / patient's age category – пол пациента / patient's gender – вид МП / type of MC – условия оказания МП / terms of MC – форма оказания МП / form of MC – средняя продолжительность лечения законченного случая (количество дней) / average duration of treatment of a completed case (number of days) – нозологические единицы с указанием кода в соответствии с МКБ-10 / nosological entities with code according to ICD-10 |
Исключены / Excluded: – фаза течения заболевания (состояния) / phase of the disease (condition) – стадия (или) степень тяжести заболевания (состояния) / stage (or) degree of severity of the disease (condition) – осложнение (при наличии) / complication (if any) |
|
Состав разработчиков / Composition of developers |
||
|
Основной разработчик не определен / The main developer is not defined Подавать предложения могут / Proposals may be submitted by: – главные внештатные специалисты МЗ РФ по профилю МП / MH RF chief external specialists of the MC profile; – органы государственной власти субъектов РФ / authorities of the constituent entities of the RF; – Федеральный фонд ОМС / Federal CHI Fund; – департаменты МЗ РФ / MH RF departments Организационное и методическое обеспечение, экспертиза, медико-экономическая оценка / Organizational and methodological support, expert review, medical and economic evaluation: – федеральное государственное бюджетное учреждение, находящееся в ведении МЗ РФ / Federal State Budgetary Institution under the jurisdiction of the MH RF Оценка / Evaluation: – департаменты МЗ РФ / MH RF departments |
Основной разработчик определен / The main developer is defined Предложения готовят / Proposals are prepared by: – главные внештатные специалисты МЗ РФ по профилю МП / MH RF chief external specialists of the МС profile Организационное и методическое обеспечение, медико-экономическая оценка / Organizational and methodological support, medical and economic evaluation: – федеральное государственное бюджетное учреждение, находящееся в ведении МЗ РФ / Federal State Budgetary Institution under the jurisdiction of the MH RF Оценка / Evaluation: – департаменты МЗ РФ / MH RF departments |
Основными разработчиками определены главные внештатные специалисты МЗ РФ по профилю медицинской помощи / The main developers are MH RF chief external specialists of the medical care profile |
|
Сроки разработки (с момента размещения клинических рекомендаций) / Development time (starting from the date of the clinical guidelines publication) |
||
|
Не более 6 мес / Not more than 6 months (в редакции 2019 г.; в первоначальной редакции не был установлен / as revised in 2019; not set in the original version) |
Не более 8 мес / Not more than 8 months |
Увеличение срока разработки / Extension of the development period |
Примечание. МЗ РФ – Министерство здравоохранения Российской Федерации; МП – медицинская помощь; ОМС – обязательное медицинское страхование; МКБ-10 – Международная статистическая классификация болезней и проблем, связанных со здоровьем, 10-го пересмотра.
Note. MH RF – Ministry of Health of the Russian Federation; MC – medical care; CHI – Compulsory Health Insurance; ICD-10 – International Statistical Classification of Diseases and Related Health Problems, 10th revision
В соответствии с действующим порядком разработки (приказ № 103н) стандарты медицинской помощи:
- состоят из паспортной и основной части, которые заполняются на основе сведений клинических рекомендаций, размещенных в Рубрикаторе МЗ РФ, и с использованием нормативных и иных документов;
- разрабатываются установленными участниками, за каждым из которых закреплены определенные функции, и в установленные сроки;
- подлежат оценке содержания и медико-экономической оценке.
Компоненты стандарта медицинской помощи. Документы, используемые при разработке
Стандарт медицинской помощи делится на паспортную и основную части. В паспортной части указываются возрастная категория, пол пациента, вид медицинской помощи, условия оказания медицинской помощи и ее форма, средняя продолжительность лечения, нозологические единицы с указанием кода в соответствии с Международной статистической классификацией болезней и проблем, связанных со здоровьем, 10-го пересмотра. В первоначальной редакции (приказ № 53н) перечень сведений паспортной части был шире за счет информации о фазе течения заболевания (состояния), стадии (или) степени тяжести заболевания (состояния), осложнении (при наличии) (см. табл. 2).
Требования к форме основной части стандарта для представления информации о медицинских услугах, лекарственных препаратах, медицинских изделиях, имплантируемых в организм человека, компонентах крови, видах лечебного питания, включая специализированные продукты лечебного питания, имеющие государственную регистрацию, нормативно не установлены. Состав информации основной части изначально был определен в ФЗ-323, и положения 2011 г. не менялись. Действующий порядок разработки стандартов (приказ № 103н) детализирует ФЗ-323 в части дополнительных условий включения медицинских услуг, лекарственных препаратов и другого, а также определяет перечень документов, используемых при разработке, на соответствие которым выполняется оценка стандарта медицинской помощи. Так, п. 8 приказа № 103н определяет, что в случае отсутствия в клинических рекомендациях международных непатентованных наименований (МНН) включение лекарственных препаратов осуществляется при одновременном соблюдении следующих условий:
- в клинических рекомендациях в тезисах-рекомендациях указана соответствующая группа АТХ;
- препарат относится к группе АТХ, указанной в клинических рекомендациях;
- препарат включается в стандарт медицинской помощи в соответствии с инструкцией по медицинскому применению.
Дополнительными условиями включения в стандарт медицинской помощи его компонентов является соответствие документам, используемым при разработке. Так, порядок разработки стандартов (приказ № 103н) регламентирует использование в работе нормативных и иных документов, на основе которых формируются паспортная часть с общей информацией и основная часть с перечнями медицинских услуг, лекарственных препаратов и т.д. (табл. 3).
Таблица 3. Нормативные и иные документы, используемые в качестве источника сведений при разработке стандарта медицинской помощи
Table 3. Regulations and other documents used as a source of information when developing a medical care standard
|
Компонент стандарта медицинской помощи / Part of medical care standard |
Источник сведений / Data source |
|
Паспортная часть / Passport part |
– Клинические рекомендации / Clinical guidelines – Международная статистическая классификация болезней и проблем, связанных со здоровьем / International Statistical Classification of Diseases and Related Health Problems |
|
Медицинские услуги / Medical services |
– Клинические рекомендации / Clinical guidelines – Номенклатура медицинских услуг / Catalogue for medical care services |
|
Лекарственные препараты / Drugs |
– Клинические рекомендации / Clinical guidelines – Инструкция по медицинскому применению лекарственного препарата / Instructions for medical use of the drug – Сведения о государственной регистрации лекарственных препаратов, содержащихся в государственном реестре лекарственных средств / Information on state registration of drugs contained in the State Drug Register – Анатомо-терапевтическо-химическая классификация / Anatomical Therapeutic Chemical Classification |
|
Медицинские изделия, имплантируемые в организм человека / Medical devices implanted in the human body |
– Клинические рекомендации / Clinical guidelines – Перечень медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи / List of medical devices implanted into human body while providing medical care within the framework of the program of state guarantees of free medical care to citizens |
|
Компоненты крови / Blood components |
– Клинические рекомендации / Clinical guidelines – Правила заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов / Rules of preparation, storage, transportation and clinical use of donor blood and its components |
|
Специализированные продукты лечебного питания, имеющие государственную регистрацию / State registered specialized products of therapeutic nutrition |
– Клинические рекомендации / Clinical guidelines – Сведения о государственной регистрации специализированных продуктов лечебного питания / Information on state registration of specialized therapeutic nutrition |
Примечание. МЗ РФ – Министерство здравоохранения Российской Федерации.
Note. MH RF – Ministry of Health of the Russian Federation.
Основным документом для формирования всех без исключения компонентов стандарта медицинской помощи, включая паспортную часть, являются клинические рекомендации, размещенные в Рубрикаторе МЗ РФ.
Состав разработчиков и сроки разработки
По сравнению с первоначальной версией порядка разработки стандартов (приказ № 53н) в составе участников произошли значительные изменения (см. табл. 2). Ранее подавать предложения могли главные внештатные специалисты (ГВС) МЗ РФ по профилю медицинской помощи, органы государственной власти субъектов РФ, Федеральный фонд обязательного медицинского страхования, департаменты МЗ РФ. Согласно действующему порядку разработки стандартов медицинской помощи (приказ № 103н) участниками процесса являются:
- ответственный департамент МЗ РФ, который инициирует начало разработки и готовит необходимые документы для утверждения стандарта, в т.ч. проект приказа;
- ГВС, которые по запросу МЗ РФ готовят предложения в стандарт;
- федеральное государственное бюджетное учреждение, находящееся в ведении МЗ РФ, которое осуществляет организационное и методическое обеспечение и проводит медико-экономическую оценку разработанного стандарта;
- департаменты МЗ РФ, которые выполняют оценку компонентов стандарта на соответствие требованиям.
В документе прописаны функции каждого участника, при этом предложения в стандарт медицинской помощи готовят главные внештатные специалисты МЗ РФ.
Предельный временной период на разработку стандарта медицинской помощи составляет 8 мес. Он считается от момента размещения на официальном сайте МЗ РФ соответствующих клинических рекомендаций и включает следующие этапы: формирование стандарта (не более 3 мес), проведение оценки и повторной оценки (в случае доработки) стандарта департаментами МЗ РФ (15 и 7 календарных дней соответственно), выполнение медико-экономической оценки стандарта (15 дней), а также подготовку и издание приказа МЗ РФ. В версии порядка разработки стандартов медицинской помощи 2019 г. предельный срок разработки составлял 6 мес, а в первоначальной версии (приказ № 53н) он не был установлен (см. табл. 2).
Оценка содержания и медико-экономическая оценка стандартов медицинской помощи
Включенные в стандарт медицинской помощи медицинские услуги, лекарственные препараты и другие компоненты подлежат оценке департаментами МЗ РФ в пределах компетенции. Количество параметров оценки различается в зависимости от оцениваемого компонента и обусловлено используемыми при разработке документами, перечень которых приведен в таблице 2. Так, имплантируемые медицинские изделия проверяются на соответствие перечню медицинских изделий [11]. При оценке лекарственных препаратов проверяются наличие государственной регистрации в государственном реестре лекарственных средств (ГРЛС), соответствие показаний и средних доз клиническим рекомендациям и инструкциям по медицинскому применению лекарственного препарата, соответствие АТХ.
Оценка стандартов медицинской помощи выполняется на этапе их подготовки. Сроки составляют 15 календарных дней для первичной оценки и 7 календарных дней – для повторной (в случае доработки стандарта). Оценка выполняется департаментами МЗ РФ одновременно, после представления стандарта в МЗ РФ.
Стандарты медицинской помощи, прошедшие оценку и согласование департаментами МЗ РФ, проходят медико-экономическую оценку, формат которой нормативно не регламентирован. Медико-экономическая оценка выполняется федеральным государственным бюджетным учреждением, находящимся в ведении МЗ РФ (ФГБУ «ЦЭККМП» МЗ РФ). Срок проведения оценки установлен в порядке разработки стандартов в 2022 г. и составляет 15 дней.
Кроме проведения медико-экономической оценки ФГБУ «ЦЭККМП» МЗ РФ осуществляет методическое и организационное обеспечение разработки стандартов медицинской помощи.
Форма стандарта медицинской помощи / The form of medical care standard
Форма представления сведений о компонентах стандарта медицинской помощи нормативно не закреплена. Несмотря на это, обзор утвержденных стандартов позволяет увидеть на практике реализацию принятых подходов к их разработке и сложившуюся форму стандарта.
Основная часть утвержденных стандартов медицинской помощи представляет собой отдельные таблицы-разделы с перечнями медицинских услуг, лекарственных препаратов, компонентов крови, медицинских изделий, имплантируемых в организм человека, видов лечебного питания, включая специализированные продукты лечебного питания. Нумерация разделов сквозная, и, как правило, разделы с медицинскими изделиями и видами лечебного питания могут иметь разную нумерацию в разных стандартах в зависимости от наличия или отсутствия других разделов.
Перечни медицинских услуг
Медицинские услуги указываются в двух разделах: «Медицинские услуги для диагностики заболевания, состояния» и «Медицинские услуги для лечения заболевания, состояния и контроля за лечением». Принцип разделения медицинских услуг по разделам не регламентирован нормативными или иными документами.
Разделы состоят из подразделов со сквозной нумерацией. Количество возможных подразделов в разделе «Медицинские услуги для диагностики заболевания, состояния» больше, чем в разделе «Медицинские услуги для лечения заболевания, состояния и контроля за лечением» (табл. 4).
Таблица 4. Перечень подразделов с медицинскими услугами в стандарте медицинской помощи
Table 4. List of subsections with medical services in the medical care standard
|
Подразделы раздела «Медицинские услуги для диагностики заболевания, состояния» / Subsections of the “Medical services for diagnostics of a disease, condition” section |
Подразделы раздела «Медицинские услуги для лечения заболевания, состояния и контроля за лечением» / Subsections of the “Medical services for treatment of a disease, condition, and treatment control” section |
|
Прием (осмотр, консультация) врача-специалиста / Medical appointment (examination, consultation) |
Прием (осмотр, консультация) и наблюдение врача-специалиста / Medical appointment (examination, consultation) and supervision by a specialist |
|
Лабораторные методы исследования / Laboratory test methods |
Лабораторные методы исследования / Laboratory test methods |
|
Инструментальные методы исследования / Instrumental methods of diagnosis |
Инструментальные методы исследования / Instrumental methods of diagnosis |
|
– |
Хирургические, эндоскопические, эндоваскулярные и другие методы лечения, требующие анестезиологического и/или реаниматологического сопровождения / Surgical, endoscopic, endovascular, and other methods of treatment requiring anesthesiology and/or resuscitation |
|
– |
Немедикаментозные методы профилактики, лечения и медицинской реабилитации / Non-medicinal methods of prevention, treatment, and medical rehabilitation |
Для медицинских услуг указываются код медицинской услуги, ее наименование, усредненные показатели частоты предоставления и кратности применения (рис. 1). Код медицинской услуги и ее наименование определяются в соответствии с номенклатурой медицинских услуг.

Рисунок 1. Пример представления медицинских услуг в стандарте медицинской помощи
Figure 1. An example of medical services presentation in a medical care standard
Перечень лекарственных препаратов
Лекарственные препараты представляются в разделе «Перечень лекарственных препаратов для медицинского применения, зарегистрированных на территории Российской Федерации, с указанием средних суточных и курсовых доз». Для них указываются код и наименование в соответствии с классификацией АТХ, наименование лекарственного препарата, усредненный показатель частоты предоставления, единицы измерения, средняя суточная доза (ССД) и средняя курсовая доза (СКД) (рис. 2).
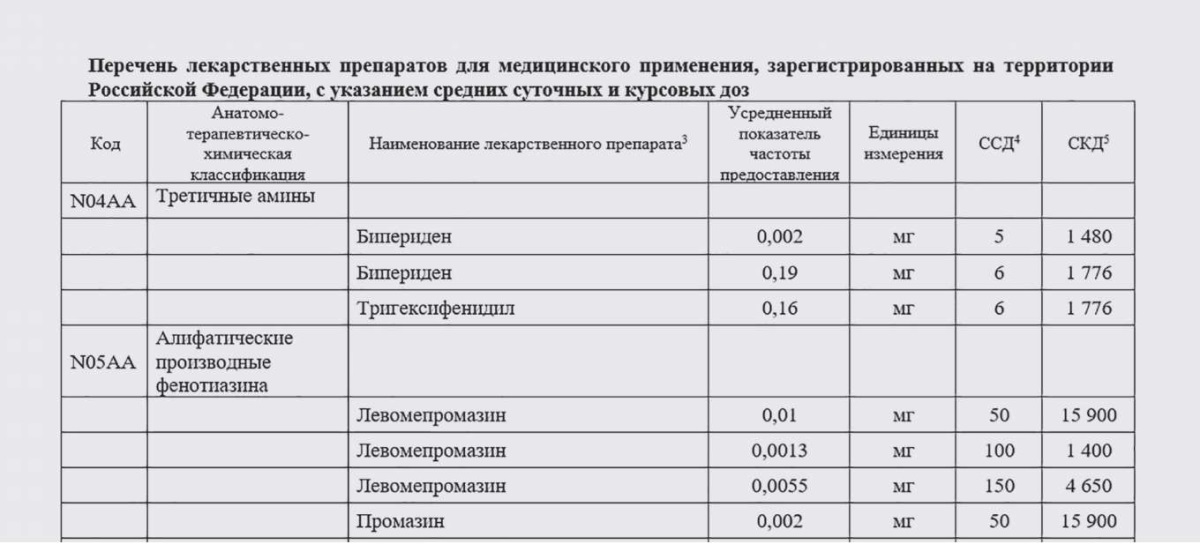
Рисунок 2. Пример представления лекарственных препаратов в стандарте медицинской помощи
Figure 2. An example of medications presentation in a medical care standard
В поле «Наименование лекарственного препарата» проставляется МНН, или группировочное, или химическое наименование препарата, а в случаях их отсутствия – торговое наименование.
В стандарты медицинской помощи один препарат может быть включен несколькими строками, если в разных клинических ситуациях он используется с разными ССД. В таком случае каждая ССД препарата будет указана отдельной строкой с отдельной СКД.
Перечень компонентов крови
Компоненты крови представляются в разделе «Компоненты крови». Для них указываются наименования в соответствии с Правилами заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов [12], усредненный показатель частоты предоставления, единицы измерения, ССД и СКД (рис. 3).
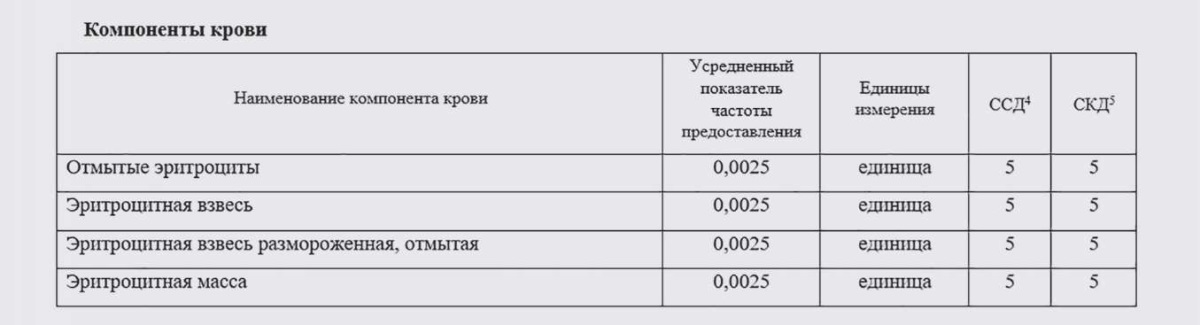
Рисунок 3. Пример представления компонентов крови в стандарте медицинской помощи
Figure 3. An example of blood components presentation in a medical care standard
Перечень медицинских изделий, имплантируемых в организм человека
Медицинские изделия, имплантируемые в организм человека, представляются в разделе «Перечень медицинских изделий, имплантируемых в организм человека». Для них в стандарте медицинской помощи указываются код и наименование вида медицинского изделия в соответствии с Перечнем медицинских изделий, имплантируемых в организм человека [11], усредненный показатель частоты предоставления и среднее количество (рис. 4).

Рисунок 4. Пример представления медицинских изделий, имплантируемых в организм человека, в стандарте медицинской помощи
Figure 4. An example of medical devices implanted in the human body presentation in a medical care standard
Перечень видов лечебного питания, включая специализированные продукты лечебного питания, имеющие государственную регистрацию
Лечебное питание и специализированные продукты лечебного питания представляются в отдельных подразделах: «Лечебное питание» и «Специализированные продукты лечебного питания».
Для лечебного питания в стандарте медицинской помощи указываются наименование вида, усредненный показатель частоты предоставления и количество (рис. 5).
Для специализированных продуктов лечебного питания указываются наименование вида, усредненный показатель частоты предоставления, единицы измерения, ССД и СКД (рис. 6).

Рисунок 5. Пример представления видов лечебного питания в стандарте медицинской помощи
Figure 5. An example of medical nutrition presentation in a medical care standard

Рисунок 6. Пример представления специализированных продуктов лечебного питания, имеющих государственную регистрацию, в стандарте медицинской помощи
Figure 6. An example of specialized therapeutic foods with state registration presentation in a medical care standard
Методология разработки стандартов медицинской помощи на основе клинических рекомендаций / Methodology for developing medical care standards based on clinical recommendations
В рамках организационного и методического обеспечения разработки стандартов медицинской помощи ФГБУ «ЦЭККМП» МЗ РФ сопровождает ГВС и их представителей при разработке стандартов.
В целях унификации подходов к разработке стандартов медицинской помощи и точности расчета усредненных показателей частоты предоставления и кратности применения медицинских услуг, лекарственных препаратов и других компонентов стандартов учреждением разработаны и размещены на официальном сайте методические рекомендации по разработке проектов стандартов [13].
Методические рекомендации определяют четыре этапа разработки стандартов медицинской помощи на основе клинических рекомендаций:
- анализ содержания клинических рекомендаций ГВС, их представителями и специалистами ФГБУ «ЦЭККМП» МЗ РФ, выделение описанных в клинических рекомендациях этапов, видов и методов диагностики, лечения и реабилитации;
- разработка для каждого метода диагностики, лечения и реабилитации стандартизированного модуля медицинской помощи – документа, по своей структуре схожего со стандартом и содержащего информацию о медицинских услугах, лекарственных препаратах и других компонентах медицинской помощи, описанных в клинических рекомендациях;
- формирование математической модели (схемы), которая позволяет оценить долю каждого стандартизированного модуля в составе стандарта;
- формирование по результатам этапов 1–3 агрегированного стандарта.
При разработке стандартизированных модулей и математической модели помимо информации из клинических рекомендаций используются статистические данные и экспертные оценки разработчиков стандарта медицинской помощи. Стандарт включает сведения из стандартизированных модулей и учитывает как усредненные показатели частоты предоставления и кратности применения отдельных компонентов стандартизированных модулей (медицинских услуг, лекарственных препаратов и др.), так и долю и кратность применения соответствующих стандартизированных модулей (а в ряде случаев и последовательность их применения), определенные математической моделью.
Стандарт медицинской помощи формируется на основе стандартизированных модулей и математической модели автоматически, с применением алгоритмов и информационных продуктов, разработанных ФГБУ «ЦЭККМП» МЗ РФ. В случае если после формирования стандарта возникает необходимость уточнения или корректировки перечней, усредненных показателей частоты применения и кратности предоставления его отдельных компонентов, требуется вернуться на предыдущие этапы и внести соответствующие изменения в стандартизированные модули и математическую модель (ручная корректировка итогового стандарта не допускается).
Стандартизированные модули и математическая модель разрабатываются ГВС и их представителями при методологической и организационной поддержке ФГБУ «ЦЭККМП» МЗ РФ. Стандарт медицинской помощи формируется ФГБУ «ЦЭККМП» МЗ РФ и согласовывается ГВС. При этом, несмотря на то что стандартизированные модули и математическая модель основываются на клинических рекомендациях, они могут содержать больше сведений, чем сформированный на их основе стандарт медицинской помощи. Дополнительные сведения необходимы для корректного расчета усредненных показателей частоты применения и кратности предоставления компонентов стандарта и могут быть также использованы для дальнейшего совершенствования клинических рекомендаций и расчета стоимости оказания медицинской помощи для случаев лечения, соответствующих стандартизированным модулям.
В случае если клиническими рекомендациями не предусмотрено разделение по возрастам пациентов (клинические рекомендации едины для взрослых и детей), то стандарты медицинской помощи, за редким исключением, формируются отдельно для детей и взрослых. Это обусловлено, в частности, порядками оказания медицинской помощи и процессом согласования стандартов.
Одним клиническим рекомендациям соответствует один стандарт медицинской помощи, за исключением случаев, когда клинические рекомендации описывают принципиально важные различия в популяции пациентов. При этом стандарты, разработанные на основе клинических рекомендаций, не разделяются по условиям оказания и видам медицинской помощи.
ОБСУЖДЕНИЕ / DISCUSSION
Принятие порядка разработки стандартов разрешило основные проблемы, возникающие при подготовке стандартов медицинской помощи. В то же время сохраняется ряд вопросов, требующих, на наш взгляд, дополнительного урегулирования.
В настоящее время стандарты медицинской помощи утверждаются по форме, в которой медицинские услуги разделены по двум разделам: «Медицинские услуги для диагностики заболевания, состояния» и «Медицинские услуги для лечения заболевания, состояния и контроля за лечением». Вместе с тем такое разделение законодательно не регламентировано, не имеет практической целесообразности и может приводить к неоднозначной трактовке как со стороны разработчиков стандарта на этапе его подготовки, так и со стороны медицинского сообщества и иных заинтересованных лиц на этапе его обсуждения или применения после утверждения. При этом для применения стандарта в качестве экономического инструмента планирования объемов и стоимости медицинской помощи при формировании ПГГ и территориальных программ государственных гарантий бесплатного оказания гражданам медицинской помощи, а не в качестве алгоритма лечения разделение медицинских услуг на разделы не требуется. В связи с этим представляется целесообразным изменение формы стандарта медицинской помощи путем объединения двух указанных разделов в единый раздел.
Результаты медико-экономической оценки стандартов медицинской помощи являются важной информацией для системы здравоохранения, т.к. оценка стоимости медицинской помощи в соответствии со стандартом позволяет оценить необходимую финансовую потребность на оказание медицинской помощи при внедрении клинических рекомендаций в систему здравоохранения вне зависимости от источников ее финансирования, предусмотренных ПГГ. В дополнение к нормативно закрепленным сроку и исполнителям проведения медико-экономической оценки следует также определить форму представления результатов медико-экономической оценки, которая будет учитывать стоимость стандарта в разрезе не только его компонентов, но и условий оказания медицинской помощи, что в дальнейшем позволит определять источники ее финансирования. В то же время разработка единого стандарта на заболевание без разделения по видам и условиям оказания медицинской помощи позволяет рассчитать усредненную стоимость оказания медицинской помощи на одного пациента в год для РФ и не ограничивает субъекты РФ, а дает им возможность адаптировать стандарты к региональным особенностям системы здравоохранения при формировании территориальных программ государственных гарантий бесплатного оказания гражданам медицинской помощи. При этом методика разработки стандартов на основе клинических рекомендаций посредством стандартизированных модулей и математической модели позволяет совершенствовать подходы к оплате медицинской помощи по клинико-статистическим группам, высокотехнологичной медицинской помощи и иным способам оплаты [14].
В настоящее время законодательно закреплено, что стандарты медицинской помощи разрабатываются на основе клинических рекомендаций. При этом имеется ряд ограничений к включению в стандарты методов диагностики, лечения или реабилитации, описанных в клинических рекомендациях. Например, отсутствие медицинских услуг в номенклатуре медицинских услуг и ограничение на включение лекарственных препаратов офф-лейбл в стандарты не позволяют в полной мере реализовать экономическую функцию стандартов медицинской помощи. При этом вопрос отсутствия медицинских услуг в номенклатуре может быть решен путем заблаговременной подачи ГВС, медицинскими организациями любой организационно-правовой формы собственности или медицинскими профессиональными некоммерческими организациями предложений по внесению или изменению медицинских услуг в номенклатуре, обусловленной описанием в клинических рекомендациях современных методов диагностики, лечения или реабилитации. Однако проблема включения лекарственных препаратов офф-лейбл в стандарты медицинской помощи на сегодняшний день не имеет однозначного решения. Внесение изменений в ФЗ-323 в части возможности включения лекарственных препаратов офф-лейбл в стандарты медицинской помощи детям для отдельных заболеваний решает проблему не в полной мере, т.к. вопрос актуален и для стандартов медицинской помощи взрослым. Поскольку клинические рекомендации являются документами, на основе которых должна организовываться и оказываться медицинская помощь, возможным путем решения проблемы может быть ужесточение требований к включению лекарственных препаратов офф-лейбл в клинические рекомендации и снятие законодательных ограничений на их включение в стандарты.
Кроме того, лекарственные препараты включаются в стандарты медицинской помощи с указанием МНН и средних доз, но без указания дополнительных характеристик. При этом для многих препаратов могут иметь как клиническую, так и экономическую значимость некоторые дополнительные характеристики, например путь введения. В ГРЛС для препаратов указывается лекарственная форма, но перечень лекарственных форм не закреплен законодательно и формулировка во многом зависит от производителя препарата. Различия между некоторыми лекарственными формами не видятся значимыми для целей стандартов медицинской помощи (например, таблетки или капсулы), некоторые особенности могут передаваться разными формулировками, имея одинаковый общий смысл (кишечнорастворимые или покрытые пленочной оболочкой). Вместе с тем от пути введения лекарственного препарата зависит не только его дозировка, имеющая клиническую значимость, но и стоимость. Таким образом, для более полного выполнения экономической функции стандарта видится целесообразным включение в форму стандарта медицинской помощи не лекарственной формы, но более общего понятия пути введения (например, перорально, внутривенно, внутримышечно и т.п.).
Законодательно закрепленная связь стандартов медицинской помощи и клинических рекомендаций позволяет включать в стандарты медицинские услуги, лекарственные препараты и другие компоненты в случае их описания в клинических рекомендациях. При этом расчетные усредненные показатели частоты предоставления и кратности применения компонентов стандарта зависят от этапа оказания медицинской помощи, клинической ситуации и популяции пациентов, для которых рекомендуется метод диагностики, лечения или реабилитации. В связи с этим наполнение стандартов зависит от полноты представления информации о применении методов диагностики, лечения и реабилитации в клинических рекомендациях.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Обзор законодательных актов показал, что долгое время процесс разработки стандартов медицинской помощи не был урегулирован, несмотря на то что с 2012 г. они являлись одними из основных документов, регулирующих оказание медицинской помощи в РФ. Порядок их разработки был определен нормативными правовыми актами только в 2018 г. Изменения законодательства в части определения роли клинических рекомендаций в системе здравоохранения и закрепление положения о разработке стандартов медицинской помощи на основе клинических рекомендаций потребовали актуализации нормативных правовых актов, которые в еще большей степени структурировали процесс разработки стандартов и определили его основные принципы.
В настоящее время нормативными актами обозначены компоненты стандарта медицинской помощи и требования к ним, определены участники процесса, их функции, сроки разработки стандарта, включая отдельные этапы, регламентирована необходимость оценки стандарта департаментами МЗ РФ и медико-экономической оценки. В то же время сохраняются вопросы, требующие дополнительного нормативного регулирования, такие как форма стандарта медицинской помощи, методология проведения медико-экономической оценки.
1. http://pravo.gov.ru/.
Список литературы
1. Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации». URL: http://www.consultant.ru/document/cons_doc_LAW_121895/ (дата обращения 10.11.2022).
2. Найговзина Н.Б., Филатов В.Б., Бороздина О.А., Николаева Н.А. Стандартизация в здравоохранении. Преодоление противоречий законодательства, практики, идеи. М.: ГЭОТАР-Медиа; 2015: 208 с.
3. Ковалева М.Ю., Сухоруких О.А. Клинические рекомендации. История создания и развития в Российской Федерации и за рубежом. Ремедиум. 2019; 1–2: 6–14. https://doi.org/10.21518/15615936-2019-1-2-6-14.
4. Ледовских Ю.А., Семакова Е.В., Авксентьева М.В. Подходы к формированию программы государственных гарантий бесплатного оказания гражданам медицинской помощи с применением стандартов медицинской помощи. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2017; 10 (4): 53–60. https://doi.org/10.17749/2070-4909.2017.10.4.053-060.
5. Стародубов В.И., Ефремова Т.А., Коробов Н.В., Лошаков Л.А. Стандарты медицинской помощи в системе здравоохранения Российской Федерации: состояние и перспективы. Здравоохранение Российской Федерации. 2015; 59 (4): 4–9.
6. Приказ Минздрава России от 13.10.2017 № 804н «Об утверждении номенклатуры медицинских услуг». URL: http://www.consultant.ru/document/cons_doc_LAW_282466/ (дата обращения 10.11.2022).
7. Федеральный закон от 29.07.2017 № 242-ФЗ «О внесении изменений в отдельные законодательные акты Российской Федерации по вопросам применения информационных технологий в сфере охраны здоровья». URL: http://www.consultant.ru/document/cons_doc_LAW_221184/ (дата обращения 10.11.2022).
8. Приказ Минздрава России от 08.02.2018 № 53н «Об утверждении порядка разработки стандартов медицинской помощи». URL: http://www.consultant.ru/document/cons_doc_LAW_299614/ (дата обращения 10.11.2022).
9. Приказ Минздрава России от 28.06.2019 № 472н «О внесении изменений в Порядок разработки стандартов медицинской помощи, утвержденный приказом Министерства здравоохранения Российской Федерации от 8 февраля 2018 г. № 53н». URL: http://www.consultant.ru/document/cons_doc_LAW_333473/ (дата обращения 10.11.2022).
10. Приказ Минздрава России от 22.02.2022 № 103н «Об утверждении порядка разработки стандартов медицинской помощи». URL: http://www.consultant.ru/document/cons_doc_LAW_418539/ (дата обращения 10.11.2022).
11. Распоряжение Правительства РФ от 31.12.2018 № 3053-р «Об утверждении перечня медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, а также перечня медицинских изделий, отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг». URL: http://www.consultant.ru/document/cons_doc_LAW_315495/ (дата обращения 10.11.2022).
12. Постановление Правительства РФ от 22.06.2019 № 797 «Об утверждении Правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов и о признании утратившими силу некоторых актов Правительства Российской Федерации». URL: http://www.consultant.ru/document/cons_doc_LAW_328029/ (дата обращения 10.11.2022).
13. Методические рекомендации по разработке проектов стандартов медицинской помощи (новая редакция). ФГБУ «ЦЭККМП» Минздрава России. 2022. URL: https://rosmedex.ru/standarts (дата обращения 10.11.2022).
14. Ледовских Ю.А., Семакова Е.В., Омельяновский В.В. Методика формирования клинико-статистических групп заболеваний на основе клинических рекомендаций с использованием стандартизированных модулей медицинской помощи. Медицинские технологии. Оценка и выбор. 2019; 3: 8–15.
Об авторах
Ю. А. ЛедовскихРоссия
Ледовских Юлия Анатольевна – к.м.н., начальник отдела методического обеспечения стандартизации
Хохловский пер., д. 10/5, Москва 109028
С. Н. Тишкина
Россия
Тишкина Светлана Николаевна – заместитель начальника отдела методического обеспечения стандартизации
Хохловский пер., д. 10/5, Москва 109028
Г. И. Пирова
Россия
Пирова Гунель Ифтихаровна – главный специалист отдела методического обеспечения стандартизации
Хохловский пер., д. 10/5, Москва 109028
Е. В. Семакова
Россия
Семакова Евгения Васильевна – заместитель начальника отдела методического обеспечения стандартизации
Хохловский пер., д. 10/5, Москва 109028
В. В. Омельяновский
Россия
Омельяновский Виталий Владимирович – д.м.н., профессор, генеральный директор; руководитель Центра финансов здравоохранения; заведующий кафедрой организации здравоохранения и общественного здоровья с курсом оценки технологий здравоохранения; главный научный сотрудник отдела экономических исследований в здравоохранении
Хохловский пер., д. 10/5, Москва 109028
Настасьинский пер., д. 3, стр. 2, Москва 127006
ул. Баррикадная, д. 2, стр. 1, Москва 123995
ул. Воронцово поле, д. 12, стр. 1, Москва 105064
WoS ResearcherID: P-6911-2018; Scopus Author ID: 6507287753
Рецензия
Для цитирования:
Ледовских Ю.А., Тишкина С.Н., Пирова Г.И., Семакова Е.В., Омельяновский В.В. Принципы разработки стандартов медицинской помощи на основе клинических рекомендаций. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023;16(1):5–16. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.160
For citation:
Ledovskikh Yu.A., Tishkina S.N., Pirova G.I., Semakova E.V., Omelyanovskiy V.V. Principles of medical care standards development based on clinical guidelines. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023;16(1):5–16. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.160

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.






































