Перейти к:
Совершенствование эффективности системы лекарственного обеспечения пациентов со злокачественными новообразованиями
https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.137
Аннотация
Актуальность. Одной из приоритетных задач здравоохранения во всем мире является сохранение оптимального баланса между затратами ресурсов и доступностью эффективной медицинской помощи. Существующий подход к оказанию лекарственной помощи пациенту с онкологическим заболеванием ограничивает своевременность и доступность лечения. Для государства, в свою очередь, логистика лекарственного обеспечения (ЛО) подразумевает колоссальные затраты, которые, однако, не являются рациональными.
Цель: оценить потребности в финансировании полного перевода финансового обеспечения медицинской помощи по профилю «онкология» в систему обязательного медицинского страхования (ОМС) путем оптимизации функций дневного стационара (ДС).
Материал и методы. В ходе исследования для достижения цели путем устранения несвойственных функций ДС проанализированы нормативные правовые документы, регулирующие лекарственную помощь и ЛО в Российской Федерации, данные деперсонифицированных (обезличенных) реестров структуры госпитализаций в ДС за 2021 г. По результатам анализа с использованием методов экспертных оценок, математического моделирования, а также изучения литературных данных разработана модель для оценки потребности в финансировании полного перевода ЛО в систему ОМС, в т.ч. с учетом скрытого дефицита.
Результаты. Общий объем средств, высвобождаемых от сокращения нерациональных госпитализаций в условиях ДС, составил 2,08% от уровня финансирования анализируемых схем. Учитывая данные о госпитализациях в ДС за 2021 г., количество нерациональных госпитализаций при переводе выбранных схем в амбулаторный этап снизится на 16,1%. Перевод всей лекарственной терапии на финансирование из средств ОМС потребует значительных дополнительных бюджетных расходов в размере 62,5 млрд руб., или 2,65% от общих расходов Программы государственных гарантий бесплатного оказания гражданам медицинской помощи (ПГГ).
Заключение. Несмотря на аргументированность предложенных изменений в области совершенствования ЛО онкологических пациентов и выявленные основания для изменения распределения финансовых средств внутри ПГГ, существуют затруднения, определяющие необходимость согласованного рассмотрения вопросов оказания лекарственной помощи.
Ключевые слова
Для цитирования:
Агафонова Ю.А., Федяев Д.В., Снеговой А.В., Омельяновский В.В. Совершенствование эффективности системы лекарственного обеспечения пациентов со злокачественными новообразованиями. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022;15(2):209-220. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.137
For citation:
Agafonova Yu.A., Fedyaev D.V., Snegovoy A.V., Omelyanovskiy V.V. Improving the efficiency of the medicine provision system for patients with malignant neoplasms. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2022;15(2):209-220. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.137
ВВЕДЕНИЕ / INTRODUCTION
Медико-демографические показатели злокачественных новообразований отражают различия в распределении факторов риска, степень экономического развития страны, социальные факторы, образ жизни населения, доступность оказания медицинской помощи, включая лекарственное обеспечение (ЛО) [1].
Cогласно статистическим данным Федеральной службы государственной статистики о заболеваемости злокачественными новообразованиями за 2020 г. отмечено снижение количества выявленных случаев до 1 440 090, что на 300 тыс. меньше показателя предыдущего года. Подобная тенденция ожидаема во всем мире и ассоциирована с коронавирусом SARS-CoV-2, вызвавшим продолжающуюся с 2019 г пандемию COVID-19 (COronaVIrus Disease 2019). Предполагается, что за краткосрочным снижением заболеваемости злокачественными новообразованиями на пике пандемии последует увеличение числа выявленных на поздних стадиях случаев и рост показателей смертности [2, 3].
Однако для онкологических заболеваний наиболее значимы данные общей выживаемости, являющиеся ключевым показателем эффективности онкологических служб [4, 5]. В исследовании CONCORD-3 были проанализированы медицинские записи 37,5 млн пациентов с выявленным злокачественным новообразованием за 15-летний период. Данные были предоставлены из 71 страны, 47 из которых передали сведения со 100% охватом населения. Показатель 5-летней выживаемости при раке легкого составил 33% в Японии и 4% в Индии. При раке молочной железы аналогичный показатель составил 90% и 40% в США и Южной Африке соответственно [6]. Таким образом, логично и обоснованно утверждение, что в странах, где приоритетом является доступность эффективной медицинской помощи, в т.ч. для онкологических пациентов, включая предоставление противоопухолевых препаратов, наблюдаются самые высокие целевые показатели [6, 7].
Вместе с тем эффективная медицинская помощь требует ресурсов. Для системы здравоохранения США в 2010 г. стоимость онкологической помощи оценивалась почти в 125 млрд долл. с ростом до 160 млрд долл. к 2020 г. [8]. Однако показатель, прогнозируемый в 2020 г., был значительно преувеличен уже в 2015 г. и составил 183 млрд долл. В настоящее время прогноз на 2030 г. составляет 246 млрд долл. по данным Сети противораковой борьбы Американского онкологического общества (англ. American Cancer Society Cancer Action Network) [9]. По данным за 2018 г., при оценке стоимости лечения онкологических заболеваний, а также доступа к лекарственной терапии для пациентов со злокачественными новообразованиями в Европе расходы здравоохранения на лечение составили 103 млрд евро, из которых 32 млрд евро были потрачены на обеспечение противоопухолевой лекарственной терапией (ПОЛТ). При этом расходы на лекарственную терапию более чем утроились – с 10 до 32 млрд евро в период с 2005 по 2018 гг. [10]. По этой причине одной из приоритетных задач здравоохранения во всем мире является сохранение оптимального баланса между затратами ресурсов и доступностью эффективной медицинской помощи.
В Российской Федерации (РФ) затраты на онкологическую помощь разделены в зависимости от условий оказания медицинской помощи. Источником финансирования стационарной медицинской помощи, оказываемой в условиях круглосуточного (КС) или дневного (ДС) стационара, являются средства фонда обязательного медицинского страхования (ОМС) в рамках базовой программы ОМС, которые за период 2021 г. составили 303,3 млрд руб., в т.ч. 135 млрд руб. в рамках Федерального проекта «Борьба с онкологическими заболеваниями»1. В 2020 г. финансовое обеспечение медицинской помощи пациентам со злокачественными новообразованиями составило 271,3 млрд руб., в т.ч. 115 млрд руб. в рамках межбюджетного трансферта из федерального бюджета. Согласно данным отчета Федерального фонда ОМС за 2020 г. наибольшее использование субвенций в разрезе типов лечения приходится на проведение ПОЛТ – 74,5% от объема использованных средств [11].
Однако данные затраты все же не покрывают всей потребности в применении ПОЛТ на всех этапах оказания медицинской помощи, т.к. источником финансирования амбулаторной медицинской помощи являются средства федерального бюджета и средства бюджета субъекта. При этом ЛО онкологических пациентов на амбулаторном этапе в большинстве случаев осуществляется и регулируется перечнем региональной льготы, что не позволяет полностью обеспечить доступность ПОЛТ. Механизм регионального или федерального финансирования накладывает на процесс льготного ЛО определенные ограничения, такие как недостаточность региональных средств на приобретение дорогостоящих современных противоопухолевых препаратов или длительность процесса закупки за счет федеральных средств, что подтверждается ежегодными отчетами Росздравнадзора: 26,5% от общего количества обращений составляют обращения по вопросам обеспечения лекарственными препаратами (ЛП) и медицинскими изделиями, из них 66% составляют вопросы по отсутствию необходимых ЛП [12]. Таким образом, ввиду нестабильности финансирования амбулаторного этапа ЛО ряду субъектов наиболее практично маршрутизировать пациентов для получения лекарственной терапии из амбулаторного звена в условия ДС, что противоречит принципам преемственности оказания медицинской помощи.
Одним из направлений совершенствования системы оказания медицинской помощи онкологическим пациентам в РФ является путь устранения несвойственных функций ДС путем перевода части ПОЛТ в амбулаторные условия с последующим переводом всей амбулаторной помощи на финансирование из средств ОМС. В настоящее время обеспечение онкологических пациентов в РФ пероральными ЛП, применяемыми в монорежиме или в составе комбинированного лечения, входит в оказание медицинской помощи в условиях ДС. Данные схемы не требуют специальных условий при получении ЛП, навыков и наблюдения за пациентом. Такой подход к оказанию лекарственной помощи не является рациональным ни с позиции пациента, вынужденного получать препарат ежедневно при обязательном наблюдении в стационаре, ни с позиции врача (онкологи обязаны проводить необоснованные осмотры с ведением документации при ежедневной выдаче таблетированных ЛП).
Цель – оценить потребности в финансировании полного перевода финансового обеспечения медицинской помощи по профилю «онкология» в систему ОМС путем оптимизации функций дневного стационара.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
Для достижения поставленной цели были поэтапно решены следующие задачи: 1) экспертная оценка отбора схем ПОЛТ, проведение которых возможно осуществлять в амбулаторных условиях; 2) анализ стоимости схем на основе структуры госпитализаций для выполнения ПОЛТ в ДС за 2021 г.; 3) оценка изменения размеров финансирования ПОЛТ в ДС на основе данных о частоте применения схем ПОЛТ и параметров Программы государственных гарантий бесплатного оказания гражданам медицинской помощи (ПГГ)2.
В ходе исследования проведен анализ действующих нормативных правовых актов, регулирующих лекарственную помощь и ЛО в РФ, выполнен ретроспективный анализ деперсонифицированных (обезличенных) реестров структуры госпитализаций за 2021 г. по медицинской помощи, оказанной в условиях ДС. Применены методы экспертных оценок, анализа данных публикаций по исследуемой теме, а также метод математического моделирования. Написание статьи было выполнено в соответствии с рекомендациями стандарта отчетности для исследований в здравоохранении SQUIRE 2.0 [13].
1-й этап / Stage 1
Проведен анализ Приложения 9 «Расшифровка клинико-статистических групп заболеваний для оплаты медицинской помощи, оказанной в условиях дневного стационара»3, на основе данных которого выполнено последующее исследование. Из справочника схем лекарственной терапии при злокачественных новообразованиях (кроме лимфоидной и кроветворной тканей) «Схемы лекарственной терапии», содержащегося в Приложении 9, выделены схемы, проведение которых целесообразно осуществлять в амбулаторных условиях.
Принцип отбора схем лекарственной терапии включал следующие критерии:
- схема содержит один или несколько ЛП с пероральным способом применения;
- схема содержит ЛП с пероральным способом применения и ЛП, не требующий при введении специальных условий, навыков и наблюдения за пациентом, вводимый однократно за курс во время посещения врача;
- ЛП, входящий в схему, применяется длительно (таким образом, было принято, что количество дней проведения в тарифе для схемы лекарственной терапии должно составлять 21 и более);
- в инструкциях по медицинскому применению ЛП, входящего в схему, размещенных в Государственном реестре лекарственных средств4, не содержится сведений об условиях применения ЛП, включая данные об обязательном его применении в условиях КС или ДС.
При соблюдении каждого из вышеперечисленных критериев схема лекарственной терапии была включена в последующий анализ. Следует отметить, что оценка отбора проведена в ходе междисциплинарной работы с привлечением к консультации онкологов и специалистов в области организации здравоохранения.
Допущения и ограничения 1-го этапа
В Приложении 9 содержится ряд схем, количество дней проведения которых в тарифе составляет менее 21 дня, либо ЛП имеет не пероральный способ применения, а вводится подкожно или внутривенно, однако его применение в условиях ДС в настоящее время является дискутабельным в экспертном сообществе. Вместе с тем, учитывая наибольшую важность схем ПОЛТ, требующих ежедневного длительного перорального приема ЛП, а также возможности совершенствования функций ДС и улучшения качества жизни пациентов при их применении, в последующую работу нами были взяты только схемы, соответствующие вышеперечисленным критериям.
В случае указания в инструкции особых условий с необходимостью врачебного контроля за проведением лечения и наблюдения специалиста без указаний на необходимость лечения в условиях ДС или КС схема лекарственной терапии с включением ЛП, содержащих вышеперечисленные особые условия, также выделена в перечень схем лекарственной терапии, проведение которых целесообразно осуществлять в амбулаторных условиях. Проведение ПОЛТ амбулаторно не противоречит особым указаниям в инструкции на необходимость врачебного контроля за проведением лечения и наблюдения специалиста, т.к. амбулаторный прием ПОЛТ, так же как и прием в условиях стационара, обязательно сопровождается контролем врачебного персонала, включая контроль лабораторных и инструментальных показателей независимо от условий оказания медицинской помощи. Такой контроль равным образом может осуществляться с применением телемедицинских технологий согласно ст. 36.2. «Особенности медицинской помощи, оказываемой с применением телемедицинских технологий» Федерального закона от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации».
2-й этап / Stage 2
Проведен анализ стоимости схем в ДС за 2021 г. Стоимость одного случая проведения ПОЛТ у взрослых со злокачественными новообразованиями определяется с учетом данных следующих показателей (согласно разделу «Особенности оплаты случаев проведения лекарственной терапии злокачественных новообразований у взрослых»):
- размер средней стоимости законченного случая лечения без учета коэффициента дифференциации (базовая ставка);
- коэффициент относительной затратоемкости по клинико-статистической группе (КСГ), к которой отнесен данный случай госпитализации;
- доля заработной платы и прочих расходов в структуре стоимости КСГ (установленное Приложением 3 к ПГГ значение, к которому применяется коэффициент дифференциации);
- коэффициент дифференциации, рассчитанный в соответствии с Постановлением № 4625.
На основе приведенных показателей выполнен расчет оплаты случаев осуществления лекарственной терапии с включением схем ПОЛТ, проведение которых возможно осуществить в амбулаторных условиях.
С помощью реестров госпитализаций в ДС за 2021 г., находящихся в распоряжении авторов, оценивали структуру распределения проведения схем ПОЛТ в общем объеме случаев оказания медицинской помощи пациентам с онкологическими заболеваниями в условиях ДС. На основе структуры схем ПОЛТ, нормативов объемов и финансирования ПГГ рассчитывали объемы финансирования, использованные для анализа доли финансирования схем ПОЛТ, проведение которых возможно осуществлять в амбулаторных условиях.
3-й этап / Stage 3
Проведена оценка изменения размеров финансирования ПОЛТ в ДС на основе данных о частоте применения схем ПОЛТ и параметров ПГГ. Анализ влияния разработанных предложений на реализацию ПГГ осуществляли методом математического моделирования в среде Excel (Microsoft, США). В рамках модели расчет снижения затрат от сокращения финансирования проведения ПОЛТ в условиях ДС выполняли путем определения разницы текущего уровня затрат на каждую схему и моделируемого, рассчитанного путем сокращения доли нелекарственных затрат. Объем сокращения финансирования определяли с учетом количества случаев госпитализации по каждой схеме.
Для оценки изменения размеров финансирования ПОЛТ в ДС на основе данных о частоте применения схем ПОЛТ и параметров ПГГ были рассчитаны объемы и уровень финансирования в рамках ПГГ на 2021 г. Отдельно расчет проводили при учете возможного перевода федеральной и региональной льготы на ОМС и роста спроса на 30%, т.к., по данным экспертов, скрытый неудовлетворенный спрос в ЛО может достигать 30% от существующего объема потребления.
Допущения и ограничения 3-го этапа
Расчет снижения затрат после перевода части схем ПОЛТ из условий ДС проводили путем определения разницы текущего уровня затрат на каждую схему и моделируемого, рассчитанного путем сокращения доли нелекарственных затрат. Помимо данной методологии вычисления могут быть выполнены иначе – например, путем расчета себестоимости по каждой схеме ПОЛТ. Однако в данном исследовании была выбрана указанная методология в силу транспарентности данных, на основе которых проводилось дальнейшее исследование. Альтернативные подходы к построению моделей, вероятно, могут привести к изменениям в итоговых расчетах.
Действующей особенностью ПГГ 2021 г. является выделение федерального компонента программы. При этом ее федеральная и региональная составляющие равнозначны, и особенности использования схем ПОЛТ в зависимости от источников финансирования определить без данных 2021 г. не представляется возможным. Вследствие этого анализ влияния на уровень госпитализации и финансирования проведен на региональном компоненте ПГГ.
Полный перевод ЛО онкологических пациентов в систему ОМС подразумевает отказ от федеральной и региональной льгот. Объем расходов по льготе, по сведениям мониторинга Росздравнадзора, за 2020 г. составил 40,5 млрд руб6. Перевод всех расходов на одноканальную систему ОМС с соответствующим финансовым обеспечением может способствовать росту доступности медицинской помощи и, как следствие, реализации существующего неудовлетворенного спроса в ЛО онкологических пациентов. Оценить скрытый неудовлетворенный спрос в рамках настоящего исследования не представляется возможным.
РЕЗУЛЬТАТЫ / RESULTS
Экспертная оценка отбора схем противоопухолевой лекарственной терапии, проведение которых возможно осуществлять в амбулаторных условиях / Expert evaluation of the selection of antitumor drug therapy regimens, which can be carried out on an outpatient basis
По результатам 1-го этапа исследования общий объем отобранных для анализа схем составил 21,7% от всех схем ПОЛТ, входящих в список применяемых в ДС (181 схема) (табл. 1). Общий объем случаев, подпадающих под возможность перевода в амбулаторное звено, – 14,39% от объема случаев ПОЛТ, проводимой в условиях ДС. Интервал расходов непосредственно на ЛП в структуре тарифа составил от 70,61% (ds19.039) до 99,68% (ds19.048).
Таблица 1. Результаты отбора схем противоопухолевой лекарственной терапии, проведение которых возможно осуществлять в амбулаторных условиях
Table 1. The results of the selection of antitumor drug therapy regimens, which can be carried out on an outpatient basis
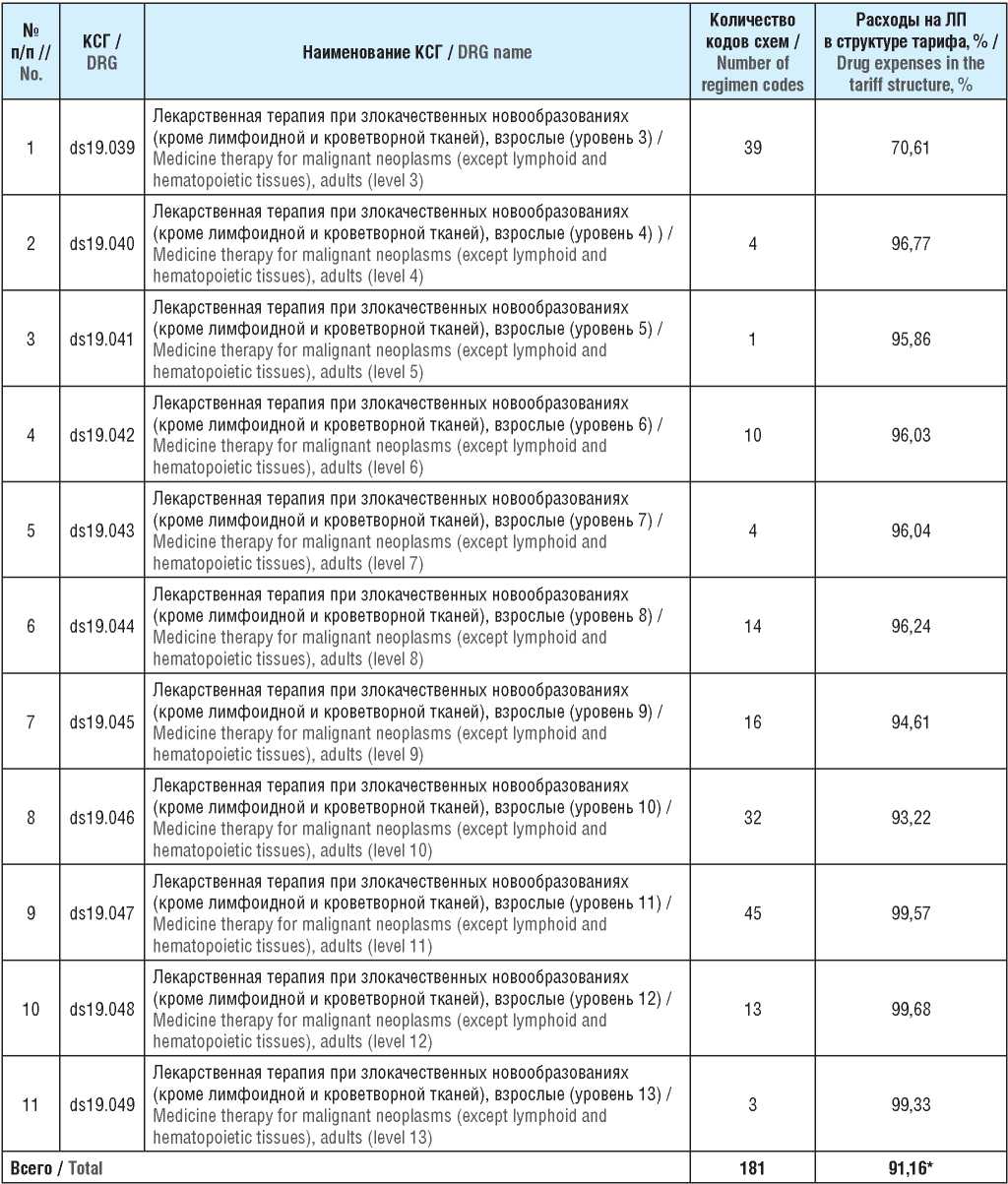
Примечание. КСГ – клинико-статистическая группа; ЛП – лекарственный препарат. * Средневзвешенный показатель.
Note. DRG – diagnosis-related group. * Mean weighted value.
Анализ стоимости схем на основе реестров структуры госпитализаций в дневной стационар за 2021 год / Analysis of the cost of schemes based on the registers of the structure of hospitalizations in a day hospital for 2021
На 2-м этапе исследования с учетом данных ПГГ о доле заработной платы и прочих расходов при проведении лекарственной терапии при злокачественных новообразованиях (кроме лимфоидной и кроветворной тканей) в условиях ДС, а также показателей, применяющихся в расчете стоимости случая КСГ, были получены результаты, представленные на рисунке 1. Расчетная стоимость по тарифу КСГ ДС по группе принадлежности схемы в ДС составила от 17 735 руб. (ds19.039) до 556 458 руб. (ds19.049).
Полученные результаты по стоимости схем по тарифу КСГ ДС в зависимости от группы ее принадлежности были использованы для расчета доли от исходного финансирования, принятого за 100%, каждой схемы ПОЛТ с учетом данных реестров за 2021 г. (рис. 2).
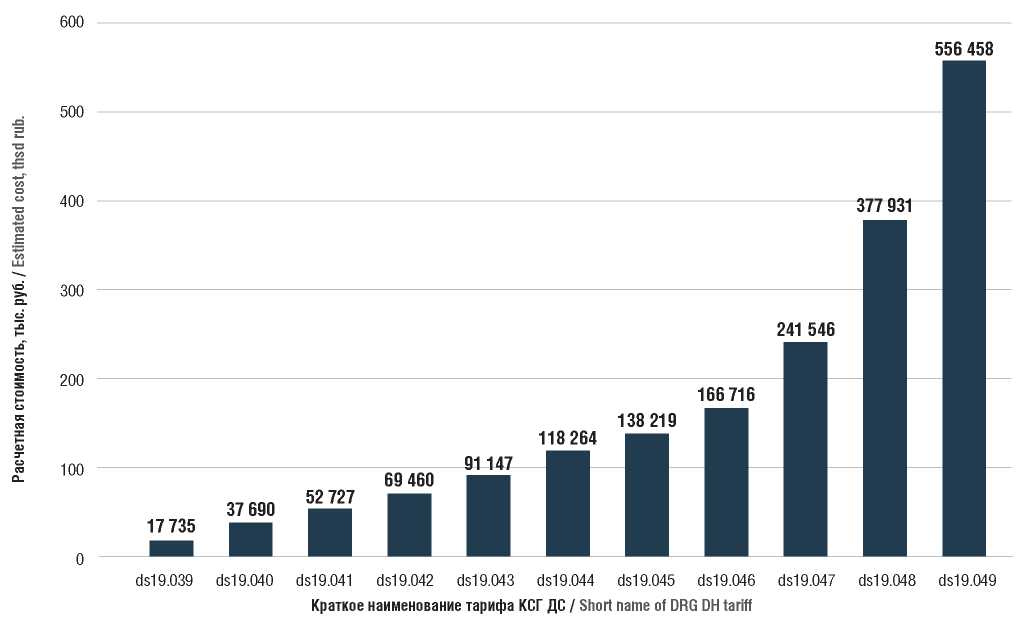
Рисунок 1. Расчетная стоимость схем противоопухолевой терапии по тарифу клинико-статистической группы (КСГ) в дневном стационаре (ДС)
Figure 1. The cost of the analyzed schemes for the treatment of malignant neoplasms in accordance with the diagnosis-related group (DRG) in day hospital (DH)
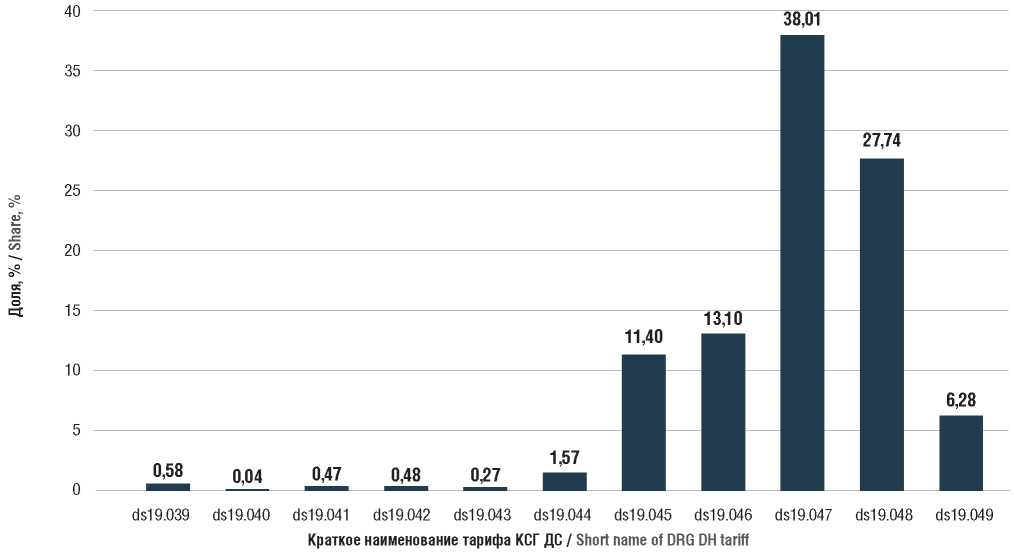
Рисунок 2. Доля финансирования схем противоопухолевой терапии, включенных в анализ, в разрезе клинико-статистических групп (КСГ) дневного стационара (ДС)
Figure 2. Share of financing of the analyzed schemes for the treatment of malignant neoplasms in accordance with the diagnosis-related groups (DRG) in day hospital (DH)
Максимальная доля финансирования составила 38,01% для КСГ ds19.047. Наибольшую долю для данной группы определило вхождение в ее состав схемы ПОЛТ sh0246 (ds19.047, энзалутамид 160 мг ежедневно), на которую в разрезе анализируемых схем ПОЛТ приходится 13,15%. При анализе схем, входящих в группы с максимальным финансированием, данные для двух других схем с максимальной долей распределяются следующим образом: 8,02% и 5,55% для схем лекарственной терапии sh0049 (ds19.048, дабрафениб 300 мг ежедневно + траметиниб 2 мг ежедневно) и sh0155 (ds19.046, палбоциклиб 125 мг в 1–21-й дни + фулвестрант 500 мг 1 раз в 28 дней (500 мг 2 раза в 1-й месяц терапии), цикл 28 дней) соответственно.
Оценка изменения размеров финансирования противоопухолевой терапии в дневном стационаре на основе данных о частоте их применения и параметров ПГГ 2021 года / Assessment of changes in the amount of funding for antitumor therapy in a day hospital based on data on the frequency of their use and the parameters of the 2021 State Guarantees Program
При расчете объема финансирования в соответствии с методикой было установлено, что общий объем средств, высвобождаемых от сокращения нерациональных госпитализаций в условиях ДС, составляет 720,15 млн руб., или 2,08% от уровня финансирования анализируемых схем. Учитывая данные о госпитализациях в ДС за 2021 г., количество нерациональных госпитализаций при переводе выбранных схем в амбулаторный этап снизится на 16,1%. Однако при переводе только таблетированных схем экономия средств ОМС остается низкой: объем расходов на ДС снизится на 14,12%. При уменьшении нормативов объема и финансовых затрат в ДС расходы в амбулаторных условиях, соответственно, вырастут (на 4,15% от номинального значения). С учетом роста расходов на обращения/посещения в амбулаторном звене экономия на снижении госпитализации в ДС составит 0,02% от общего объема расходов ПГГ (рис. 3).
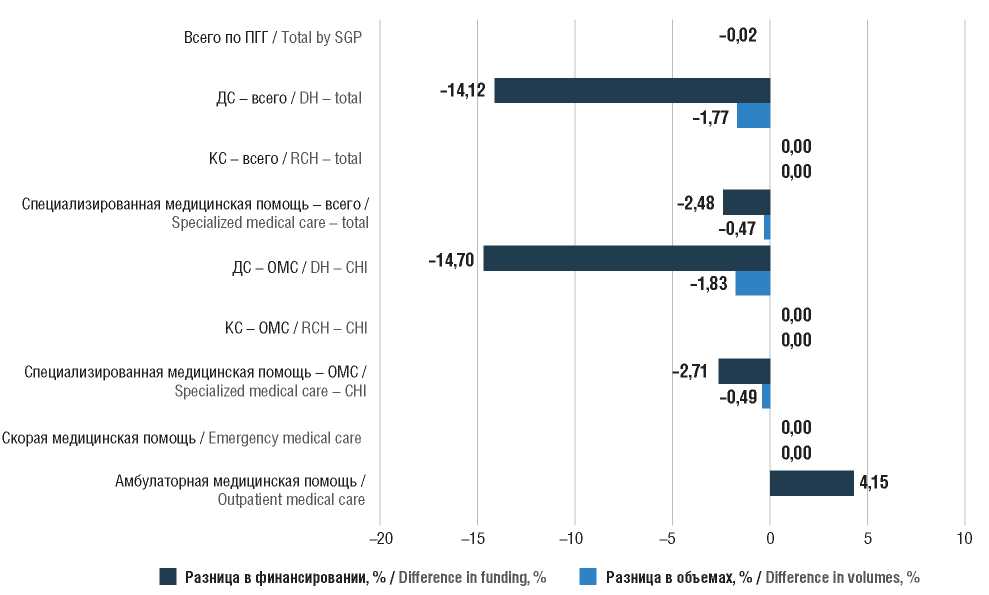
Рисунок 3. Результаты расчетов параметров ПГГ в целом с учетом предложений по переводу лекарственного обеспечения из дневного стационара в амбулаторное звено (относительные значения).
ПГГ – Программа государственных гарантий бесплатного оказания гражданам медицинской помощи; ДС – дневной стационар; КС – круглосуточный стационар; ОМС – обязательное медицинское страхование
Figure 3. The results of SGP parameter calculations generally taking into account proposals for the transfer of drug provision from a day hospital to an outpatient unit (relative values). SGP – State Guarantees Program for Provision of Free Medical Care to Citizens; DH – day hospital; RCH – round-the-clock hospital; CHI – Compulsory Health Insurance
Перевод всей лекарственной терапии на финансирование из средств ОМС потребует значительных дополнительных бюджетных расходов в размере 62,5 млрд руб., или 2,65% от общих расходов ПГГ (рис. 4). Также вырастут объемы медицинской помощи и расходы, связанные с амбулаторным посещением профильных специалистов.
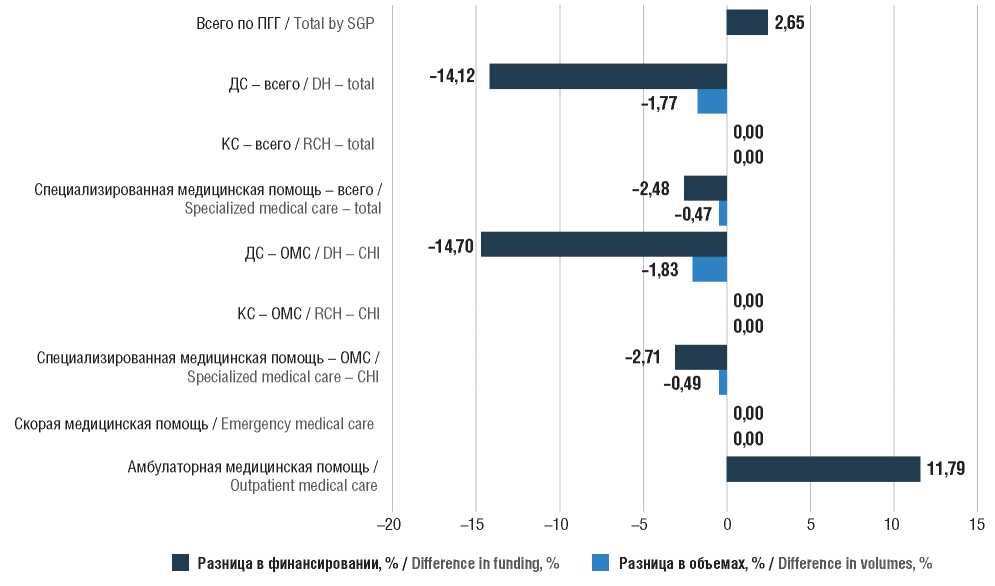
Рисунок 4. Результаты расчетов параметров ПГГ в целом с учетом предложений по полному переводу лекарственного обеспечения в систему ОМС и скрытого дефицита (относительные значения). ПГГ – Программа государственных гарантий бесплатного оказания гражданам медицинской помощи; ДС – дневной стационар; КС – круглосуточный стационар; ОМС – обязательное медицинское страхование
Figure 4. The results of SGP parameter calculations generally taking into account proposals for the transfer of drug provision to the CHI system and the hidden deficit (relative values). SGP – State Guarantees Program for Provision of Free Medical Care to Citizens; DH – day hospital; RCH – round-the-clock hospital; CHI – Compulsory Health Insurance
ОБСУЖДЕНИЕ / DISCUSSION
Механизм организации лекарственной помощи включает финансовые, организационные и управленческие аспекты. Таким образом, рационализация ЛО путем устранения несвойственных функций ДС для пациентов со злокачественными новообразованиями – одна из граней взаимосвязанной и сложно функционирующей системы. Проведенное нами исследование демонстрирует, что в области совершенствования ЛО сохраняется амбивалентность: с одной стороны, очевидна необходимость рационализации ЛО онкологических пациентов, с другой – без вложения дополнительных усилий и затрат возникают трудности в ее осуществлении. В одной из работ нашего коллектива рассмотрены ключевые проблемы ЛО онкологических пациентов на каждом из этапов оказания лекарственной помощи [14]. Решение одной из них путем устранения несвойственных функций ДС и обеспечения доступного и своевременного ЛО пациентам обусловливает ряд закономерных изменений:
- рациональное изменение распределения финансовых средств внутри ПГГ;
- устранение несвойственной функции ДС (выдачи лекарств);
- сокращение и перераспределение коечного фонда в ДС;
- рост доступности медицинской помощи;
- обеспечение преемственности оказания медицинской помощи пациентам.
Помимо очевидных плюсов перевода части схем ПОЛТ на проведение в амбулаторных условиях существуют и определенные ограничения, затрагивающие разные области функционирования лекарственной помощи. В частности, ограничением внедрения предлагаемых подходов может являться дефицит медицинского персонала и коек, на ликвидацию которого потребуется время, а также дополнительная потребность в финансовом обеспечении ПГГ. Приведенные в работе подходы по погружению финансирования лекарственной помощи в систему ОМС и их оценка показывают, что в рамках действующей ПГГ целесообразно делать это постепенно, ориентируясь на существующие возможности бюджета Фонда ОМС. Так, перевод ПОЛТ из ДС в амбулаторные условия без учета нереализованного спроса может привести к экономии бюджетных средств из-за сокращения издержек на содержание коек в ДС. Но при этом данный подход поднимает организационные вопросы по перепрофилированию коечного фонда в медицинских организациях и пересмотру нормативов объемов и финансирования медицинской помощи в ПГГ. Отдельно следует отметить, что погружение амбулаторной лекарственной помощи в ОМС повысит доступность медицинской помощи в регионах и может привести к росту спроса на данный вид помощи, что, в свою очередь, потребует повышения расходов системы ОМС.
Кроме формирования механизма рационального финансирования ЛО существует необходимость актуализации нормативно-правового регулирования данной области, исследования и анализа предложенных аспектов с позиции доказательной медицины. Так, число пациентов во всем мире, выбирающих амбулаторную монотерапию пероральными противоопухолевыми ЛП и комбинированную терапию пероральными и инъекционными ЛП, постоянно увеличивается, т.к. люди в первую очередь заинтересованы в повышении качества жизни. Таким образом, по результатам ряда исследований, при равной эффективности и токсичности пациенты предпочитают пероральную терапию внутривенной при возможности такой замены [15–17]. Однако перевод схем ПОЛТ из условий ДС в амбулаторное звено оставляет открытым вопрос, на какой период времени пациент должен получать необходимый ЛП или комбинацию ЛП.
Результаты самостоятельного приема лекарств, выявления и контроля возможных побочных нежелательных реакций при проведении пероральной терапии изучены в ряде исследований. Показано, что самостоятельный контроль за приемом лекарств при незлокачественных хронических заболеваниях, например гипертонической болезни, приводит к лучшему контролю заболевания и лучшему качеству жизни [18, 19]. Самоконтроль для пациентов, получающих пероральную химиотерапию, не менее важен, поскольку влияет на приверженность к лечению, качество жизни и безопасность [20–22]. В настоящее время разрабатываются и внедряются в клиническую практику шкалы и опросники для измерения способности к самоконтролю пациентов, получающих пероральную химиотерапию [23]. Кроме того, телемедицинские технологии позволяют осуществлять контроль за соблюдением терапии и безопасностью пациента [24, 25]. Тем не менее вопрос определения периода времени, который является научно обоснованным и целесообразным для каждой схемы терапии, открыт для дальнейшего изучения.
Следует отметить, что согласно общемировой практике ограниченный доступ к пероральной ПОЛТ является препятствием для эффективного лечения населения во всем мире [1, 26–28]. В странах Европы и Америки функционируют различные подходы к ЛО ПОЛТ, но при этом везде действует система оценки различных схем терапии и ограничения доступа их к государственному финансированию. Одним из ключевых факторов при доступе препаратов на государственный рынок является уровень финансирования онкологической помощи в рамках государственных расходов на здравоохранение. Плательщик зачастую ограничивает доступ к тем или иным ЛП в рамках различных условий оказанияпомощи (амбулаторно или стационарно), вводит механизм соплатежей или формирует закрытые списки препаратов, финансирование которых эффективно с точки зрения государственных расходов. Ограничивают всеобщий доступ к ЛО онкологических пациентов также децентрализация ЛО, длительное ожидание одобрения препарата для конкретной нозологии или его включения в списки для возмещения через страхование, дефицит ЛП и ряд других аспектов.
Одним из факторов, который еще раз подчеркнул необходимость решений в области ЛО, стали ограничения, возникшие в период пандемии COVID-19. Они вывели данную проблему на еще более актуальный уровень в связи с необходимостью ограничить контакты и риски для пациентов, получающих противоопухолевое лечение.
ЗАКЛЮЧЕНИЕ / CONCLUSION
В исследовании определено направление совершенствования системы ЛО онкологических пациентов в РФ – устранение несвойственных функций ДС с последующим погружением соответствующих препаратов в систему ОМС. Отсутствие стабильного финансирования в амбулаторном сегменте не позволяет полностью обеспечить доступность ПОЛТ, что, в свою очередь, препятствует достижению целей по борьбе со злокачественными новообразованиями. Результаты исследования, а также разработанная модель могут использоваться для дальнейшего анализа влияния изменений в подходах к ЛО онкологических пациентов на реализацию ПГГ отдельно по каждому субъекту РФ или в целом по всей стране. Проведенная работа показывает, что, несмотря на прогресс, достигнутый в области ЛО, для выстраивания оптимальной модели необходимо учитывать преемственность ЛО.
Наши результаты подчеркивают важность проведения работ и дальнейших исследований по рационализации ЛО по профилю «онкология» и формирования преемственности оказания медицинской помощи пациентам со злокачественными новообразованиями. Данная тема часто затрагивается в профессиональном сообществе, однако консенсус до сих пор не достигнут, что определяет необходимость сотрудничества с целью достижения лучшей клинической практики для пациента.
1. Паспорт федерального проекта «Борьба с онкологическими заболеваниями» (приложение к протоколу заседания проектного комитета по национальному проекту «Здравоохранение» от 14.12.2018 № 3).
2. Постановление Правительства РФ от 28.12.2020 № 2299 (ред. от 19.11.2021) «О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2021 год и на плановый период 2022 и 2023 годов».
3. Письмо Минздрава России № 11-7/И/2-20691, ФФОМС № 00-10-26-2-04/11-51 от 30.12.2020 «О методических рекомендациях по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования».
4. https://grls.rosminzdrav.ru.
5. Письмо Минздрава России № 11-7/И/2-20691, ФФОМС № 00-10-26-2-04/11-51 от 30.12.2020 «О методических рекомендациях по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования»; Постановление Правительства РФ от 28.12.2020 № 2299 «О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2021 год и на плановый период 2022 и 2023 годов».
6. Показатели реализации субъектами Российской Федерации переданных полномочий Российской Федерации по лекарственному обеспечению отдельных категорий граждан, реализации Постановления Правительства Российской Федерации от 26.11.2018 № 1416 (ВЗН) и Распоряжения Правительства Российской Федерации от 31.12.2018 № 3053-р по состоянию на 28.12.2020.
Список литературы
1. Cortes J., Perez-García J.M., Llombart-Cussac A., et al. Enhancing global access to cancer medicines. CA Cancer J Clin. 2020; 70 (2): 105–24. https://doi.org/10.3322/caac.21597.
2. Sung H., Ferlay J., Siegel R.L., et al. Global Cancer Statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021; 71 (3): 209–49. https://doi.org/10.3322/caac.21660.
3. Здравоохранение в России. 2021. Статистический сборник. М.; 2021: 171 с. URL: https://rosstat.gov.ru/storage/mediabank/Zdravoohran-2021.pdf (дата обращения 16.02.2022).
4. Mariotto A.B., Noone A.M., Howlader N., et al. Cancer survival: an overview of measures, uses, and interpretation. J Natl Cancer Inst Monogr. 2014; 2014 (49): 145–86. https://doi.org/10.1093/jncimonographs/lgu024.
5. Shulman L.N., Palis B.E., McCabe R., et al. Survival as a quality metric of cancer care: use of the National Cancer Data Base to assess hospital performance. J Oncol Pract. 2018; 14 (1): e59–72. https://doi.org/10.1200/JOP.2016.020446.
6. Allemani C., Matsuda T., Di Carlo V., et al. Global surveillance of trends in cancer survival 2000-14 (CONCORD-3): analysis of individual records for 37 513 025 patients diagnosed with one of 18 cancers from 322 population-based registries in 71 countries. Lancet. 2018; 391 (10125): 1023–75. https://doi.org/10.1016/S0140-6736(17)33326-3.
7. American Cancer Society. Cancer Treatment & Survivorship. Facts & Figures 2019–2021. URL: https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/cancer-treatment-and-survivorship-facts-and-figures/cancer-treatment-and-survivorship-facts-and-figures-2019-2021.pdf (дата обращения 16.02.22).
8. Mariotto A.B., Yabroff K.R., Shao Y., et al. Projections of the cost of cancer care in the United States: 2010–2020. J Natl Cancer Inst. 2011; 103 (2): 117–28. https://doi.org/10.1093/jnci/djq495.
9. American Cancer Society Cancer Action Network. The Costs of cancer. 2020 edition. URL: https://www.fightcancer.org/sites/default/files/National%20Documents/Costs-of-Cancer-2020-10222020.pdf (дата обращения 16.02.22).
10. Hofmarcher T., Lindgren P., Wilking N., Jönsson B. The cost of cancer in Europe 2018. Eur J Cancer. 2020; 129: 41–9. https://doi.org/10.1016/j.ejca.2020.01.011.
11. Отчет о результатах деятельности Федерального фонда обязательного медицинского страхования в 2020 году. М.; 2021: 148 с. URL: https://www.ffoms.gov.ru/system-oms/about-fund/fund-activities/1_ОТЧЕТ_о_результатах_деятельности_ФОМС_за_2020_год.pdf (дата обращения 16.02.22).
12. Доклад об осуществлении государственного контроля (надзора) в сфере охраны здоровья граждан и об эффективности такого контроля (надзора) в 2020 году. М.; 2021: 146 с. URL: https://roszdravnadzor.gov.ru/spec/about/plans/documents/71757 (дата обращения 16.02.22).
13. Ogrinc G., Davies L., Goodman D., et al. SQUIRE 2.0 (Standards for QUality Improvement Reporting Excellence): revised publication guidelines from a detailed consensus process. Perm J. 2015; 19 (4): 65–70. https://doi.org/10.7812/TPP/15-141.
14. Агафонова Ю.А., Федяев Д.В., Омельяновский В.В., Снеговой А.В. Преемственность лекарственного обеспечения на амбулаторном и стационарном этапах терапии онкологических пациентов. Проблемы и пути решения. Медицинские технологии. Оценка и выбор. 2021; 3: 37–44. https://doi.org/10.17116/medtech20214303137.
15. Eek D., Krohe M., Mazar I., et al. Patient-reported preferences for oral versus intravenous administration for the treatment of cancer: a review of the literature. Patient Prefer Adherence. 2016; 10: 1609–21. https://doi.org/10.2147/PPA.S106629.
16. Twelves C., Gollins S., Grieve R., Samuel L. A randomised cross-over trial comparing patient preference for oral capecitabine and 5-fluorouracil/leucovorin regimens in patients with advanced colorectal cancer. Ann Oncol Off J Eur Soc Med Oncol. 2006; 17 (2): 239–45. https://doi.org/10.1093/annonc/mdj023.
17. Weingart S.N., Brown E., Bach P.B., et al. NCCN Task Force Report: Oral chemotherapy. J Natl Compr Canc Netw. 2008; 6 (Suppl. 3): S1–14.
18. Persell S.D., Karmali K.N., Lee J.Y., et al. Associations between health literacy and medication self-management among community health center patients with uncontrolled hypertension. Patient Prefer Adherence. 2020; 14: 87–95. https://doi.org/10.2147/PPA.S226619.
19. Hallberg I., Ranerup A., Kjellgren K. Supporting the self-management of hypertension: patients’ experiences of using a mobile phone-based system. J Hum Hypertens. 2016; 30 (2): 141–6. https://doi.org/10.1038/jhh.2015.37.
20. Tuominen L., Ritmala-Castrén M., Nikander P., et al. Empowering patient education on self-care activity among patients with colorectal cancer – a research protocol for a randomised trial. BMC Nurs. 2021; 20 (1): 94. https://doi.org/10.1186/s12912-021-00617-z.
21. Jacobs J.M., Ream M.E., Pensak N., et al. Patient experiences with oral chemotherapy: adherence, symptoms, and quality of life. J Natl Compr Canc Netw. 2019; 17 (3): 221–8. https://doi.org/10.6004/jnccn.2018.7098.
22. Tokdemir G., Kav S. The effect of structured education to patients receiving oral agents for cancer treatment on medication adherence and self-efficacy. Asia-Pacific J Oncol Nurs. 2017; 4 (4): 290–8. https://doi.org/10.4103/apjon.apjon_35_17.
23. Peng Q., Wu W. Development and validation of oral chemotherapy self-management scale. BMC Cancer. 2020; 20 (1): 890. https://doi.org/10.1186/s12885-020-07404-0.
24. Skrabal Ross X., Gunn K.M., Patterson P., Olver I. Development of a smartphone program to support adherence to oral chemotherapy in people with cancer. Patient Prefer Adherence. 2019; 13: 2207–15. https://doi.org/10.2147/PPA.S225175.
25. Kongshaug N., Skolbekken J.A., Faxvaag A., Hofsli E. Cancer patients’ perceived value of a smartphone app to enhance the safety of home-based chemotherapy: feasibility study. JMIR Form Res. 2021; 5 (1): e20636. https://doi.org/10.2196/20636.
26. Cardoso F., MacNeill F., Penault-Llorca F., et al. Why is appropriate healthcare inaccessible for many European breast cancer patients? – The EBCC 12 manifesto. Breast. 2021; 55: 128–35. https://doi.org/10.1016/j.breast.2020.12.010.
27. WHO report on cancer: setting priorities, investing wisely and providing care for all. World Health Organization; 2020. URL: https://apps.who.int/iris/handle/10665/330745 (дата обращения 16.02.22).
28. Communication from the commission to the European Parliament and the Council Europe’s Beating Cancer Plan. URL: https://eur-lex.europa.eu/legal-content/en/TXT/?uri=COM%3A2021%3A44%3AFIN (дата обращения 16.02.22).
Об авторах
Ю. А. АгафоноваРоссия
Агафонова Юлия Андреевна – специалист отдела способов оплаты медицинской помощи Управления экономики и финансирования здравоохранения; аспирант кафедры онкологии факультета дополнительного профессионального образования. РИНЦ SPIN-код: 6317-0280
Хохловский пер., д. 10/5, Москва 109028
ул. Делегатская, д. 20, стр. 1, Москва 127473
Д. В. Федяев
Россия
Федяев Денис Валерьевич – начальник Управления экономики и финансирования здравоохранения; научный сотрудник Центра финансов здравоохранения. WoS ResearcherID: W-3848-2019; Scopus Author ID: 57206481925; РИНЦ SPIN-код: 6864-5660
Хохловский пер., д. 10/5, Москва 109028
Настасьинский пер., д. 3/2, Москва 127006
А. В. Снеговой
Россия
Снеговой Антон Владимирович – д.м.н., профессор кафедры онкологии факультета дополнительного профессионального образования; заведующий отделом лекарственного противоопухолевого лечения. РИНЦ SPIN-код: 8398-2396
ул. Делегатская, д. 20, стр. 1, Москва 127473
ул. 3-я Парковая, д. 51, стр. 1, Москва 105425
В. В. Омельяновский
Россия
Омельяновский Виталий Владимирович – д.м.н., профессор, генеральный директор; руководитель Центра финансов здравоохранения; заведующий кафедрой экономики, управления и оценки технологий здравоохранения. WoS ResearcherID: P-6911-2018; Scopus Author ID: 6507287753; РИНЦ SPIN-код: 1776-4270
Хохловский пер., д. 10/5, Москва 109028
Настасьинский пер., д. 3/2, Москва 127006
ул. Баррикадная, д. 2/1, стр. 1, Москва 125993
Рецензия
Для цитирования:
Агафонова Ю.А., Федяев Д.В., Снеговой А.В., Омельяновский В.В. Совершенствование эффективности системы лекарственного обеспечения пациентов со злокачественными новообразованиями. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022;15(2):209-220. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.137
For citation:
Agafonova Yu.A., Fedyaev D.V., Snegovoy A.V., Omelyanovskiy V.V. Improving the efficiency of the medicine provision system for patients with malignant neoplasms. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2022;15(2):209-220. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.137

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.






































