Перейти к:
Эффективность таргетных лекарственных препаратов в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации: обновление систематического обзора
https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.128
Аннотация
Актуальность. Систематический обзор позволяет определить основные методы терапии заболевания, а синтез доказательств помогает сравнить клиническую эффективность разных опций терапии. С течением времени появляются новые лекарственные препараты (ЛП) и клинические исследования, поэтому ранее проведенные сетевые метаанализы требуют дополнения.
Цель: обновление существующего систематического обзора и сетевого метаанализа с учетом рандомизированных клинических исследований (РКИ) по зарегистрированному в Российской Федерации новому препарату класса ингибиторов интерлейкина 23 (ИЛ-23) – рисанкизумаба, а также новых опубликованных результатов РКИ, изучающих эффективность терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом другими таргетными ЛП; обновление значений числа пациентов, которых необходимо пролечить (англ. number needed to treat, NNT) для достижения ответа на терапию, и затрат на его достижение (англ. сost per responder, CpR) по показателям индекса площади поражения и тяжести псориаза (англ. Psoriasis Area and Severity Index, PASI) 75/90 за 12–16 нед и 1 год терапии.
Материал и методы. Мы провели обновление систематического поиска литературы в базах данных PubMed/MEDLINE и Embase. В синтез доказательств были включены РКИ, оценивающие эффективность адалимумаба (АДА), инфликсимаба (ИНФ), этанерцепта (ЭТЦ), цертолизумаба пэгола (ЦЗП), иксекизумаба (ИКСЕ), нетакимаба (НТК), секукинумаба (СЕК), рисанкизумаба (РИС), гуселькумаба (ГУС), устекинумаба (УСТ), тофацитиниба (ТОФА) и апремиласта (АПР) после 12 нед терапии. Выполнен байесовский метаанализ с построением моделей метарегрессий для учета высокой гетерогенности в характеристиках популяции между РКИ и существенных различий в эффекте плацебо. Рассматриваемые ЛП были ранжированы на основе значений площади поверхности под кумулятивной кривой распределения (англ. surface under the cumulative ranking curve, SUCRA). Дополнительно проведен анализ по классам ЛП.
Результаты. В сеть были добавлены 23 новых РКИ. Ингибитор ИЛ-23 РИС, недавно зарегистрированный в России, присоединился к группе наиболее эффективных ЛП, таких как ингибиторы ИЛ-17 НТК и ИКСЕ, а также ингибитор ИЛ-23 ГУС. По показателю PASI 75 РИС и ИКСЕ продемонстрировали статистически значимое превосходство по сравнению со всеми ингибиторами фактора некроза опухоли альфа (ФНОα) (ИНФ, АДА, ЭТЦ), малыми молекулами (ТОФA, АПР) и ингибитором ИЛ-12/23 УСТ, в то время как НТК и ГУС характеризовались сопоставимой эффективностью с ИНФ и превосходили оставшиеся препараты. Все ингибиторы ФНОα имели сопоставимую эффективность. В случаях ГУС, ИКСЕ, ИНФ, НТК, РИС и СЕК для достижения одного ответа по критерию PASI 75 необходимо пролечить не более 2 пациентов, по критерию PASI 90 – не более 3 (по верхней границе 95% байесовского доверительного интервала). Как и в опубликованном ранее исследовании, НТК характеризовался наименьшими затратами на достижение одного ответа на терапию как за период 12 нед, так и за 1 год терапии.
Заключение. Добавление исследований с прямым сравнением ЛП и увеличение статистической мощности сетевого метаанализа позволили выявить ранее не идентифицированные значимые различия между опциями терапии среднетяжелого и тяжелого вульгарного псориаза.
Ключевые слова
Для цитирования:
Соколова В.Д., Саблева Н.А., Младов В.В., Толкачева Д.Г. Эффективность таргетных лекарственных препаратов в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации: обновление систематического обзора. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022;15(1):131-144. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.128
For citation:
Sokolova V.D., Sableva N.A., Mladov V.V., Tolkacheva D.G. Efficacy of targeted drugs for the treatment of adults with moderate-to-severe plaque psoriasis in the Russian Federation: a systematic literature review update. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2022;15(1):131-144. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.128
ВВЕДЕНИЕ / INTRODUCTION
Псориаз обыкновенный (ПсО, бляшечный или вульгарный) – хроническое заболевание кожи, характеризующееся появлением папулезных высыпаний. Выявлено несколько клинических фенотипов псориаза, среди которых обыкновенный псориаз составляет 90% случаев, что делает его на данный момент самым распространенным иммуноопосредованным заболеванием в мире: от 0,51% до 11,43% среди взрослого населения и от 0% до 1,37% у детей [1]. По российским данным за 2018 г., распространенность псориаза составила 242,4 случая на 100 тыс. населения, заболеваемость – 66,5 случаев на 100 тыс. [2].
Коморбидные нозологии для ПсО, такие как депрессия, сердечно-сосудистые заболевания и псориатический артрит (ПсА), усугубляют состояние пациента, что приводит к ухудшению качества жизни и инвалидизации [3]. Существенный вклад в патогенез заболевания вносят фактор некроза опухоли альфа (ФНОα), дендритные клетки и Т-клетки. Воздействие на данные патогенетические механизмы ПсО является базой для новых методов терапии [4].
Лечение предполагает симптоматическую терапию, целью которой является снижение частоты обострений и проявлений заболевания [2]. На территории Российской Федерации (РФ) зарегистрированы генно-инженерные биологические препараты (ГИБП) следующих классов: ингибиторы ФНОα (иФНОα) – адалимумаб (АДА), инфликсимаб (ИНФ), этанерцепт (ЭТЦ) и цертолизумаба пэгол (ЦЗП); ингибиторы интерлейкина 17 (иИЛ-17) – иксекизумаб (ИКСЕ), нетакимаб (НТК) и секукинумаб (СЕК), иИЛ-23 – рисанкизумаб (РИС) и гуселькумаб (ГУС), иИЛ-12/23 – устекинумаб (УСТ). Помимо ГИБП на рынке также присутствуют малые молекулы: ингибитор янус-киназ (иЯК) тофацитиниб (ТОФА) и селективный ингибитор фосфодиэстеразы 4-го типа (иФДЭ4) апремиласт (АПР).
В 2019 г. был опубликован первый систематический обзор и сетевой метаанализ эффективности и безопасности применения таргетных лекарственных препаратов (ЛП) в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным ПсО в РФ [5], по результатам которого классы иИЛ-17 и иИЛ-23 показали наиболее высокую эффективность по сравнению с другими таргетными препаратами. Большинство анализируемых ЛП характеризовались благоприятным профилем безопасности. В 2020 г. появилось дополнение к метаанализу с анализом числа взрослых пациентов со среднетяжелым и тяжелым вульгарным ПсО, которых необходимо пролечить для достижения одного ответа на терапию (англ. number needed to treat, NNT), по показателям индекса площади поражения и тяжести псориаза (англ. Psoriasis Area and Severity Index, PASI) 75/90 (75% и 90% снижение тяжести заболевания по сравнению с исходным уровнем) и соответствующих ему затрат на достижение ответа на терапию (англ. сost per responder, CpR) после 12 нед и 1 года терапии для каждого исследуемого ЛП [6].
Цель — обновление существующего систематического обзора и сетевого метаанализа с учетом рандомизированных клинических исследований (РКИ) по зарегистрированному в РФ новому препарату класса иИЛ-23 – рисанкизумабу, а также новых опубликованных результатов РКИ, изучающих эффективность терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом другими таргетными ЛП; обновление значений NNT и CpR по PASI 75/90 за 12–16 нед и 1 год терапии.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
Систематический поиск литературы / Systematic literature search
Обновление систематического поиска осуществляли два исследователя (В.Д. Соколова и Н.А. Саблева) с учетом прежнего протокола и методологии, описанных ранее [5]. Доступ к базе данных (БД) Embase был ограничен на момент первоначального обзора, и поиск в этой БД выполнялся через Кокрейновскую библиотеку (англ. Cochrane Library), поэтому было принято решение провести полноценный поиск в Embase. Стратегия поиска представлена в Приложении 1. Временной диапазон поиска в Embase не ограничивали. Также проведено обновление поиска в PubMed/ MEDLINE с использованием ранее заявленной стратегии и ограничением временного диапазона (начиная с даты прошлого поиска). Кроме того, проверяли списки литературы оригинальных обзоров и статей на предмет дополнительных релевантных исследований.
Обновление выполняли по всем первоначальным критериям эффективности: частота достижения PASI 75, PASI 90, PASI 100, общая оценка состояния пациента врачом или исследователем (англ. Physician’s/Investigator’s Global Assessment, PGA/IGA 0/1), дерматологический индекс качества жизни (англ. Dermatology Life Quality Index, DLQI). Исходы эффективности оценивали после 12 нед терапии (после 10 нед у ИНФ, после 16 нед у ЦЗП, ГУС и РИС). В качестве основного исхода эффективности рассматривали долю пациентов, достигших PASI 75 после 12 нед терапии.
В связи с отсутствием статистически значимых различий между большинством препаратов и плацебо (ПЛА) по профилю безопасности [5] и коротким плацебо-контролируемым периодом в РКИ мы приняли решение не проводить обновление систематического обзора по критериям безопасности.
Сбор и оценка качества данных / Data collection and quality evaluation
Сбор данных из дополнительно отобранных РКИ осуществлялся на основе исходной таблицы MS Excel (Microsoft, США) одним экспертом (В.Д. Соколова) и валидировался вторым независимым исследователем (В.В. Младов). Данные, представленные только в графическом виде, извлекались с помощью специального программного обеспечения (WebPlotDigitizer).
Два независимых эксперта (В.Д. Соколова и Н.А. Саблева) определяли методологическое качество дополнительно отобранных РКИ на основе инструмента оценки риска систематической ошибки (англ. Risk of Bias, RoB2), рекомендованного Кокрейновским сообществом [7].
Для нового набора РКИ была также проведена оценка клинической, методологической и статистической гетерогенности по методологии, описанной ранее [5]. Риск публикационного смещения для нового набора РКИ по каждому анализируемому исходу оценивали на основе модифицированной воронкообразной диаграммы (англ. funnel plot).
Сетевой метаанализ / Network meta-analysis
Один исследователь (В.В. Младов) проводил моделирование сетевого метаанализа c использованием методологии, описанной в исходной статье [5]. Два независимых эксперта (Д.Г. Толкачева, В.Д. Соколова) выполняли последующую валидацию полученных результатов.
Несмотря на добавление 23 новых РКИ, вариабельность ответа в группе плацебо сохранилась (см. Приложение 2), в связи с чем были проведены сетевые метаанализы с поправкой на ответ в группе плацебо.
Результаты непрямых сравнений таргетных препаратов на основе сетевого метаанализа представлены как отношения рисков (ОР) с 95% байесовскими доверительными интервалами (БДИ). Дополнительно для каждого ЛП рассчитаны значения площади под кумулятивной кривой распределения (англ. Surface Under the Cumulative RAnking curve, SUCRA)1, что позволяет учесть местоположение и дисперсию всех относительных эффектов [8].
Также мы проводили анализ по классам ЛП (иИЛ-17, иИЛ-12/23, иИЛ-23, иФНОα, иЯК и иФДЭ4) с применением аналогичной методологии моделирования.
Обновление значений NNT и CpR / Updating NNT and CpR values
Мы обновили данные предыдущего анализа [6] с учетом выхода новых препаратов – РИС и биоаналога ЭТЦ, а также изменения цен на ИКСЕ и биоаналог ИНФ.
РЕЗУЛЬТАТЫ / RESULTS
Результаты систематического поиска / Results of a systematic search
Результаты поиска и процесс отбора публикаций отражены на рисунке 1. Поиск в PubMed/MEDLINE с обновленной стратегией (добавление РИС) и фильтром на дату публикации идентифицировал 130 новых записей. Поиск в Embase определил 1102 записи, а 1 публикация была добавлена из списка литературы другого исследования. После удаления дубликатов 1160 записей перешли на стадию скрининга и 1041 из них была исключена по ряду причин (см. рис. 1). В итоге 117 полнотекстовых публикаций были оценены на приемлемость. В финальный анализ были включены 22 новые публикации, описывающие результаты 23 РКИ.
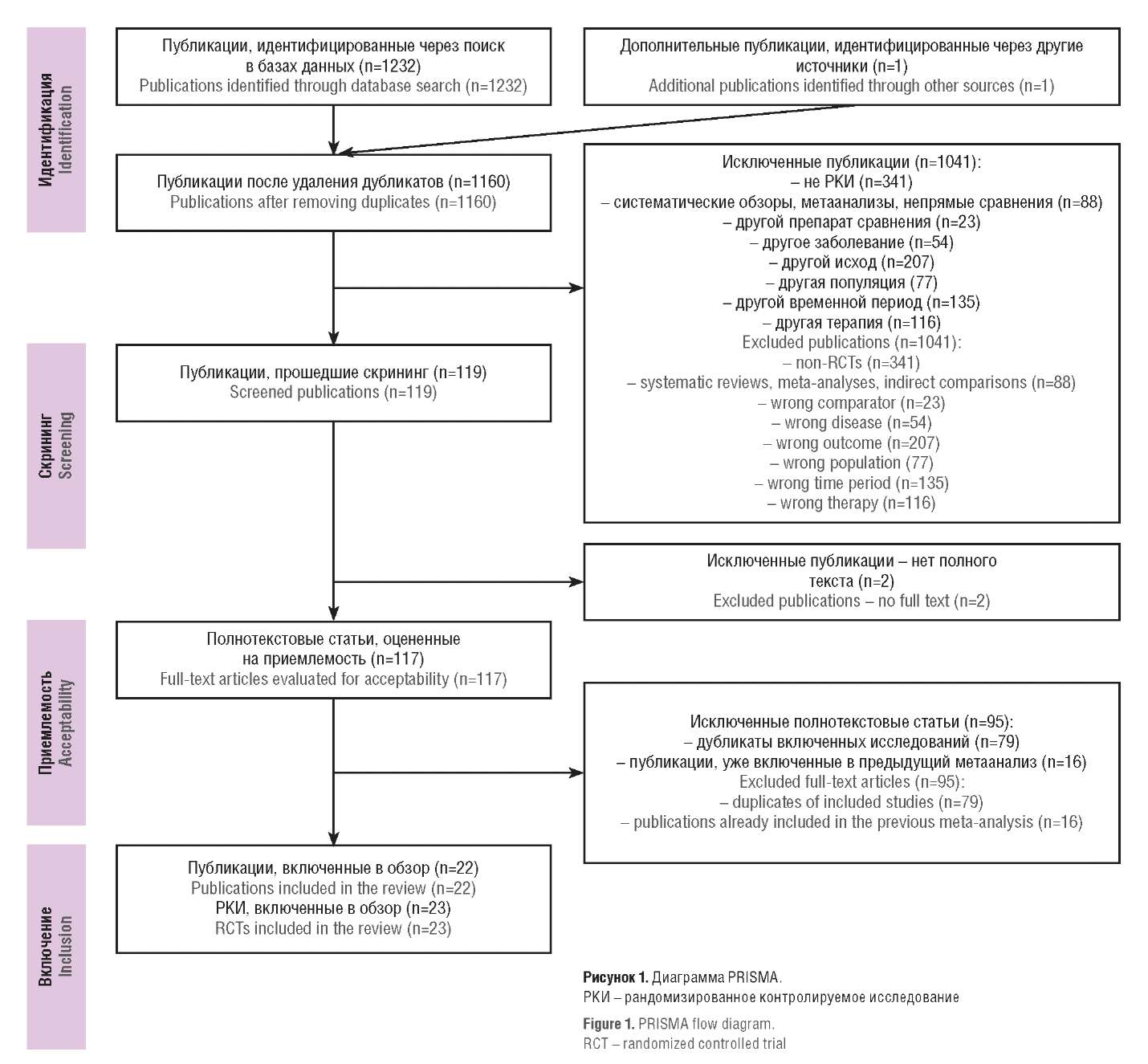
Рисунок 1. Диаграмма PRISMA. РКИ – рандомизированное контролируемое исследование
Figure 1. PRISMA flow diagram. RCT – randomized controlled trial
Характеристика отобранных исследований и целевой популяции / Characteristics of selected studies and target population
Общая сетевая диаграмма РКИ, включенных в систематический обзор и последующий синтез, представлена на рисунке 2.
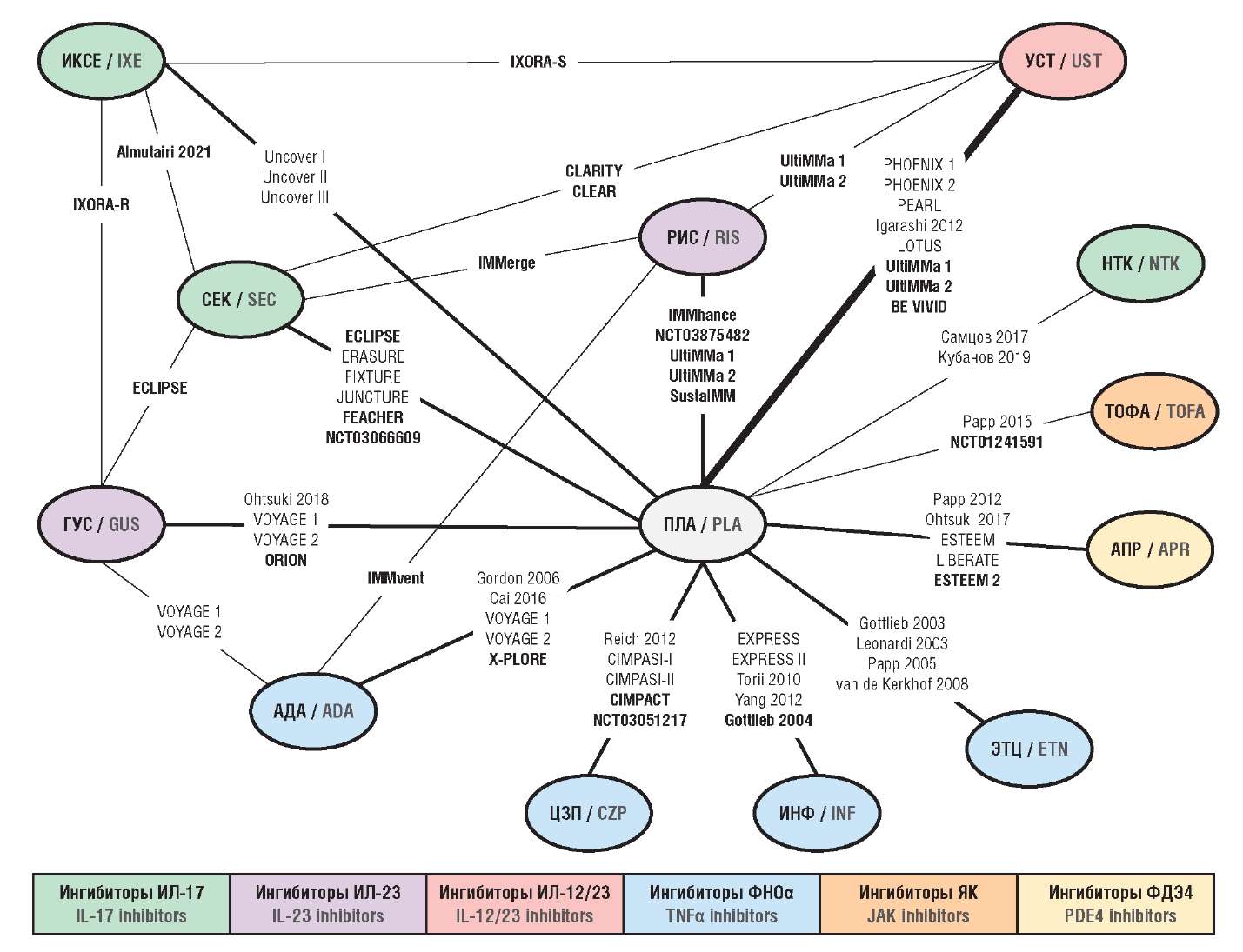
Рисунок 2. Общая сетевая диаграмма. Названия добавленных в сеть
рандомизированных контролируемых исследований отмечены жирным шрифтом.
ИКСЕ – иксекизумаб; УСТ – устекинумаб; СЕК – секукинумаб; РИС – рисанкизумаб; НТК – нетакимаб; ТОФА – тофацитиниб; ГУС – гуселькумаб; АПР – апремиласт; АДА – адалимумаб; ЦЗП – цертолизумаба пэгол; ИНФ – инфликсимаб; ЭТЦ – этанерцепт; ПЛА – плацебо; ИЛ – интерлейкин; ЯК – янус-киназа; ФДЭ4 – фосфодиэстераза 4-го типа; ФНОα – фактор некроза опухоли альфа
Figure 2. General network diagram. Added randomized control trials are highlighted in bold type.
IXE – ixekizumab; UST – ustekinumab; SEC – secukinumab; RIS – risankizumab; NTK – netakimab; TOFA – tofacitinib; GUS – guselkumab; APR – apremilast; ADA – adalimumab; CZP – certolizumab pegol; INF – infliximab; ETN – etanercept; PLА – placebo; IL – interleukin; JK – janus kinase; PDE4 – phosphodiesterase, type 4; TNFα – tumor necrosis factor alpha
Все дополнительно включенные публикации были на английском языке (см. Приложение 3). Большинство включенных РКИ (17) – исследования III фазы, 2 исследования (см. Приложение 3: 11, 12) II фазы, 2 исследования [14][21] адаптивного дизайна II–III фазы, 2 исследования (см. Приложение 3: 1, 5) на IV (постмаркетинговой) фазе. Дизайн 15 РКИ включал плацебо-контроль, а в 6 из них присутствовал также активный компаратор, в то время как в 8 РКИ (см. Приложение 3: 1, 3, 5, 16–18, 20, 22) сравнивали эффективность двух активных ЛП между собой без группы плацебо. Также в 8 из 23 отобранных РКИ (см. Приложение 3: 2, 4, 8, 11–14, 21) был проведен анализ разных доз. В 22 РКИ участники были «заслеплены», и только 1 РКИ (см. Приложение 3: 22) было открытым. Все РКИ оценивали эффективность после 12–16 нед терапии. Общее количество участников в добавленных РКИ составило 9326 человек, среднее количество участников в одном исследовании – 405 человек. Длительность заболевания в среднем составила 17,6 года – от 12,7 (см. Приложение 3: 7) до 20,9 (см. Приложение 3: 21) года. Значения PASI на скрининге изменялись в промежутке от 16,9 (см. Приложение 3: 1) до 27,3 (см. Приложение 3: 8), у 19,2% пациентов в анамнезе присутствовал ПсА, причем данное значение колеблется в интервале от 8% (см. Приложение 3: 10) до 35% (см. Приложение 3: 18). Во всех РКИ исследовалась смешанная популяция в отношении опыта биологической терапии, однако в 1 исследовании (см. Приложение 3: 9) не указано, какая популяция была исследована. Доля бионаивной популяции составила от 40% (см. Приложение 3: 11) до 91% (см. Приложение 3: 2). Данные по исходным характеристикам участников и эффективности представлены в Приложениях 4 и 5 соответственно.
Была выявлена высокая статистическая гетерогенность по критерию PASI 75 у пары АПР+ПЛА (5), значительная статистическая гетерогенность по PASI 75 отмечена у пар НТК+ПЛА (2), ИКСЕ+ПЛА (3), по PASI 100 – у пары СЕК+УСТ (2). Оценка статистической гетерогенности представлена в Приложении 6.
Таким образом, наблюдалась незначительная методологическая гетерогенность, связанная с временным периодом оценки исходов эффективности, незначительная клиническая гетерогенность, связанная с длительностью заболевания, а также высокая статистическая гетерогенность по ряду пар препаратов. Несмотря на наличие статистической гетерогенности, результаты прямых и непрямых сравнений согласованны (см. Приложение 7).
Результаты RoB2 представлены в Приложении 8. В дополнительных 23 исследованиях проводился анализ всех рандомизированных пациентов (англ. Intention To Treat, ITT). Двадцати РКИ присвоен низкий уровень риска систематической ошибки, неопределенный риск систематической ошибки был отмечен у трех РКИ (см. Приложение 3: 1, 12, 13) в силу недостаточности представленных данных для комплексной оценки (протокол исследования, план статистического анализа). Высокую оценку риска не получило ни одно исследование.
Публикационное смещение было выявлено только для исхода DLQI (см. Приложение 9).
Результаты сетевого метаанализа / Results of network meta-analysis
Сравнение эффективности
Для всех исходов эффективности использованы результаты моделей случайных эффектов, скорректированных на ответ в группе плацебо, которые учитывали выявленную гетерогенность между РКИ. Результаты сравнения эффективности таргетных препаратов после 12 нед терапии представлены на рисунке 3.
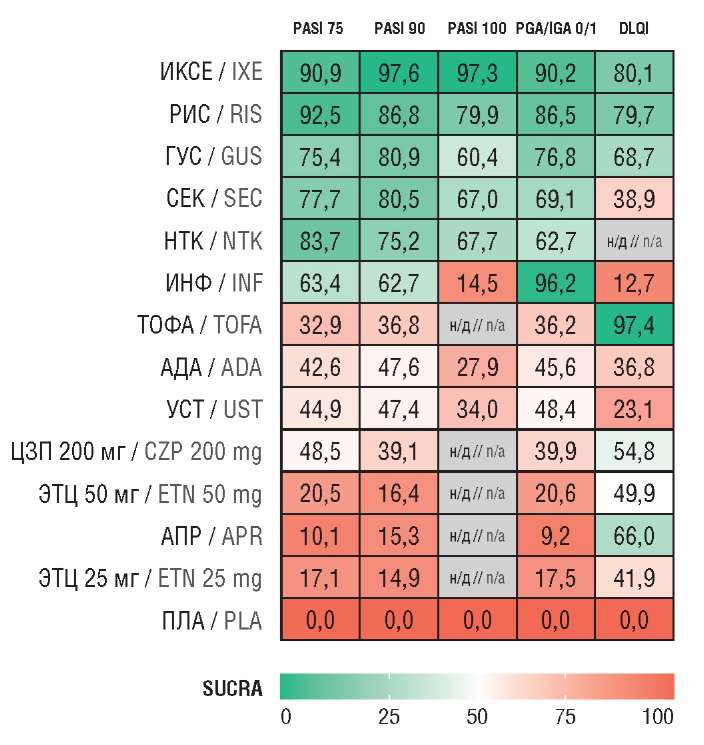
Рисунок 3. Значения площади под кумулятивной кривой распределения
(англ. Surface Under the Cumulative RAnking curve, SUCRA) для критериев эффективности.
ИКСЕ – иксекизумаб; РИС – рисанкизумаб; ГУС – гуселькумаб; СЕК – секукинумаб; НТК – нетакимаб; ИНФ – инфликсимаб; ТОФА – тофацитиниб; АДА – адалимумаб; УСТ – устекинумаб; ЦЗП – цертолизумаба пэгол; ЭТЦ – этанерцепт; АПР – апремиласт; PASI (англ. Psoriasis Area and Severity Index, PASI) 75/90/100 – индекс площади поражения и тяжести псориаза (75/90/100% снижение тяжести заболевания по сравнению с исходным уровнем); PGA/IGA 0/1 (англ. Physician’s/ Investigator’s Global Assessment) – общая оценка состояния пациента врачом/ исследователем; DLQI (англ. Dermatology Life Quality Index) – дерматологический индекс качества жизни; н/д – нет данных
Figure 3. Surface Under the Cumulative RAnking curve (SUCRA) values for efficacy outcomes.
IXE – ixekizumab; RIS – risankizumab; GUS – guselkumab; SEC – secukinumab; NTK – netakimab; INF – infliximab; TOFA – tofacitinib; ADA – adalimumab; UST – ustekinumab; CZP – certolizumab pegol; ETN – etanercept; APR – apremilast; PASI – Psoriasis Area and Severity Index; 75/90/100 – index of the lesion area and severity of psoriasis (75/90/100% reduction in the severity of the disease compared to the baseline level); PGA/IGA 0/1 – Physician’s/Investigator’s Global Assessment; DLQI – Dermatology Life Quality Index; n/a – no data available
Все препараты продемонстрировали статистически значимое превосходство над плацебо, а также большинство ЛП (кроме ЭТЦ) показало превосходство над АПР, как и в первоначальном сетевом метаанализе (рис. 3, 4). Попарное непрямое сравнение таргетных ЛП выявило, что иИЛ-23 РИС присоединился к группе наиболее эффективных препаратов, таких как иИЛ-17 НТК и ИКСЕ, а также иИЛ-23 ГУС. Данные препараты характеризовались сопоставимой эффективностью по достижению PASI 75 после 12–16 нед терапии. Также РИС и ИКСЕ показали статистически значимое превосходство по сравнению со всеми иФНОα (ИНФ, АДА, ЭТЦ), малыми молекулами (ТОФ, АПР) и иИЛ-12/23 УСТ, в то время как НТК и ГУС характеризовались сопоставимой эффективностью с ИНФ и превосходили оставшиеся препараты. Добавление новых исследований по СЕК увеличило мощность анализа и позволило данному ЛП продемонстрировать сопоставимую эффективность по показателю PASI 75 после 12 нед терапии с НТК, РИС, ИКСЕ и ГУС, а также превосходство над всеми иФНОα, кроме ИНФ и иИЛ-12/23 УСТ. В новом анализе ИНФ обладал сопоставимой эффективностью не только с ЦЗП, как в прошлом сетевом метаанализе, но и с АДА и УСТ. Попарные непрямые сравнения таргетных препаратов по другим исходам представлены в Приложении 10. Совокупные частоты достижения ответа отражены в Приложении 11.
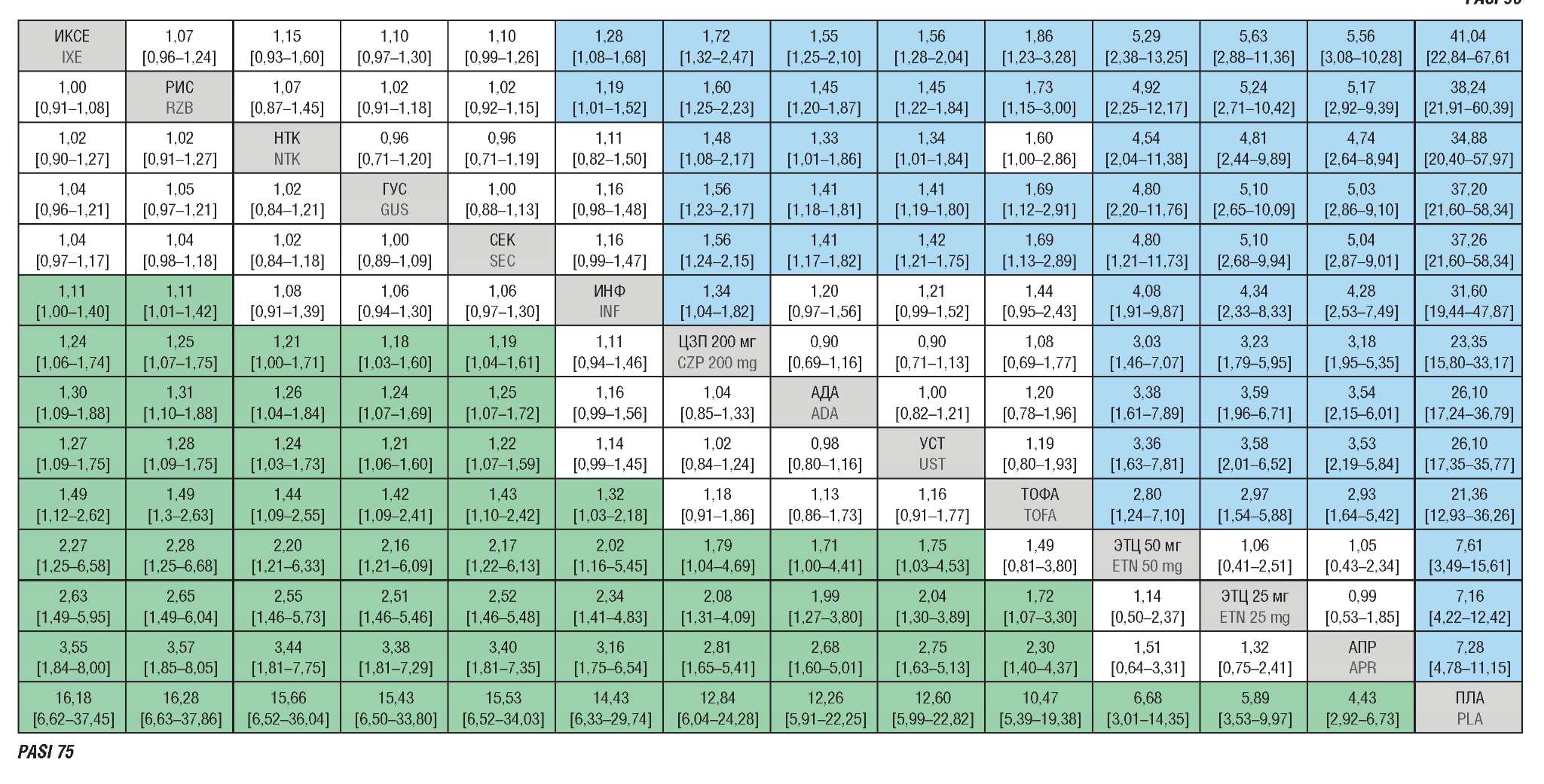
Рисунок 4. Совокупные размеры относительных эффектов (относительный риск (ОР)
и 95% байесовский доверительный интервал) для показателей PASI 75 и PASI 90.
Статистически значимые различия выделены цветом. Для PASI 75 значение в ячейке равно ОР препарата по столбцу к препарату по строке, для PASI 90 – ОР препарата по строке к препарату по столбцу. ОР в обратном направлении – 1/ОР в ячейке.
PASI (англ. Psoriasis Area and Severity Index, PASI) 75/90 – индекс площади поражения и тяжести псориаза (75/90% снижение тяжести заболевания по сравнению с исходным уровнем); ИКСЕ – иксекизумаб; РИС – рисанкизумаб; НТК – нетакимаб; ГУС – гуселькумаб; СЕК – секукинумаб; ИНФ – инфликсимаб; ЦЗП – цертолизумаба пэгол; АДА – адалимумаб; УСТ – устекинумаб; ТОФА – тофацитиниб; ЭТЦ – этанерцепт; АПР – апремиласт; ПЛА – плацебо
Figure 4. Network meta-analysis estimates (pooled values of risk ratio (RR)
and credible interval) of efficacy based on PASI 75 and PASI 90.
Statistically significant results are colored. For PASI 75, the value in the cell is equal to the RR of the drug in the column to the drug in the row; for PASI 90 – RR of the drug in the row to the drug in the column. In order to obtain RRs for comparisons in the opposite directions, inverse RR values (1/RR) should be taken.
PASI – Psoriasis Area and Severity Index; 75/90 – index of the lesion area and severity of psoriasis (75/90% reduction in the severity of the disease compared to the baseline level); IXE – ixekizumab; RIS – risankizumab; NTK – netakimab; GUS – guselkumab; SEC – secukinumab; INF – infliximab; CZP – certolizumab pegol; ADA – adalimumab; UST – ustekinumab; TOFA – tofacitinib; ETN – etanercept; APR – apremilast; PLA – placebo
Анализ по классам
По результатам анализа по классам препаратов иИЛ-23 и иИЛ17 занимали высшие ранги по всем исходам и продемонстрировали превосходство в эффективности над иИЛ-12/23, иФНОα и малыми молекулами. При этом иИЛ-12/23 и иФНОα характеризовались сопоставимой эффективностью. Подробные результаты анализа представлены в Приложении 12.
Обновление значений NNT и CpR
По результатам оценки 95% БДИ для значений NNT снова подтвердился вывод о статистически значимом превосходстве всех ЛП над плацебо. ГУС, ИКСЕ, ИНФ, НТК, РИС и СЕК демонстрируют по верхней границе 95% БДИ, что для достижения одного ответа по критерию PASI 75 необходимо пролечить не более 2 пациентов, по критерию PASI 90 – не более 3 (рис. 5).
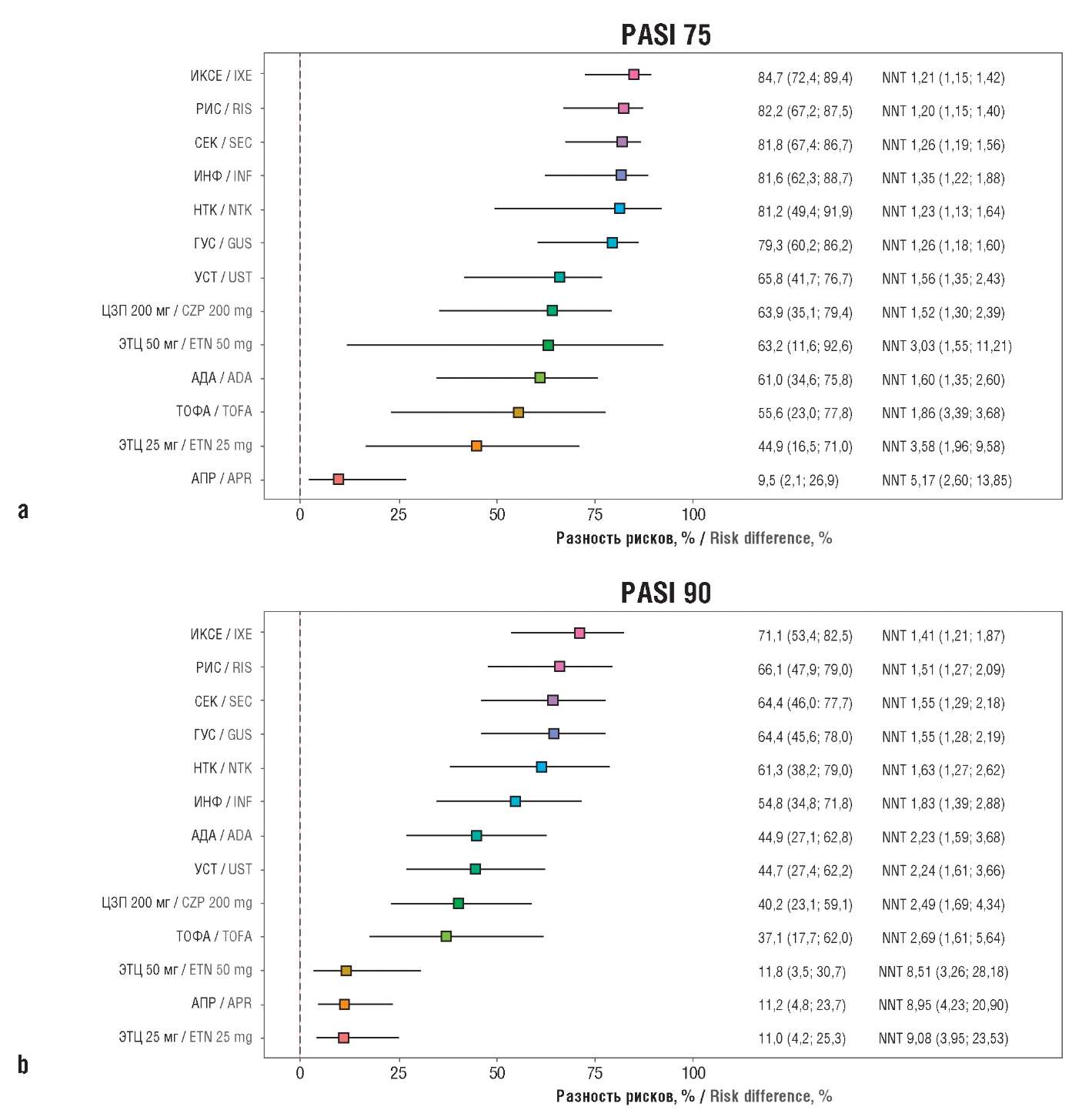
Рисунок 5. Значения разности рисков и числа пациентов,
которых необходимо пролечить для достижения одного ответа на терапию
(англ. number needed to treat, NNT) таргетных препаратов
относительно плацебо для PASI 75 (a) и PASI 90 (b).
PASI (англ. Psoriasis Area and Severity Index, PASI) 75/90 – индекс площади поражения и тяжести псориаза (75/90% снижение тяжести заболевания по сравнению с исходным уровнем); ИКСЕ – иксекизумаб; РИС – рисанкизумаб; СЕК – секукинумаб; ИНФ – инфликсимаб; НТК – нетакимаб; ГУС – гуселькумаб; УСТ – устекинумаб; ЦЗП – цертолизумаба пэгол; ЭТЦ – этанерцепт; АДА – адалимумаб; ТОФА – тофацитиниб; АПР – апремиласт
Figure 5. Risk difference and number needed to treat (NNT) values
for targeted drugs vs. placebo for PASI 75 (a) and PASI 90 (b).
PASI – Psoriasis Area and Severity Index; 75/90 – index of the lesion area and severity of psoriasis (75/90% reduction in the severity of the disease compared to the baseline level); IXE – ixekizumab; RIS – risankizumab; SEC – secukinumab; INF – infliximab; NTK – netakimab; GUS – guselkumab; UST – ustekinumab; CZP – certolizumab pegol; ETN – etanercept; ADA – adalimumab; TOFA – tofacitinib; APR – apremilast
Стоимость таргетных препаратов, режим их применения, а также стоимость терапии представлены в Приложении 13.
Анализ CpR по критериям PASI 75/90 демонстрирует, что НТК характеризуется наименьшей величиной CpR, что согласуется с результатами предыдущего исследования [5] (рис. 6, 7). Основное отличие – результаты CpR по АПР: препарат переместился на последние строки графика, попав в группу наиболее затратных ЛП. Подробные результаты анализа CpR представлены в Приложениях 14 и 15.
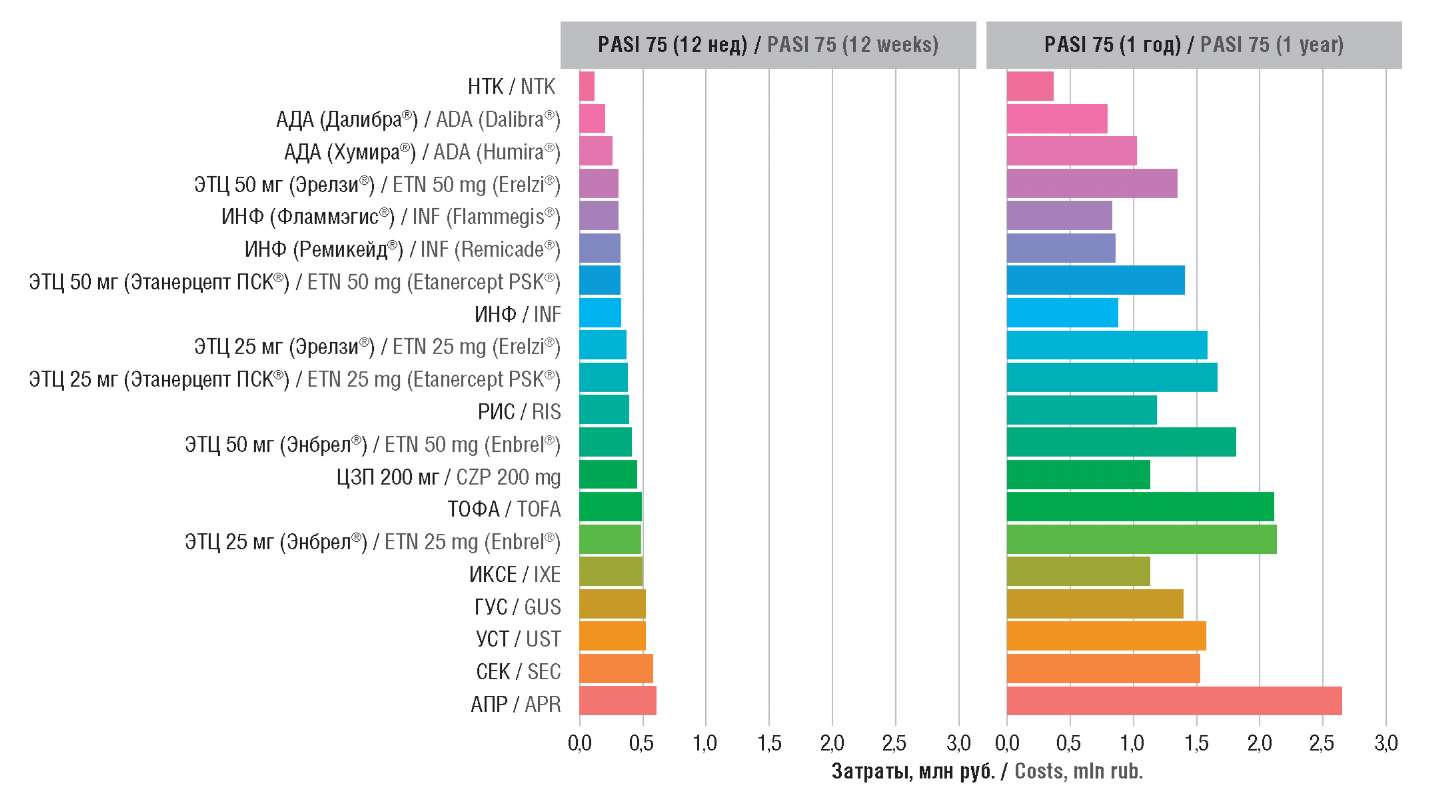
Рисунок 6. Затраты на достижение ответа на терапию по критерию PASI 75
после 12 нед и 1 года терапии.
PASI (англ. Psoriasis Area and Severity Index, PASI) 75 – индекс площади поражения и тяжести псориаза (75% снижение тяжести заболевания по сравнению с исходным уровнем); НТК – нетакимаб; АДА – адалимумаб; ЭТЦ – этанерцепт; ИНФ – инфликсимаб; РИС – рисанкизумаб; ЦЗП – цертолизумаба пэгол; ТОФА – тофацитиниб; ИКСЕ – иксекизумаб; ГУС – гуселькумаб; УСТ – устекинумаб; СЕК – секукинумаб; АПР – апремиласт
Figure 6. Сost per responder values for targeted drugs
for PASI 75 after 12 weeks and 1 year of therapy.
PASI – Psoriasis Area and Severity Index; 75 – index of the lesion area and severity of psoriasis (75% reduction in the severity of the disease compared to the baseline level); NTK – netakimab; ADA – adalimumab; ETN – etanercept; INF – infliximab; RIS – risankizumab; CZP – certolizumab pegol; TOFA – tofacitinib; IXE – ixekizumab; GUS – guselkumab; UST – ustekinumab; SEC – secukinumab; APR – apremilast
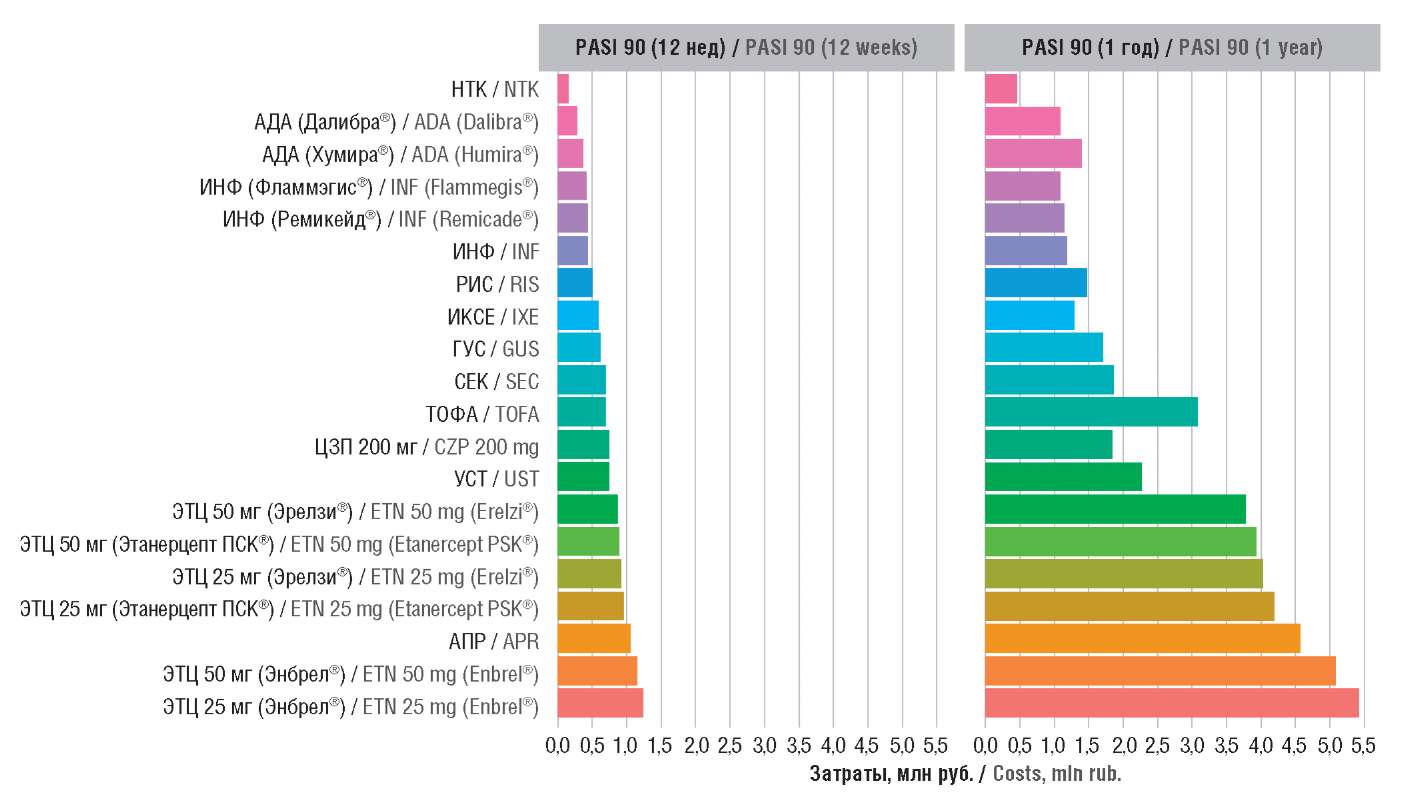
Рисунок 7. Затраты на достижение ответа на терапию по критерию PASI 90
после 12 нед и 1 года терапии.
PASI (англ. Psoriasis Area and Severity Index, PASI) 90 – индекс площади поражения и тяжести псориаза (90% снижение тяжести заболевания по сравнению с исходным уровнем); НТК – нетакимаб; АДА – адалимумаб; ИНФ – инфликсимаб; РИС – рисанкизумаб; ИКСЕ – иксекизумаб; ГУС – гуселькумаб; СЕК – секукинумаб; ТОФА – тофацитиниб; ЦЗП – цертолизумаба пэгол; УСТ – устекинумаб; ЭТЦ – этанерцепт; АПР – апремиласт
Figure 7. Сost per responder values for targeted drugs for PASI 90
after 12 weeks and 1 year of therapy.
PASI – Psoriasis Area and Severity Index; 90 – index of the lesion area and severity of psoriasis (90% reduction in the severity of the disease compared to the baseline level); NTK – netakimab; ADA – adalimumab; INF – infliximab; RIS – risankizumab; IXE – ixekizumab; GUS – guselkumab; SEC – secukinumab; TOFA – tofacitinib; CZP – certolizumab pegol; UST – ustekinumab; ETN – etanercept; APR – apremilast
ОБСУЖДЕНИЕ / DISCUSSION
По сравнению с предшествующим опубликованным систематическим обзором [4], в данное исследование были дополнительно включены 22 публикации, описывающие результаты оценки эффективности применения таргетных препаратов в 23 РКИ. Добавленные исследования включали в себя как новые РКИ (см. Приложение 3: 1–5, 8, 9, 11–13, 15–17, 19–21), появившиеся после публикации систематического обзора, так и исследования по препарату РИС (см. Приложение 3: 6, 7, 10, 14, 18, 22), который недавно зарегистрирован в РФ и не был включен в исходный поиск. Увеличение размера выборки и статистической мощности сетевого метаанализа позволили выявить ранее не идентифицированные значимые различия между ЛП по частоте ответов PASI и другим исходам. Скорее всего, это обусловлено включением РКИ с прямым сравнением препаратов, а не только с группой плацебо (см. Приложение 3: 1, 3, 5, 16–18, 20, 22).
По результатам обновления сетевого метаанализа РИС попал в группу наиболее эффективных ЛП для терапии взрослых пациентов со среднетяжелым и тяжелым бляшечным ПсО наряду с НТК, ГУС, ИКСЕ и СЕК. По всем проанализированным исходам эффективности РИС был включен в тройку препаратов с самыми высокими рангами согласно распределению SUCRA (см. рис. 3).
По результатам анализа PASI 90 после 12 нед терапии установлено отсутствие статистически значимых различий у ИНФ по сравнению с ГУС и НТК, хотя в первоначальном исследовании ИНФ характеризовался сопоставимой эффективностью по данному показателю только с СЕК. В то же время ранее АДА и УСТ уступали ИНФ в эффективности по PASI 90, а в данном анализе статистически значимых различий выявлено не было. Появление новых сведений по ТОФА позволило сравнить его эффективность по этому показателю с другими ЛП и выявить его превосходство над ЭТЦ, АПР и плацебо, а также сопоставимую эффективность с НТК, ИНФ, АДА, УСТ и ЦЗП. Показаны более высокие значения показателя NNT для достижения PASI 90, что обусловлено ростом требований к его достижению.
Как и в исходном систематическом обзоре, не все ЛП были включены в анализ по PASI 100 в связи с отсутствием данных (не включены ЭТЦ, ЦЗП, ТОФА и АПР). По этому показателю ИКСЕ продемонстрировал статистически значимое преимущество по сравнению с ГУС, хотя до этого препараты характеризовались сопоставимой эффективностью.
По исходу PGA/IGA 0/1 после 12 нед терапии ИНФ показал превосходство над всеми препаратами, кроме ИКСЕ, РИС и ГУС, что подтвердило результаты исходного сетевого метаанализа. Однако дополнительные данные по эффективности препарата позволили выявить статистически значимое преимущество ИНФ по сравнению с СЕК. В обновленном анализе сохранялось превосходство иИЛ-17 (за исключением НТК) и иИЛ-23 (РИС, ГУС) над иФНОα (АДА, ЦЗП и ЭТЦ), иИЛ-12/23 (УСТ) и малыми молекулами (АПР и ТОФА).
Обновление сетевого метаанализа особенно повлияло на сравнение ЛП по показателю DLQI, т.к. удалось включить в анализ препараты, по которым ранее отсутствовали данные (ТОФА, РИС, СЕК и АДА). ТОФА продемонстрировал самую высокую эффективность по этому показателю и превосходство над иФНОα (кроме ЭТЦ 50 мг), иИЛ-17 СЕК и иФДЭ4 АПР. Все иФНОα обладали эффективностью, сопоставимой между собой, а также с АПР и СЕК, в то время как в опубликованном сетевом метаанализе УСТ и ИНФ демонстрировали преимущество в эффективности. По результатам обновленного исследования ИКСЕ, РИС и ГУС характеризовались отсутствием статистически значимых различий по сравнению с ТОФА, АПР, ЦЗП и ЭТЦ.
Полученные выводы согласуются с результатами других недавно опубликованных сетевых метаанализов сравнительной эффективности таргетных ЛП в терапии среднетяжелого и тяжелого бляшечного ПсО [9][10–12]. Например, авторы кокрейновского обзора [10] доказали, что иИЛ-17 (ИКСЕ, СЕК и др.), иИЛ-23 (РИС и ГУС) и иФНОα ИНФ значительно эффективнее по показателю PASI 90, чем УСТ и другие иФНОα (АДА, ЦЗП, ЭТЦ). По результатам нашего исследования, с точки зрения достижения чистой или почти чистой кожи (PASI 100) ИКСЕ был связан с самым высоким значением SUCRA, а РИС характеризовался вторым рангом, что также подтвердили авторы сетевого метаанализа, проведенного ранее Британской ассоциацией дерматологов [11]. Исследователи из Японии [12] продемонстрировали, что ИКСЕ и РИС связаны с самыми высокими показателями ответа PASI 90 и PASI 100 и самыми высокими значениями SUCRA.
Анализ эффективности препаратов по классам отражает тенденции последних лет в реальной клинической практике. Перечень ГИБП для терапии пациентов с ПсО в РФ существенно расширился. В настоящее время активно применяются не только иФНОα и иИЛ-12/23, но и препараты более новых классов – иИЛ-17 и иИЛ-23 [13], которые показали высокую эффективность в рамках проведенного сетевого метаанализа. Появление в арсенале практического здравоохранения ГИБП классов иИЛ-17 и иИЛ-23 позволило добиваться амбициозных целей лечения (PASI 90, PASI 100) [14], в то время как опыт многолетнего применения иФНОα свидетельствует о доказанном в условиях реальной клинической практики возможном снижении терапевтического ответа при долгосрочном их применении [14][15].
Результаты анализа затрат на достижение ответа за 12 нед и 1 год терапии привели к схожим выводам. НТК показал низкое значение NNT и характеризовался наименьшими затратами на достижение ответа; аналогичные результаты он демонстрирует в других нозологиях: анкилозирующий спондилит [16][17] и ПсА [18]. Несмотря на высокие показатели NNT для некоторых препаратов (АДА, ЭТЦ, ИНФ), выход биоаналогов способствует снижению стоимости терапии и повышает ее доступность для пациентов [19–21].
В данном обзоре рассматривалась оценка показателей эффективности после 10–16 нед терапии – клинически значимого индукционного периода для оценки эффективности ГИБП [22]. Несмотря на то что согласно клиническим рекомендациям оптимальным периодом оценки считается 12 нед лечения [2], все чаще в РКИ новых препаратов исследователи оценивают показатели после 16 нед (см. Приложение 3: 5–7, 9, 10, 14, 17, 18, 22). Это может быть связано с тенденцией на урежение режима применения ГИБП как в период индукции, так и в долгосрочной перспективе: в первый год терапии ГУС необходимо 8 введений, а РИС – всего 6, в то время как 1 год терапии ЭТЦ состоит из 52 введений, а АДА – из 27 (согласно действующим в РФ инструкциям по медицинскому применению).
Для проведения будущих систематических обзоров необходимо больше информации об участниках РКИ, чтобы обеспечить систематический анализ подгрупп для биологически наивных пациентов. ПсО часто протекает с ПсА или другими сопутствующими системными заболеваниями [23], поэтому становятся актуальны РКИ на более широкой популяции с оценкой эффективности препаратов в разных подгруппах, а также исследования последовательностей ГИБП [24–26]. Кроме того, будущие исследования должны предоставлять адекватное описание данных, касающихся других важных модификаторов потенциального эффекта, таких как предыдущее системное лечение, наличие у участников избыточного веса или ожирения, продолжительность ПсО, его исходная тяжесть и наличие ПсА.
После того как установлено преимущество ЛП по сравнению с плацебо, только прямые сравнения эффективности между различными ЛП будут полезны для врачей как основная доказательная база сравнительной клинической эффективности препаратов. Необходимы дополнительные сравнения между биологическими агентами (иИЛ-17 по сравнению с иИЛ-12/23, иИЛ-23 по сравнению с иИЛ-12/23, иФНОα по сравнению с иИЛ-12/23).
Ограничения исследования / Limitations of the study
Ряд результатов оценки сравнительной эффективности таргетных ЛП, полученных в рамках данного систематического обзора (в т.ч. превосходство в эффективности иИЛ-17, иИЛ-12/23 и некоторых иФНОα (ИНФ) по сравнению с малыми молекулами), не отражает реальную клиническую практику. В настоящее время биологические методы терапии позиционируются регулирующими органами как методы третьей линии терапии с установлением обязательных критериев назначения, которым должны соответствовать пациенты (среднетяжелое или тяжелое течение заболевания после неэффективности предыдущей терапии, непереносимость или противопоказания к базисным системным препаратам) [2]. Несмотря на использование индексов PASI, отсутствуют единые стандарты по интерпретации ПсО, в результате чего понятия среднетяжелой и тяжелой степеней вариативны, и это приводит к откладыванию момента назначения ГИБП пациентам. Кроме того, специалисты вынуждены ограничивать закупку ГИБП ввиду нехватки бюджета и недостатка информации для обоснования финансирования конкретного препарата.
Для лечения пациента с ПсО препаратами ГИБП в Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2022 г. и на плановый период 2023 и 2024 гг. указано, что можно воспользоваться квотами высокотехнологичной медицинской помощи, однако их число ограничено и получить такую помощь можно только в лечебно-профилактическом учреждении третьего уровня, что препятствует широкому распространению такого метода, особенно для пациентов, проживающих в районных центрах, поселках, деревнях. На лечение тяжелого ПсО с применением генной терапии выделено всего 110 тыс. руб. на единицу оказания медицинской помощи, включая применение ГИБП, – немногим более средней стоимости одного введения большей части таргетных ЛП, причем эта цифра включает не только закупку лекарств, но и ряд других позиций. Также существует возможность обеспечения пациентов со среднетяжелым и тяжелым ПсО таргетной терапией в рамках регионального бюджета, но региональные бюджеты по большей части дефицитны и не имеют тенденции к увеличению, что приводит к созданию реестра пациентов, нуждающихся в дорогостоящей терапии, но не получающих ее в короткий срок. Еще одна возможность получить ГИБП – это бюджет, выделяемый по Федеральному закону от 17 июля 1999 г. № 178-ФЗ «О государственной социальной помощи», позволяющий обеспечить больных, имеющих статус инвалида, и здесь также наблюдается проблема. Если пациент имеет инвалидность по ПсО, при получении высокоэффективной терапии она снимается и лечение в рамках данного источника финансирования прекращается.
Таким образом, вопрос выбора терапии первой линии, места ГИБП в терапии среднетяжелого и тяжелого ПсО в рамках российской системы здравоохранения до сих пор остается дискуссионным.
С клинической точки зрения развивается стратегия по долгосрочному назначению высокоэффективных и безопасных препаратов, позволяющих добиться клинической ремиссии псориаза и максимально ее пролонгировать. Необходимы препараты с высокой выживаемостью терапии, чтобы обеспечить непрерывный контроль над заболеванием, потому что сохранение клинической ремиссии в течение долгого периода времени так же важно, как и успешная ремиссия после индукционной терапии. Кроме того, лечение должно быть простым в использовании, хорошо переноситься пациентами и иметь минимальные требования к мониторингу, поскольку удобство применения также является важным вопросом при лечении хронических заболеваний, требующих длительной терапии. Наконец, стоимость препарата должна быть доступной большинству пациентов и системе здравоохранения. Однако в рамках сетевого метаанализа не оценивается удобство применения ЛП, т.к. кратность введения и лекарственная форма препаратов не учитываются.
Хотя NNT является легко понятным и очень полезным показателем для пациентов и врачей, может возникнуть вопрос о его валидности, поскольку методика расчета данного показателя требует допущения общего среднего риска контрольной группы, применимого ко всем исследованиям сети. Это довольно серьезное допущение, особенно в сетях, включающих также прямые сравнительные РКИ между активными ЛП. Выводы, полученные в нашем исследовании, ограничены выборкой исследуемой популяции (участники представлены в основном пациентами трудоспособного возраста (средний возраст 47 лет) со среднетяжелой или тяжелой степенью заболевания (с общим средним баллом PASI 21 на исходном уровне)) и индукционной фазой лечения (измерения эффективности проводились через 10–16 нед после старта терапии), что недостаточно актуально для хронического заболевания, требующего пожизненной терапии. Плацебо-контролируемые долгосрочные РКИ в таком случае являются неэтичными из-за значительного влияния на здоровье пациентов в группе плацебо. Однако долгосрочные исследования, сравнивающие эффективность различных таргетных ЛП между собой, были бы этичными и информативными. Такие долгосрочные исследования также могли бы помочь в корректировке терапии пациентов со стабильным течением заболевания.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Данное исследование представляет собой обновление систематического обзора и сетевого метаанализа эффективности таргетных препаратов для терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным ПсО. Мы использовали метарегрессионный анализ и интерпретировали результаты модели случайных эффектов с поправкой на ответ в группе плацебо в связи с высокой гетерогенностью популяции и существенными различиями в плацебо-эффекте в отобранных РКИ. Также были обновлены значения NNT и CpR.
По результатам обновленного сетевого метаанализа иИЛ-17 НТК и ИКСЕ, а также иИЛ-23 ГУС и РИС продемонстрировали высокую эффективность по сравнению с другими таргетными препаратами для лечения вульгарного ПсО как по доле пациентов, достигших PASI 75, так и по другим исходам (PASI 90/100, PGA/IGA 0/1, DLQI) после 12 нед терапии. При этом НТК характеризовался наименьшей величиной CpR по критериям PASI 75/90 после 12 нед и 1 года терапии.
1. Выражается числом от 0% до 100% и отражает общий рейтинг ЛП в сети доказательств: чем ближе к 100%, тем выше вероятность попадания ЛП в верхний ранг.
Список литературы
1. Michalek I.M., Loring B., John S.M. A systematic review of worldwide epidemiology of psoriasis. J Eur Acad Dermatol Venereol. 2017; 31 (2): 205–12. https://doi.org/10.1111/jdv.13854.
2. Клинические рекомендации. Псориаз (2020). URL: https://www.rodv.ru/upload/iblock/aa2/aa20a2fc65b13df3899140167777092d.pdf (дата обращения 10.02.2022).
3. Хисматуллина З.Р., Аминева А.М., Курочкин Д.П. и др. Псориаз, псориатический артрит, метаболические нарушения и сердечнососудистые заболевания. Что общего? Клиническая дерматология и венерология. 2020; 19 (2): 139–47. https://doi.org/10.17116/klinderma202019021139.
4. Griffiths C.E., Barker J.N. Pathogenesis and clinical features of psoriasis. Lancet. 2007; 370 (9583): 263–71. https://doi.org/10.1016/S0140-6736(07)61128-3.
5. Толкачева Д.Г., Соколова В.Д., Младов В.В. Эффективность и безопасность таргетных лекарственных препаратов в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации. Медицинские технологии. Оценка и выбор. 2019; 4: 76–86. https://doi.org/10.31556/2219-0678.2019.38.4.076-086.
6. Бакулев А.Л., Младов В.В., Соколова В.Д., Толкачева Д.Г. Таргетные лекарственные препараты в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации: число пациентов, которых необходимо пролечить для достижения ответа на терапию, и затраты на его достижение. Медицинские технологии. Оценка и выбор. 2020; 42 (4): 58–74. https://doi.org/10.17116/medtech20204204158.
7. Омельяновский В.В., Хачатрян Г.Р., Никитина А.В. и др. Методические рекомендации по выполнению сетевого метаанализа. М.; 2019. URL: https://rosmedex.ru/wp-content/uploads/2020/10/mr-po-vypolneniyu-setevogo-meta-analiza.pdf (дата обращения 10.02.2022).
8. Davies C., Cipriani A., Ioannidis J.P., et al. Lack of evidence to favor specific preventive interventions in psychosis: a network metaanalysis. World Psychiatry. 2018; 17 (2): 196–209. https://doi.org/10.1002/wps.20526.
9. Sterne J.A., Savović J., Page M.J., et al. RoB 2: a revised tool for assessing risk of bias in randomised trials. Br Med J. 2019; 366: I4898. https://doi.org/10.1136/bmj.l4898.
10. Sbidian E., Chaimani A., Afach S., et al. Systemic pharmacological treatments for chronic plaque psoriasis: a network metaanalysis. Cochrane Database Syst Rev. 2020; 1 (1): CD011535. https://doi.org/10.1002/14651858.CD011535.pub3.
11. Armstrong A.W., Soliman A.M., Betts K.A., et al. Comparative efficacy and relative ranking of biologics and oral therapies for moderate-to-severe plaque psoriasis: a network meta-analysis. Dermatol Ther (Heidelb). 2021; 11 (3): 885–905. https://doi.org/10.1007/s13555-021-00511-1.
12. Mahil S.K., Ezejimofor M.C., Exton L.S., et al. Comparing the efficacy and tolerability of biologic therapies in psoriasis: an updated network meta-analysis. Br J Dermatol. 2020; 183 (4): 638–49. https://doi.org/10.1111/bjd.19325.
13. Бакулев А.Л. Современные проблемы генно-инженерной биологической терапии больных псориазом. Вестник дерматологии и венерологии. 2020; 97 (2): 51–7. https://doi.org/10.25208/vdv1109.
14. Nast A., Jacobs A., Rosumeck S., Werner R.N. Efficacy and safety of systemic long-term treatments for moderate-to-severe psoriasis: a systematic review and meta-analysis. J Invest Dermatol. 2015; 135 (11): 2641–8. https://doi.org/10.1038/jid.2015.206.
15. Thaçi D., Blauvelt A., Reich K., et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate to severe plaque psoriasis: CLEAR, a randomized controlled trial. J Am Acad Dermatol. 2015; 73 (3): 400–9. https://doi.org/10.1016/j.jaad.2015.05.013.
16. Mladov V., Sokolova V., Tolkacheva D. PBI16 number needed to treat and incremental costs per responder for biologics in adult patients with active radiographic axial spondyloarthritis in the Russian Federation. Value in Health. 2021; 24 (Suppl. 1): S17. https://doi.org/10.1016/j.jval.2021.04.087.
17. Sokolova V., Mladov V., Tolkacheva D. PBI15 biologics to treat adults with active radiographic axial spondyloarthritis in the Russian Federation: number needed to treat and cost per responder. Value in Health. 2021; 24 (Suppl. 1): S17. https://doi.org/10.1016/j.jval.2021.04.086.
18. Sokolova V., Mladov V., Tolkacheva D. POSC283 number needed to treat and incremental costs per responder for biologics and targeted synthetic drugs in adult patients with active psoriatic arthritis in the Russian Federation. Value in Health. 2022; 25 (Suppl.): S189. https://doi.org/10.1016/j.jval.2021.11.920.
19. Бакулев А.Л., Младов В.В., Соколова В.Д., Толкачева Д.Г. Таргетные лекарственные препараты в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации: число пациентов, которых необходимо пролечить для достижения ответа на терапию, и затраты на его достижение. Медицинские технологии. Оценка и выбор. 2020; 42 (4): 58–74. https://doi.org/10.17116/medtech20204204158.
20. Barker J., Baker H., Nadeem A., et al. Health economic assessment of optimal biological treatment for moderate-to-severe psoriasis. Clin Drug Investig. 2021; 41 (11): 1011–20. https://doi.org/10.1007/s40261-021-01089-4.
21. Hendrix N., Ollendorf D.A., Chapman R.H., et al. Cost-effectiveness of targeted pharmacotherapy for moderate to severe plaque psoriasis. J Manag Care Spec Pharm. 2018; 24 (12): 1210–7. https://doi.org/10.18553/jmcp.2018.24.12.1210.
22. Fahrbach K., Sarri G., Phillippo D.M., et al. Short-term efficacy of biologic therapies in moderate-to-severe plaque psoriasis: a systematic literature review and an enhanced multinomial network meta-analysis. Dermatol Ther (Heidelb). 2021; 11 (6): 1965–98. https://doi.org/10.1007/s13555-021-00602-z.
23. Насонов Е.Л., Коротаева Т.В., Лила А.М., Кубанов А.А. Можно ли предотвратить развитие псориатического артрита у пациентов с псориазом? Научно-практическая ревматология. 2019; 57 (3): 250–4. https://doi.org/10.14412/1995-4484-2019-250-254.
24. Egeberg A., Danø A., Pedersen M.H., et al. Modeling the optimal sequence of biologic therapies in plaque psoriasis in Spain. J Med Econ. 2021; 24 (1): 1134–42. https://doi.org/10.1080/13696998.2021.1970953.
25. Klijn S.L., van den Reek J.M., van de Wetering G., et al. Biologic treatment sequences for plaque psoriasis: a cost-utility analysis based on 10 years of Dutch real-world evidence from Bio CAPTURE. Br J Dermatol. 2018; 178 (5): 1181–9. https://doi.org/10.1111/bjd.16247.
26. Mauskopf J., Samuel M., McBride D., et al. Treatment sequencing after failure of the first biologic in cost-effectiveness models of psoriasis: a systematic review of published models and clinical practice guidelines. Pharmacoeconomics. 2014; 32 (4): 395–409. https://doi.org/10.1007/s40273-014-0130-5.
Об авторах
В. Д. СоколоваРоссия
независимый эксперт исследовательских проектов Проектного офиса Северо-Западного института управления,
Краснопресненская наб., д. 2, Москва 103274
Н. А. Саблева
Россия
независимый эксперт исследовательских проектов Проектного офиса Северо-Западного института управления,
Краснопресненская наб., д. 2, Москва 103274
В. В. Младов
Россия
аспирант,
Университетская наб., д. 7–9, Санкт-Петербург 199034
Д. Г. Толкачева
Россия
независимый эксперт исследовательских проектов Проектного офиса Северо-Западного института управления,
Краснопресненская наб., д. 2, Москва 103274
Дополнительные файлы

|
1. ПРИЛОЖЕНИЯ | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(2MB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Соколова В.Д., Саблева Н.А., Младов В.В., Толкачева Д.Г. Эффективность таргетных лекарственных препаратов в терапии взрослых пациентов со среднетяжелым и тяжелым вульгарным псориазом в Российской Федерации: обновление систематического обзора. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022;15(1):131-144. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.128
For citation:
Sokolova V.D., Sableva N.A., Mladov V.V., Tolkacheva D.G. Efficacy of targeted drugs for the treatment of adults with moderate-to-severe plaque psoriasis in the Russian Federation: a systematic literature review update. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2022;15(1):131-144. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.128

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.






































