Перейти к:
Фармакоэкономическое исследование пероральной противоопухолевой терапии: результаты комбинированного ABC/VEN- и частотного анализа
https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.318
Аннотация
Актуальность. Современная онкология столкнулась с парадоксальной ситуацией: стремительный рост стоимости противоопухолевой терапии не всегда сопровождается пропорциональным увеличением ее эффективности. Это создает серьезные экономические барьеры для систем здравоохранения по всему миру. В условиях ограниченных ресурсов особую актуальность приобретают методы рационального распределения лекарственного бюджета. Комбинированный ABC/VEN-анализ представляет собой эффективный инструмент для решения этой задачи. Такой подход особенно важен при анализе современных пероральных противоопухолевых препаратов, занимающих все более значимое место в терапии онкологических заболеваний.
Цель: оценить структуру затрат на пероральную противоопухолевую терапию методами ABC/VEN- и частотного анализа.
Материал и методы. Распределение по АВС-категориям осуществлялось согласно общепринятой методологии. В группу А (наиболее затратные препараты) вошли схемы, общая стоимость которых составила 80% от всех затраченных средств, группу С (наименее затратные) составили схемы с не более 5% всех затрат. Остальные схемы включены в группу В (менее затратные), на осуществление терапии которыми израсходовано 15% всех средств. Итоговые затраты определялись исходя из стоимости лекарственной терапии по схеме в условиях дневного стационара и количества случаев оказания медицинской помощи по данной схеме за 2022 г. Формальная методология VEN-анализа заключалась в распределении схем в соответствии с наличием содержащихся в них препаратов из Примерного перечня Всемирной организации здравоохранения основных лекарственных средств. Отдельно в части как АВС, так и VEN проанализированы данные в разрезе групп химиотерапии, гормональной терапии, таргетной терапии или комбинированной схемы лечения. Частотный анализ проведен с учетом количества госпитализаций пациентов, получивших ту или иную схему противоопухолевой терапии по данным реальной практики деперсонифицированных реестров структуры госпитализаций.
Результаты. Анализ распределения ресурсов подтвердил действие принципа Парето, при котором 80% финансовых затрат пришлось на 9,3% (95% ДИ 6,0–13,7) терапевтических схем (23 схемы), составивших высокозатратную группу А. В группу С (не более 5% затрат) вошли 164 схемы (66,7%; 95% ДИ 60,4–72,5). Остальные препараты оказались в группе В (15% затрат) – 24 схемы (9,8%; 95% ДИ 6,4–14,2). При этом 35 схем (14,2%; 95% ДИ 10,1–19,2) в 2022 г. не использовались. Распределение схем по группам VEN также было сопоставимо с рекомендуемым: 149 схем (60,6%; 95% ДИ 54,2–66,7) для группы V, 63 схемы (25,6%; 95% ДИ 20,3–31,5) для группы E и 34 схемы (13,8%; 95% ДИ 9,8–18,8) для группы N. Объединенный ABC/VEN-анализ продемонстрировал, что группа А преимущественно включает препараты группы V (52,2%). Однако в части ABC/VEN-анализа также выявлены диспропорции: обнаруженная значительная доля (39,1%) препаратов категории N в группе А требует особого внимания и указывает на необходимость создания механизмов регулирования назначений высокозатратных препаратов.
Заключение. Полученные результаты создают основу для разработки сбалансированных подходов к лекарственному обеспечению в онкологии, сочетающих принципы клинической целесообразности и экономической эффективности. Исследование обосновывает необходимость распределения средств, гарантирующих приоритетное обеспечение доказательно эффективных схем лечения в условиях ресурсных ограничений.
Ключевые слова
Для цитирования:
Агафонова Ю.А. Фармакоэкономическое исследование пероральной противоопухолевой терапии: результаты комбинированного ABC/VEN- и частотного анализа. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2025;18(2):164–174. https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.318
For citation:
Agafonova J.A. Pharmacoeconomic study of oral anticancer therapy: results of combined ABC/VEN and frequency analysis. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2025;18(2):164–174. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.318
ВВЕДЕНИЕ / INTRODUCTION
Системы здравоохранения во всем мире сталкиваются с беспрецедентным ростом финансовой нагрузки для обеспечения современного противоопухолевого лечения. По данным отчета Global Oncology Trends от IQVIA Institute for Human Data Science, глобальные расходы на противоопухолевые препараты выросли до 223 млрд долл. США в 2023 г. и, по прогнозам, повысятся до 409 млрд долл. к 2028 г. [1]. Этот стремительный рост затрат, в первую очередь, обусловлен появлением дорогостоящих таргетных препаратов и иммуноонкологических опций, стоимость которых часто превышает 100 тыс. долл. на лечение одного пациента [2].
Парадоксально, но высокая стоимость и инновационность многих современных противоопухолевых лекарственных препаратов (ЛП) далеко не всегда коррелирует с их клинической эффективностью. Как демонстрируют исследования, менее трети показаний, ускоренно одобренных с незрелыми данными о выживаемости, приводят к статистически значимому улучшению данного показателя [3]. В свою очередь, между эффективностью ЛП и его стоимостью может быть установлена обратная корреляция, что было подтверждено в исследовании J.C. Del Paggio et al. [4].
При этом фармацевтические затраты в онкологии растут быстрее, чем в других областях медицины, создавая угрозу устойчивости систем здравоохранения даже в экономически развитых странах [5]. В этих условиях особую актуальность приобретают методы рационального управления лекарственными ресурсами. Одним из эффективных инструментов для анализа и оптимизации затрат на противоопухолевую лекарственную терапию (ПОЛТ) является комбинированный ABC/VEN-анализ. Этот метод позволяет одновременно оценить как финансовую нагрузку (ABC-анализ), так и клиническую значимость (VEN-анализ) различных схем терапии [6][7].
Особую ценность ABC/VEN-анализ приобретает в условиях ограниченных ресурсов, позволяя выявлять неоправданно дорогие ЛП с низкой клинической эффективностью, жизненно важные, но недофинансируемые схемы терапии, а также резервы для оптимизации лекарственного бюджета.
Цель – оценить структуру затрат на пероральную противоопухолевую терапию методами ABC/VEN- и частотного анализа.
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
Схемы противоопухолевой терапии / Anticancer therapy regimens
Для проведения анализа за период 2022 г. была изучена информация из соответствующего году справочника схем лекарственной терапии при злокачественных новообразованиях (кроме лимфоидной и кроветворной тканей). Данный справочник входит в структуру файлов по расшифровке клинико-статистических групп (КСГ) заболеваний для оплаты медицинской помощи («Расшифровка клинико-статистических групп заболеваний для оплаты медицинской помощи, оказанной в условиях дневного стационара»1).
Из анализа были исключены схемы с точками в коде, предусматривающие перерыв между введениями ЛП, во время которого пациент может нуждаться в круглосуточном либо ежедневном наблюдении.
Все схемы ПОЛТ, включенные в соответствующие каждому анализируемому году справочники, разделены на три группы:
– схемы только с пероральными формами препаратов (включая комбинацию нескольких пероральных препаратов);
– схемы только с инъекционными формами препаратов (внутривенное, подкожное введение);
– комбинированные схемы (пероральная + иная формы).
Согласно справочнику схем лекарственной терапии при злокачественных новообразованиях (кроме лимфоидной и кроветворной тканей) за 2022 г. общее количество схем составило 668 (табл. 1). Данные анализировались без учета схем с точками в коде.
Таблица 1. Распределение схем противоопухолевой терапии с различными формами препаратов в 2022 г., n (%)
Table 1. Distribution of anticancer therapy regimens with different drug forms in 2022, n (%)
|
Схемы / Regimens |
Количество схем / Number of regimens |
|
Схемы только с пероральными формами / Regimens with only oral forms |
68 (10,2) |
|
Схемы только с инъекционными формами / Regimens with only injectable forms |
422 (63,2) |
|
Комбинированные схемы / Сombination regimens |
178 (26,6) |
|
Всего / Total |
668 (100,0) |
В дальнейший анализ брались схемы только с пероральными формами ЛП и комбинированные схемы, включающие пероральный препарат, – 68 (27,6%) и 178 (72,4%) соответственно. Итоговое количество схем составило 246 (100%).
Стоимость затрат на схему / Cost of regimen expenditures
Итоговые затраты на схему ПОЛТ определялись исходя из стоимости терапии в схеме в условиях дневного стационара (ДС) и количества случаев оказания медицинской помощи по данной схеме. Таким образом, в анализе не учитывались затраты на ведение пациента в условиях ДС, включающие затраты на фонд оплаты труда медицинских работников и прочие косвенные расходы, являющиеся частью стоимости случая оказания медицинской помощи.
Стоимость лекарственной терапии по схеме определялась по формуле:
СЛП × Дср,
где СЛП – стоимость непосредственно ЛП; Дср – среднее количество дней введения ЛП в госпитализации.
Для оценки количества случаев оказания медицинской помощи по данным схемам в ДС проведен анализ оказанной медицинской помощи в условиях ДС за 2022 г. В качестве источника использовались деперсонифицированные (обезличенные) реестры структуры госпитализаций медицинских организаций онкологического профиля.
В дальнейший анализ брались только затраты непосредственно на пеоральный ЛП в схеме.
Распределение схем по видам ПОЛТ / Distribution of regimens by ACDT types
Для проведения анализа в части определения затрат по группам ПОЛТ была выполнена разгруппировка всех 246 схем ПОЛТ. Схемы группировались в соответствии с видом ПОЛТ, к которому относятся включенные в схему препараты, а именно химиотерапия, гормональная терапия, таргетная терапия или комбинированная схема лечения.
Разделение ЛП на таргетные и иные группы (химиотерапевтические препараты, препараты гормональной терапии, комбинированные схемы) основано на данных базы препаратов реестра нормативно-справочной информации (НСИ) «Схемы противоопухолевой лекарственной терапии» актуальной на 2022 г. версии 1.28 и перечня P. Pantziarka et al. [8] (табл. 2).
Таблица 2. Распределение схем противоопухолевой терапии в соответствии с видом терапии, n (%)
Table 2. Distribution of anticancer therapy regimens according to the type of therapy, n (%)
|
Вид терапии / Type of therapy |
Количество схем / Number of regimens |
|
Гормонотерапия / Hormone therapy |
70 (28,46) |
|
Комбинированная терапия* / Сombination therapy* |
104 (42,28) |
|
Таргетная терапия / Targeted therapy |
39 (15,85) |
|
Химиотерапия / Chemotherapy |
33 (13,41) |
|
Всего / Total |
246 (100,0) |
Примечание. * В данной классификации к комбинированным схемам относились схемы с комбинацией в одной схеме препаратов из разных групп, например химиотерапевтический препарат в комбинации с таргетным препаратом.
Note. * In this classification, combination regimens refer to those that include a combination of drugs from different groups within a single regimen, such as a chemotherapeutic agent combined with a targeted drug.
Методология ABC/VEN- и частотного анализа / Methodology for ABC/VEN and frequency analysis
Дифференциация по АВС‑методологии позволяет установить категории ЛП по уровню приходящихся на них затрат. В соответствии с данными о стоимости расходов на схему ПОЛТ проведены АВС-распределение и частотный анализ схем. В группу А (наиболее затратные препараты) вошли схемы ПОЛТ, общая стоимость которых составила 80% от всех затраченных средств. В группу С (наименее затратные) включены схемы, на которые использовано не более 5% всех затрат на ПОЛТ. Остальные схемы составили группу В (менее затратные), на осуществление терапии которыми израсходовано 15% всех средств.
Методология VEN-анализа заключалась в распределении схем ПОЛТ на три группы. В классическом VEN-анализе распределение основано на степени важности: V (англ. vital) – жизненно необходимые, Е (англ. essential) – важные, и N (англ. non-essential) – несущественные препараты. Учитывая, что речь идет о противоопухолевых ЛП для всех солидных онкологических заболеваний, мы посчитали наиболее корректным проведение VEN-анализа не экспертным, а формальным методом (на основании соответствия нормативным документам – обычно утвержденным перечням и/или клиническим рекомендациям). Данный подход позволил устранить субъективность экспертной оценки, поскольку значимость конкретного противоопухолевого препарата вариабельна в зависимости от заболевания, наличия определенных мишеней для препарата и ряда других факторов. Кроме того, формальный подход позволяет обеспечить воспроизводимость результатов за счет использования унифицированных критериев.
Таким образом, формальный подход VEN-анализа заключался в распределении схем в соответствии с наличием содержащихся в них ЛП из Примерного перечня Всемирной организации здравоохранения (ВОЗ) основных лекарственных средств (англ. Model List of Essential Medicines) [9]. Данный перечень не только учитывает эффективность и клиническую значимость конкретного ЛП (как, например, шкала ESMO-MCBS2), но и включают оценку пользы для населения, влияние на бюджет, устойчивость и возможности системы здравоохранения [10]. Если препарат в схеме был включен в перечень, то схема относилась к категории V, если нет – к категории N. Если в схеме содержались оба вида ЛП, она относилась к категории E.
Отдельно в части как АВС, так и VEN проанализированы данные в разрезе групп, к которым были отнесены схемы: химиотерапия, гормональная терапия, таргетная терапия или комбинированная схема лечения. Частотный анализ проведен по количеству госпитализаций пациентов, получивших ту или иную схему ПОЛТ, по данным реальной практики деперсонифицированных реестров структуры госпитализаций.
Статистический анализ / Statistical analysis
Статистическая обработка данных проводилась в среде Microsoft Excel (Microsoft, США). Дополнительно использовалась программа StatTech v. 4.8.0 (ООО «Статтех», Россия). Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка (при числе исследуемых менее 50) или критерия Колмогорова–Смирнова (при числе исследуемых более 50). В случае отсутствия нормального распределения количественные данные представлены медианой (Me) и нижним и верхним квартилями [ Q1; Q3]. Категориальные данные описывались с указанием абсолютных значений и процентных долей, 95% доверительные интервалы (ДИ) для процентных долей рассчитывались по методу Клоппера–Пирсона. Сравнение трех и более групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с применением критерия Краскела–Уоллиса, апостериорные сравнения – с помощью критерия Данна с поправкой Холма. Сравнение процентных долей при анализе многопольных таблиц сопряженности проводилось с использованием критерия χ² Пирсона. Апостериорные сравнения выполнялись с помощью критерия χ² Пирсона с поправкой Холма. Различия считались статистически значимыми при p<0,05.
РЕЗУЛЬТАТЫ / RESULTS
АВС-анализ / ABC analysis
В группу А (наиболее затратные препараты) вошли схемы лекарственной терапии, общие затраты на которые составили 80% от всех средств. Данная группа представлена 23 схемами ПОЛТ (9,3%; 95% ДИ 6,0–13,7). В группу С (наименее затратные препараты) включены схемы ПОЛТ, на закупку которых использовано не более 5% всех затрат на медикаменты: 164 схемы (66,7%; 95% ДИ 60,4–72,5). Остальные препараты составили группу В (менее затратные), на закупку которых израсходовано 15% всех средств. Сюда вошли 24 схемы ПОЛТ (9,8%; 95% ДИ 6,4–14,2).
Дополнительно отметим, что 35 схем (14,2%; 95% ДИ 10,1–19,2), входящих в КСГ 2022 г., не использовались для оплаты случаев лечения (они составили группу D), что позволяет предположить, что они не применялись у пациентов за анализируемый период. Результаты АВС-анализа приведены на рисунке 1.
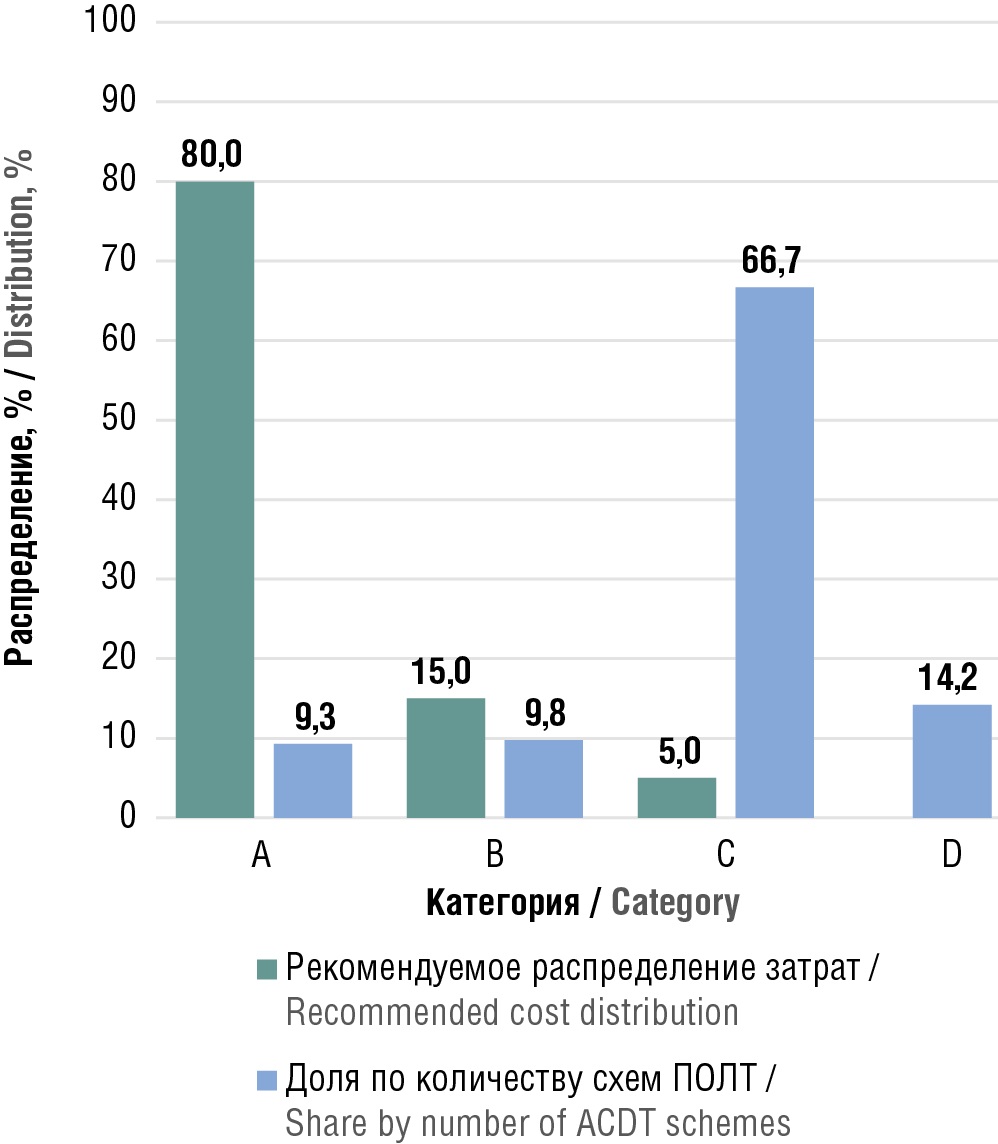
Рисунок 1. Результаты АВС-анализа (распределение схем по группам затрат).
ПОЛТ – противоопухолевая лекарственная терапия
Figure 1. Results of the ABC analysis (distribution of schemes by cost groups).
ACDT – anticancer drug therapy
Дополнительный анализ в разрезе видов терапии, к которым была отнесена схема (химиотерапия, гормональная терапия, таргетная терапия или комбинированная схема лечения), выявил тенденции, представленные в таблице 3 и на рисунке 2. В результате оценки корреляции вида терапии в зависимости от категории ABC получены статистически значимые различия (p<0,001).
Таблица 3. Распределение групп, к которым были отнесены схемы, по категориям АВС, n (%)
Table 3. Distribution of groups to which the regimens were assigned according to ABC categories, n (%)
|
Вид терапии / Therapy type |
Категория ABC / ABC category |
p |
|||
|
A |
B |
C |
D |
||
|
Гормонотерапия / Hormone therapy |
3 (13,0) |
6 (25,0) |
44 (26,8) |
17 (48,5) |
<0,001* pA–C<0,001 pA–D<0,001 pB–C<0,001 pB–D<0,001 pC–D=0,045 |
|
Комбинированная терапия / Combinaton therapy |
5 (21,7) |
4 (16,7) |
79 (48,2) |
16 (45,7) |
|
|
Таргетная терапия / Targeted therapy |
15 (65,2) |
11 (45,8) |
12 (7,3) |
1 (2,9) |
|
|
Химиотерапия / Chemotherapy |
0 (0,0) |
3 (12,5) |
29 (17,7) |
1 (2,9) |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
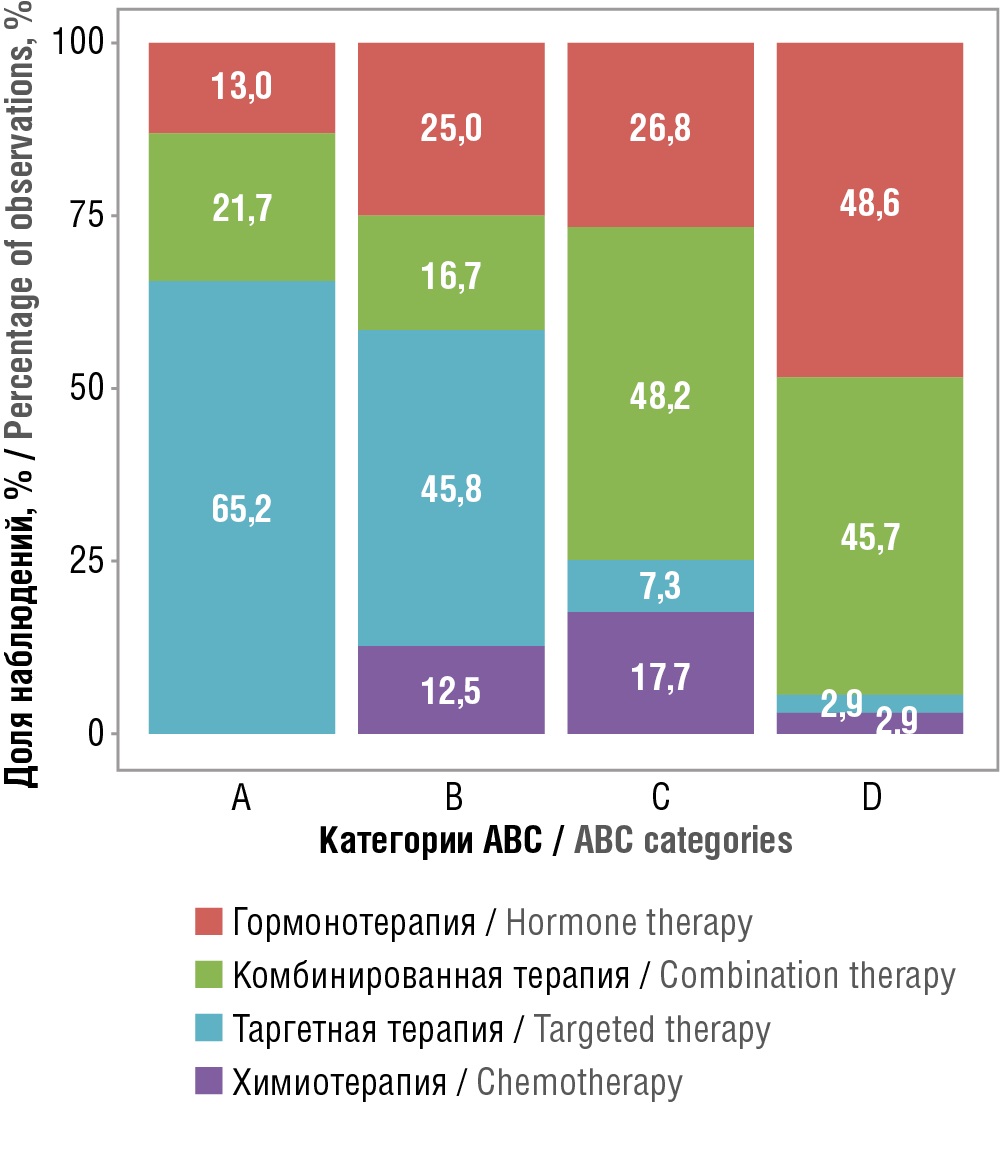
Рисунок 2. Распределение групп, к которым были отнесены схемы, по категориям АВС
Figure 2. Distribution of groups to which the regimens were assigned according to ABC categories
VEN-анализ / VEN analysis
При дальнейшей интерпретации распределения схем терапии по категориям VEN в соответствии с Примерным перечнем ВОЗ мы руководствовались рекомендуемыми показателями: 60% для группы V, 30% для группы E и 10% для группы N [11]. В группу V вошло 149 схем (60,6%; 95% ДИ 54,2–66,7) в группу Е – 63 схемы (25,6; 95% ДИ 20,3–31,5), в группу N – 34 схемы (13,8%; 95% ДИ 9,8–18,8). Данные приведены на рисунке 3.
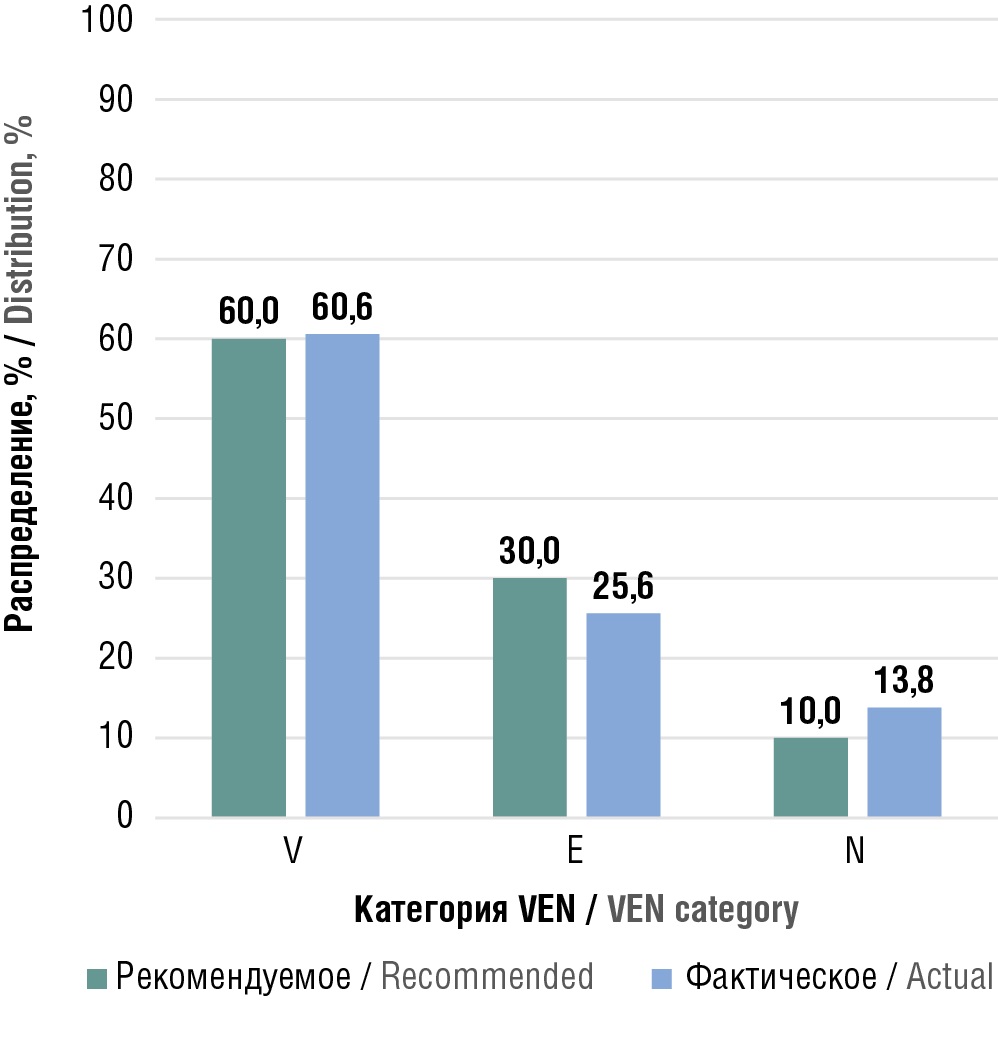
Рисунок 3. Результаты VEN-анализа в сравнении с рекомендуемыми показателями
Figure 3. Results of the VEN analysis compared to recommended values
Дополнительный анализ в разрезе видов терапии, к которым были отнесены схемы (химиотерапия, гормональная терапия, таргетная терапия или комбинированная схема лечения), выявил тенденции, представленные в таблице 4 и на рисунке 4. При оценке видов терапии в зависимости от категории VEN установлены статистически значимые различия (p<0,001).
Таблица 4. Распределение групп, к которым были отнесены схемы, по категориям VEN, n (%)
Table 4. Distribution of groups to which the regimens were assigned according to VEN categories, n (%)
|
Вид терапии / Therapy type |
Категория VEN / VEN category |
p |
||
|
V |
E |
N |
||
|
Гормонотерапия / Hormone therapy |
49 (32,9) |
19 (30,2) |
2 (5,9) |
<0,001* pV–N<0,001 pE–N<0,001 |
|
Комбинированная терапия / Combination therapy |
60 (40,3) |
36 (57,1) |
8 (23,5) |
|
|
Таргетная терапия / Targeted therapy |
16 (10,7) |
3 (4,8) |
20 (58,8) |
|
|
Химиотерапия / Chemotherapy |
24 (16,1) |
5 (7,9) |
4 (11,8) |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
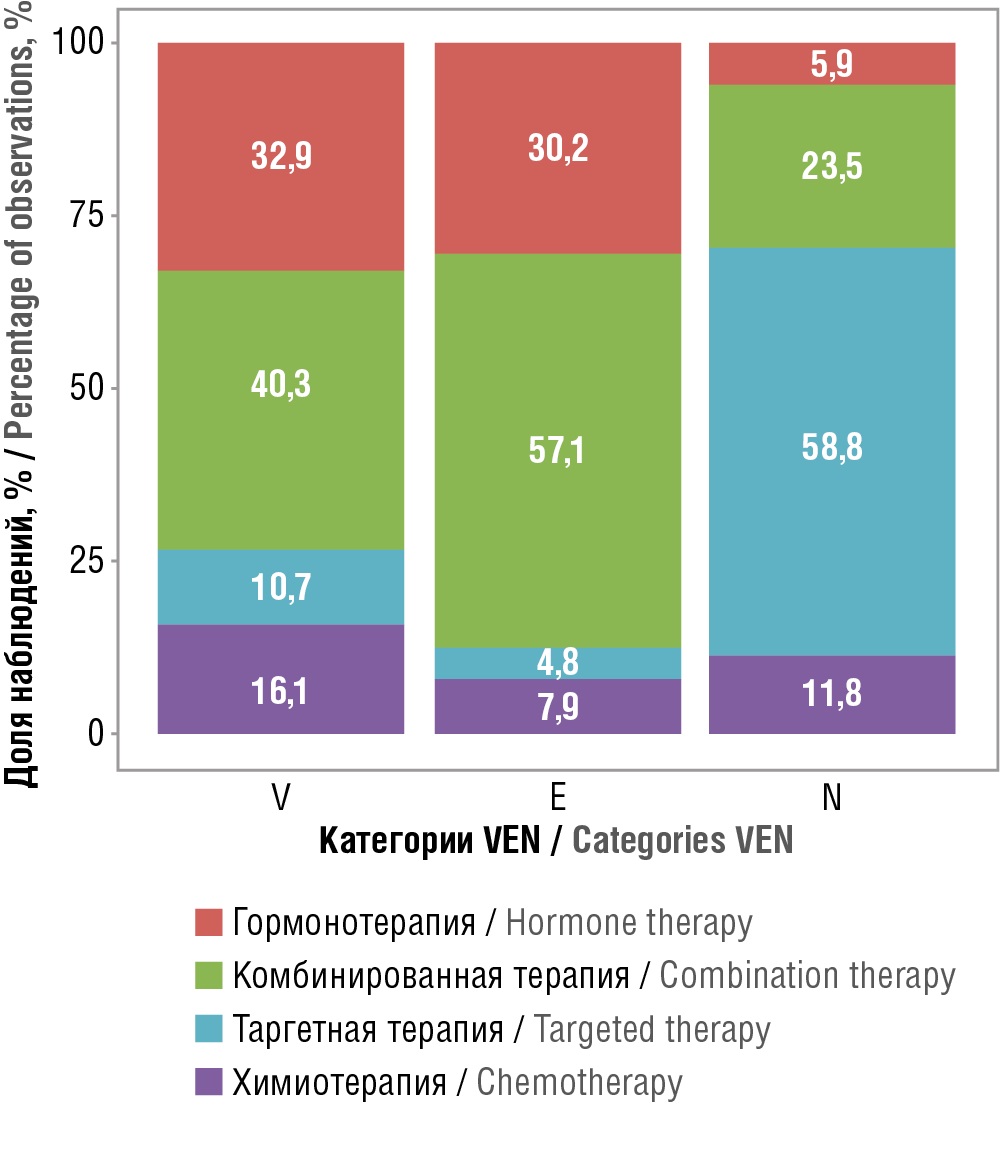
Рисунок 4. Распределение групп, к которым были отнесены схемы, по категориям VEN
Figure 4. Distribution of groups to which the regimens were assigned according to VEN categories
Объединенный ABC/VEN-анализ // Combined ABC/VEN analysis
При сравнении распределения схем по категориям VEN в зависимости от категорий ABC выявлены статистически значимые различия (p<0,001). Результаты приведены в таблице 5 и на рисунке 5.
Таблица 5. Распределение схем противоопухолевой терапии по категориям VEN в зависимости от категории ABC, n (%)
Table 5. Distribution of anticancer therapy regimens by VEN categories depending on ABC category, n (%)
|
Категория VEN / VEN сategory |
Категория ABC / ABC category |
p |
|||
|
A |
B |
C |
D |
||
|
V |
12 (52,2) |
11 (45,8) |
103 (62,8) |
23 (65,7) |
<0,001* pA–C<0,001 pA–D=0,014 pB–C=0,001 pB–D=0,025 |
|
E |
2 (8,7) |
4 (16,7) |
47 (28,7) |
10 (28,6) |
|
|
N |
9 (39,1) |
9 (37,5) |
14 (8,5) |
2 (5,7) |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
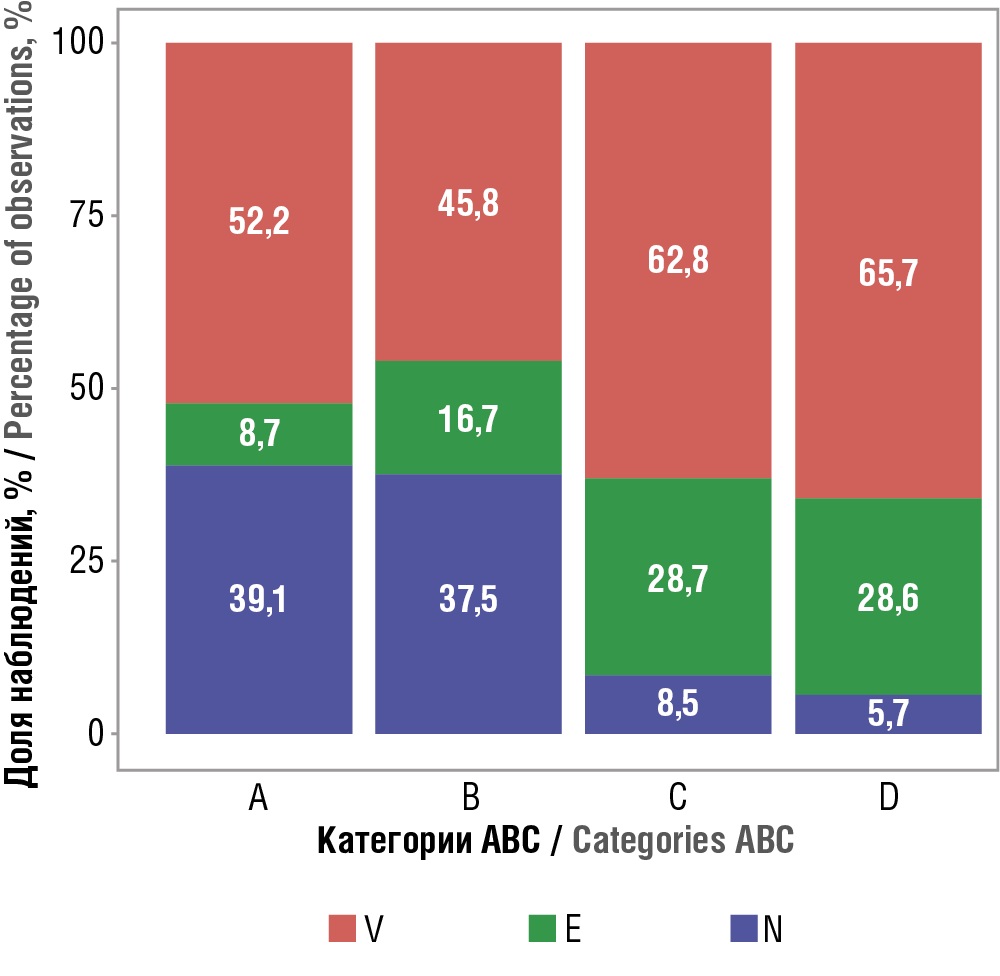
Рисунок 5. Распределение схем противоопухолевой терапии по категориям VEN в зависимости от категории ABC
Figure 5. Distribution of anticancer therapy regimens by VEN categories depending on ABC category
Внутригрупповое распределение схем по категориям в рамках объединенного ABC/VEN-анализа также представлено в таблице 6 и на рисунке 6. При сопоставлении категорий ABC в зависимости от категорий VEN тоже установлены статистически значимые различия (p<0,001).
Таблица 6. Распределение схем противоопухолевой терапии по категориям ABC в зависимости от категории VEN, n (%)
Table 6. Distribution of anticancer therapy regimens by categories ABC depending on VEN category, n (%)
|
Категория ABC / ABC category |
Категория VEN / VEN category |
p |
||
|
V |
E |
N |
||
|
A |
12 (8,1) |
2 (3,2) |
9 (26,5) |
<0,001* pV–N<0,001 pE–N<0,001 |
|
B |
11 (7,4) |
4 (6,3) |
9 (26,5) |
|
|
C |
103 (69,1) |
47 (74,6) |
14 (41,2) |
|
|
D |
23 (15,4) |
10 (15,9) |
2 (5,8) |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
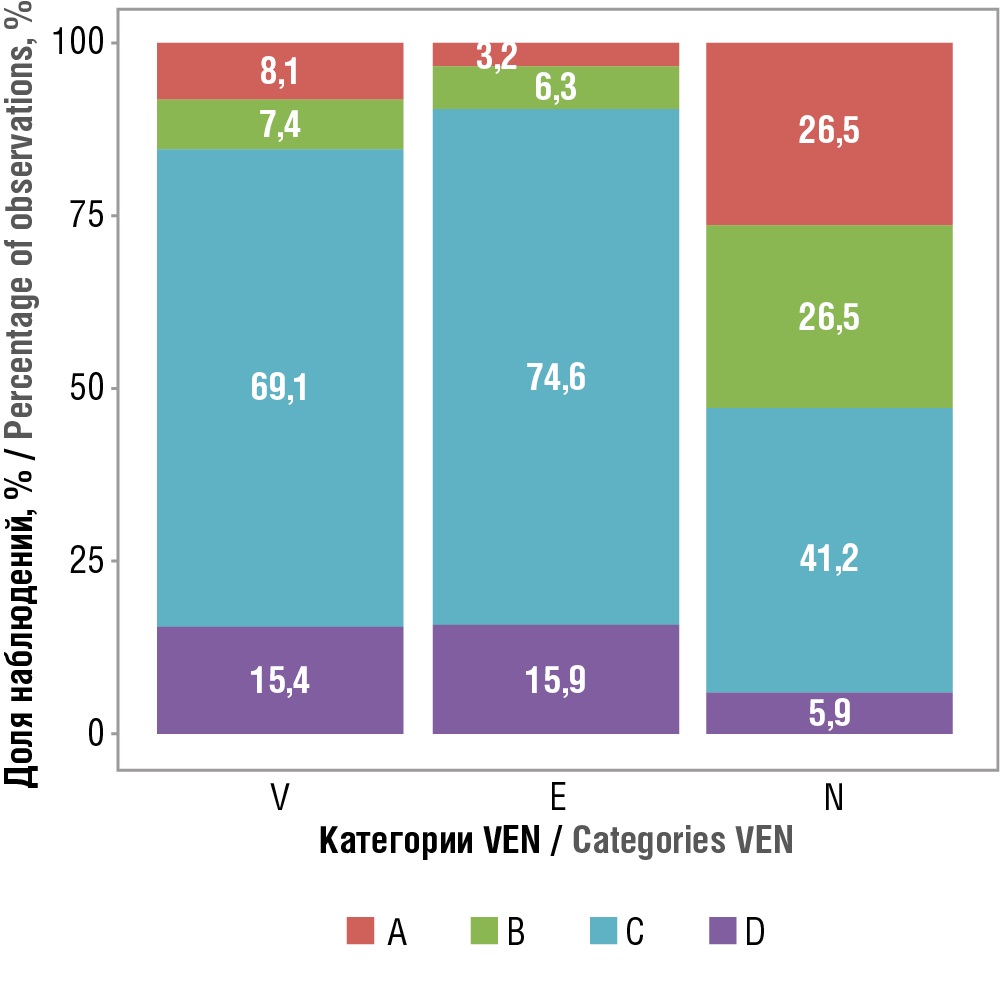
Рисунок 6. Распределение схем противоопухолевой терапии по категориям ABC в зависимости от категории VEN
Figure 6. Distribution of anticancer therapy regimens by categories ABC depending on VEN category
Частотный анализ / Frequency analysis
Медиана количества госпитализаций в схеме за 2022 г. составила 180,0 [ 30,0; 1031,5] с минимальным количеством госпитализаций в схеме, равным 2, и максимальным – 55 914.
Частотный анализ количества госпитализаций пациентов, получивших ту или иную схему ПОЛТ, показал, что более 50% всех случаев госпитализации пришлось на 10 схем ПОЛТ. Из них наибольшую долю составили схемы с применением капецитабина в дозе 2000 мг/м² в 1–14‑й дни в составе схемы XELOX (17,5%), энзалутамида в дозе 160 мг в ежедневной монотерапии (6,9%) и капецитабина в дозе 1750–2500 мг/м² в 1–14‑й дни с циклом 21 день (5,9%). На остальные 236 из 246 схем ПОЛТ пришлось 48,57%. При этом доля госпитализаций в 222 схемах из 246 составила менее 1% в каждой. Из них, как указывалось ранее, 35 схем в целом не использовались за анализируемый период.
Дополнительно выполнен анализ количества случаев госпитализации в зависимости от получаемого вида противоопухолевой терапии (табл. 7, рис. 7). Выявлены статистически значимые различия в количестве случаев госпитализации между различными видами терапии (p<0,001). При этом наибольшее число госпитализаций, несмотря на количество схем, включенных в анализ, зарегистрировано при применении таргетной терапии (Me 1650 [ 483,00; 2847,50]), что достоверно превышает показатели других видов лечения (p<0,001).
Таблица 7. Распределение количества случаев госпитализации в зависимости от вида терапии
Table 7. Distribution of the number of hospitalizations depending on therapy type
|
Вид терапии / Therapy type |
Количество случаев госпитализаций / Number of hospitalizations |
p |
||
|
Me |
Q1; Q3 |
n |
||
|
Гормонотерапия (ГТ) / Hormone therapy (HT) |
94,50 |
2,00; 387,50 |
70 |
<0,001* pТТ–ГТ<0,001 / pТТ–HТ<0,001 pТТ–КТ<0,001 / pТТ–CТ<0,001 pХТ–ТТ=0,005 / pСhТ–ТТ=0,005 |
|
Комбинированная терапия (КТ) / Combination therapy (CT) |
43,00 |
5,00; 262,25 |
104 |
|
|
Таргетная терапия (ТТ) / Targeted therapy (TT) |
1650,00 |
483,00; 2847,50 |
39 |
|
|
Химиотерапия (ХТ) / Chemotherapy (ChT) |
117,00 |
33,00; 581,00 |
33 |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
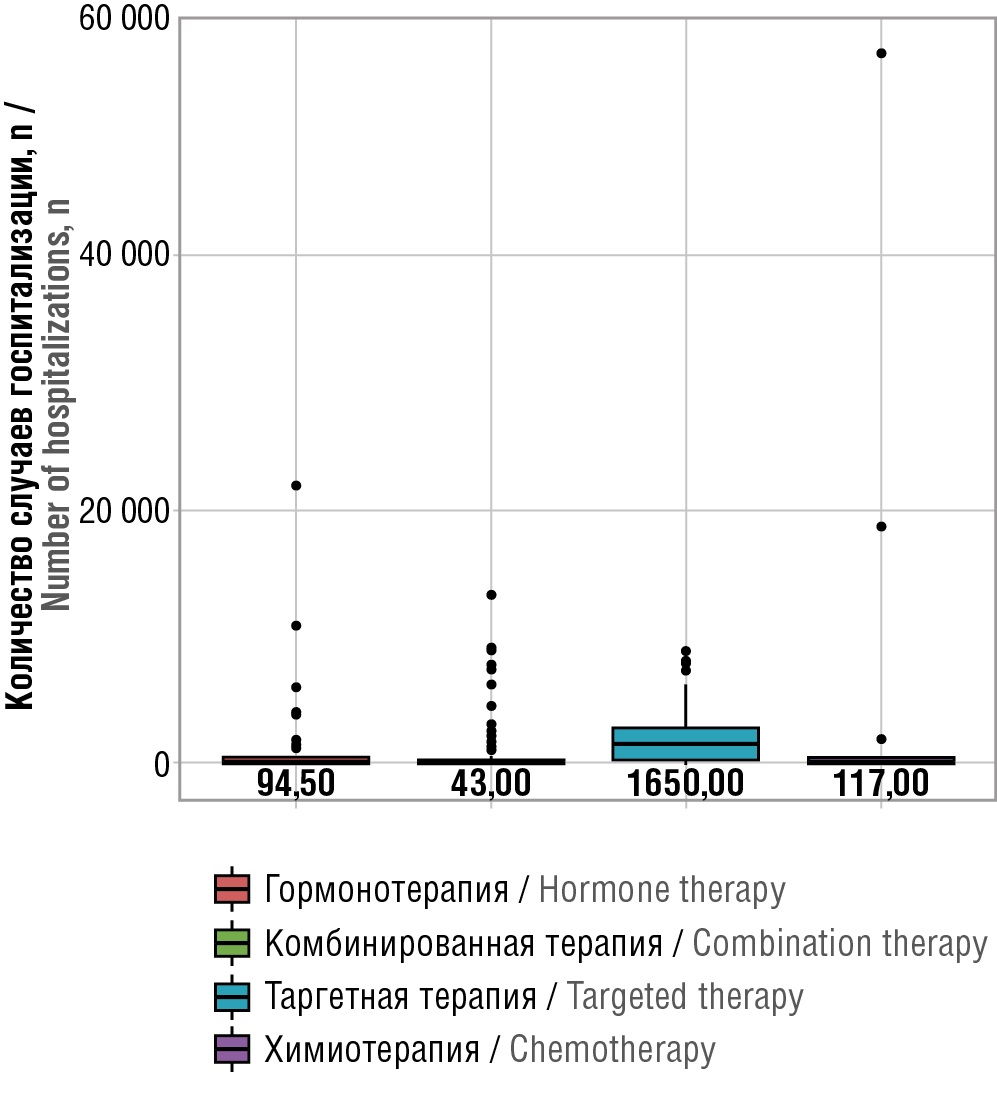
Рисунок 7. Распределение количества случаев госпитализации в зависимости от вида терапии
Figure 7. Distribution of the number of hospitalizations depending on therapy type
Дополнительно выполнен анализ количества случаев госпитализации в зависимости от категории ABC (табл. 8, рис. 8). Установлены статистически значимые различия (p<0,001). Большинство пациентов (Me 5798,00 [ 2066,50; 7987,50]) получали высокозатратную терапию категории А.
Таблица 8. Распределение количества случаев госпитализации в зависимости от категории ABC
Table 8. Distribution of the number of hospitalizations depending on ABC category
|
Вид терапии / Therapy type |
Количество случаев госпитализации / Number of hospitalizations |
p |
||
|
Me |
Q1; Q3 |
n |
||
|
A |
5798,00 |
2066,50; 7987,50 |
23 |
<0,001* pC–A<0,001 pD–A<0,001 pC–B<0,001 pD–B<0,001 pD–C<0,001 |
|
B |
1173,50 |
851,00; 2187,25 |
24 |
|
|
C |
87,50 |
18,25; 289,25 |
164 |
|
|
D |
0,00 |
0,00; 0,00 |
35 |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
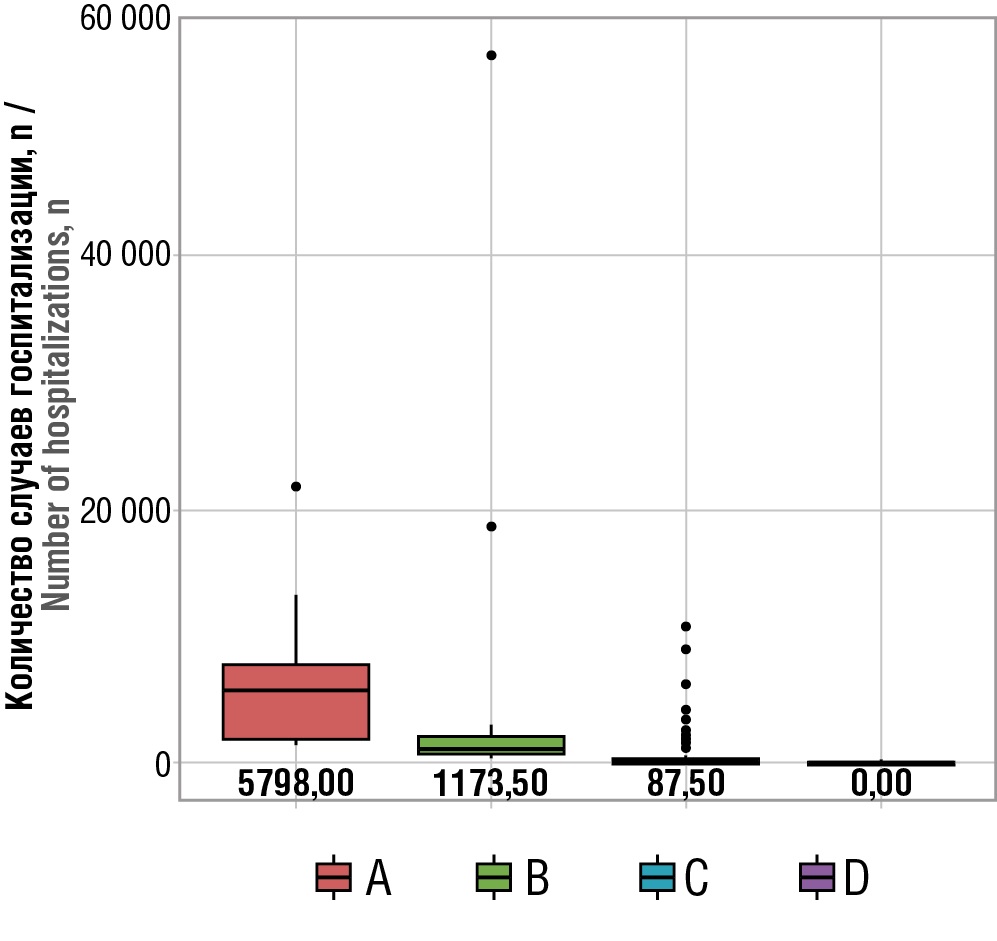
Рисунок 8. Распределение количества случаев госпитализации в зависимости от категории ABC
Figure 8. Distribution of the number of hospitalizations depending on ABC category
Также проведен анализ количества случаев госпитализации в зависимости от категории VEN (табл. 9, рис. 9). Получены статистически значимые различия (p<0,001). Важно отметить, что преимущественно госпитализации были связаны с получением терапии категории N (Me 563,50 [ 135,00; 1797,00]).
Таблица 9. Распределение количества случаев госпитализации в зависимости от категории VEN
Table 9. Distribution of the number of hospitalizations depending on VEN category
|
Категория VEN / VEN category |
Количество случаев госпитализации / Number of hospitalizations |
p |
||
|
Me |
Q1; Q3 |
n |
||
|
V |
114,00 |
7,00; 763,00 |
149 |
<0,001* pE–V=0,028 pN–V=0,008 pN–E<0,001 |
|
E |
33,00 |
4,50; 222,00 |
63 |
|
|
N |
563,50 |
135,00; 1797,00 |
34 |
|
Примечание. * Различия показателей статистически значимы (p<0,05).
Note. * Differences are statistically significant (p<0.05).
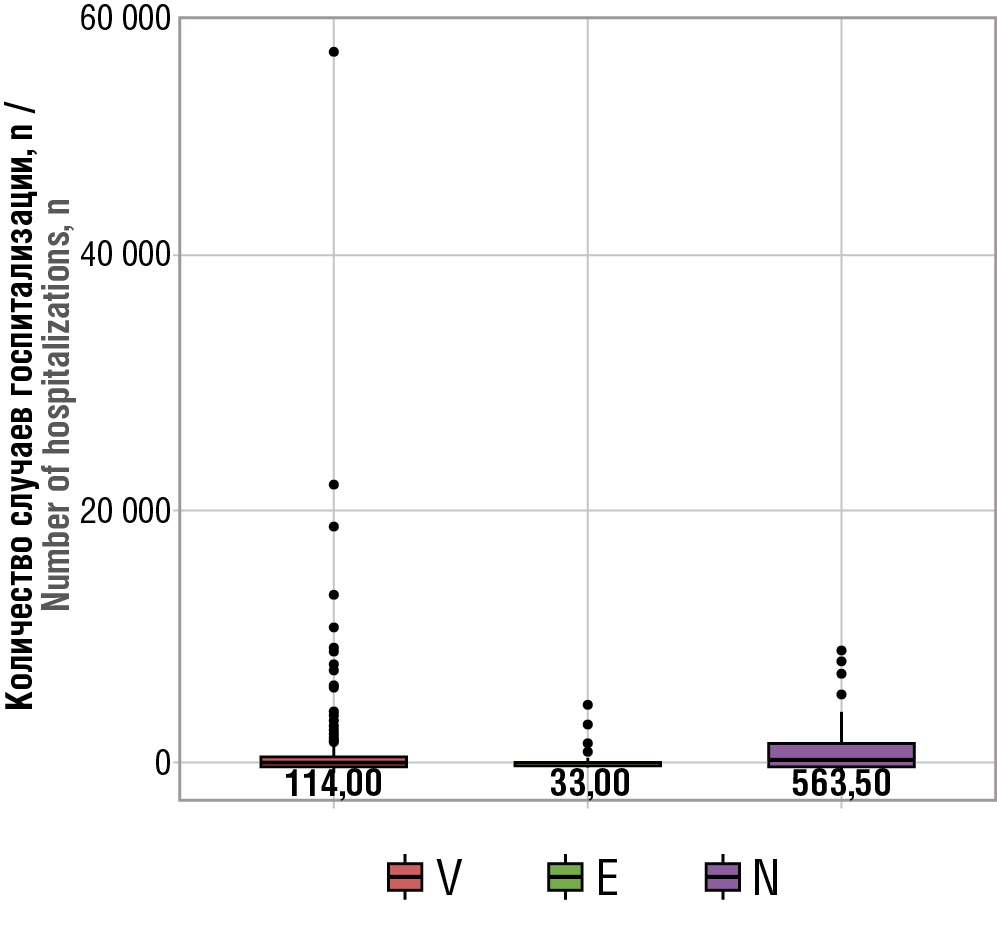
Рисунок 9. Распределение количества случаев госпитализации в зависимости от категории VEN
Figure 9. Distribution of the number of hospitalizations depending on VEN category
ОБСУЖДЕНИЕ / DISCUSSION
Проведенное исследование выявило существенные диспропорции в структуре финансирования противоопухолевой терапии, характерные для современных систем лекарственного обеспечения. Глобально анализ распределения ресурсов подтвердил действие принципа Парето, при котором 80% финансовых затрат пришлось на 9,3% терапевтических схем, составивших высокозатратную группу А. Примечательно, что более половины (52,2%) этих высокозатратных схем относятся к категории жизненно необходимых препаратов (V), что свидетельствует о рациональном подходе к распределению средств на инновационные методы лечения с доказанной эффективностью. Однако обнаруженная значительная доля (39,1%) препаратов категории N в группе А требует особого внимания, т.к. превышает описанные в литературе рекомендуемые показатели [11].
Результатом, требующим особого внимания, стало сосредоточение 62,8% жизненно необходимых препаратов (V) в группе С (всего 5% затрат). Прежде всего такой показатель мы связываем с высокой долей химиотерапевтических и гормональных препаратов, включенных в Примерный перечень ВОЗ и обладающих как высокой доказанной эффективностью, так и низкой затратностью [10][12].
Структура терапевтических групп демонстрирует выраженную поляризацию. Таргетная терапия, являющаяся основой современной онкологической помощи, составляет 65,2% в высокозатратной группе А, тогда как в низкозатратной группе С ее доля снижается до 7,3%, а в группе В равна 45,8%. Такой значительный разрыв между ценовыми категориями может свидетельствовать о существовании «бюджетных» таргетных агентов, а также о недостаточном использовании более доступных и эквивалентных аналогов при их наличии, включая дженерики и биосимиляры [13]. К данной проблеме обращаются также W.Y. Cheung et al., указывая на необходимость переоценки экономической эффективности и соотношения затрат и полезности схем лечения [14].
Особого внимания заслуживает полное отсутствие химиотерапевтических схем в группе А и их незначительное количество (12,5%) в группе В. Эта тенденция соответствует глобальному вектору развития онкологической помощи с увеличением стоимости онкологической терапии в целом во всем мире преимущественно за счет персонализированных опций [15][16]. Выявленные 35 неиспользуемых схем (группа D), среди которых преобладают (65,7%) жизненно необходимые препараты, указывают на потенциальные организационные барьеры или потерю актуальности данных протоколов лечения.
В структуре высокозатратной группы А выявлено неоптимальное распределение ресурсов – значительная доля дорогостоящих схем (А) приходится на менее значимые препараты группы N (39,1%), тогда как большинство жизненно важных схем (V) сосредоточены в низкозатратной группе С (62,8%). При этом в категории жизненно приоритетных схем в группе V 69,1% составили схемы низкозатратной группы С. Такое распределение свидетельствует о нерациональном перераспределении ресурсов в пользу менее клинически и социально значимых, но дорогостоящих терапевтических опций и указывает на необходимость пересмотра приоритетов финансирования в пользу доказательно значимых вариантов терапии.
Полученные результаты в части проведения частотного анализа указывают на существенную вариабельность нагрузки на стационарную помощь в зависимости от выбранной схемы противоопухолевого лечения. Анализ количества случаев госпитализации в зависимости от категорий ABC и VEN выявил, что наибольшее число госпитализаций связано с категорией A (наиболее дорогостоящими схемами), что подчеркивает важность проведения глубинного анализа назначения терапии в данной группе. Количество случаев госпитализации в категории V имеет высокую частоту с медианным значением 114. Однако неожиданно высокая частота использования схем категории N требует дополнительного анализа.
Полученные результаты демонстрируют необходимость разработки адаптивной системы лекарственного обеспечения, которая учитывала бы как клиническую значимость препаратов, так и экономическую эффективность их применения. Особую актуальность приобретает создание механизмов мониторинга назначений высокозатратных препаратов, например не включенных в Примерный перечень ВОЗ, а также анализ причин неиспользования значительного числа схем из категории V. Перспективным направлением также представляется учет данных реальной клинической практики при обновлении перечней схем в КСГ с дополнительным детальным анализом причин, по которым схемы не используются в клинической практике.
Проведенное исследование обосновывает необходимость разработки сбалансированной системы лекарственного обеспечения в онкологии, которая, с одной стороны, гарантирует неограниченный доступ пациентов к эффективным методам лечения, а с другой – обеспечивает рациональное использование ограниченных ресурсов здравоохранения. Следует сохранить беспрепятственный доступ пациентов к эффективным схемам лечения, поскольку ограничение терапии при онкологических заболеваниях недопустимо с медицинской и этической точек зрения. Однако критически важно внедрить мультикритериальную систему оценки противоопухолевых препаратов, учитывающую: клиническую эффективность (основанную на демонстрации выигрыша в выживаемости пациентов), социальную значимость (включающую влияние на качество жизни пациентов), фармакоэкономические параметры, воздействие на систему здравоохранения в целом. Такой мультикритериальный подход позволит оптимизировать процесс принятия решений о финансировании, обеспечивая приоритетное выделение средств для терапевтических опций с доказанной клинико-экономической эффективностью. Реализация предложенной модели будет способствовать устойчивому развитию онкологической помощи, сочетающей принципы медицинской целесообразности, социальной справедливости и экономической рациональности.
Ограничения исследования / Limitations of the study
Проведенный анализ имеет несколько методологических ограничений, которые следует учитывать при интерпретации результатов. Во-первых, исследование охватывает данные исключительно за 2022 г., что не позволяет проследить динамику изменений в структуре лекарственного обеспечения. Во-вторых, в оценку не были включены схемы терапии с точкой в коде, предусматривающие перерыв между введениями ПОЛП, во время которого пациент может нуждаться в круглосуточном либо ежедневном наблюдении. В-третьих, анализ учитывал только случаи госпитализации, финансируемые в системе обязательного медицинского страхования, без учета других возможных источников оплаты медицинской помощи.
Дополнительным ограничением можно считать распределение препаратов по группам VEN в соответствии с наличием их в Примерном перечне ВОЗ. Перечни основных лекарственных средств ВОЗ предоставляют основанные на фактических данных рекомендации по оптимизации установления приоритетов на уровне страны для дорогостоящих лекарственных средств. Таким образом, сама концепция данного перечня направлена на устранение проблем, связанных с появлением большого объема и быстрым темпом новых разработок, предлагающих незначительные выгоды по высоким ценам [10][12]. В таком случае ряд инновационных препаратов, которые либо не успели показать явных преимуществ в выживаемости, либо не достигли порога эффективности, заданного ВОЗ, не включается в перечень. Данный фактор также мог повлиять на формирование группы N.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Проведенное исследование не только выявляет ключевые диспропорции в системе лекарственного обеспечения, но и определяет конкретные направления для оптимизации, которая может способствовать формированию более сбалансированного подхода к финансированию противоопухолевой терапии. Полученные данные имеют большое значение для совершенствования лекарственной помощи и разработки эффективных стратегий распределения финансовых средств в онкологии без снижения доступности и качества терапии для пациентов. Результаты могут послужить основой для разработки рациональных подходов к финансированию онкологической помощи в условиях ограниченных ресурсов.
1. Приложение к письму Минздрава России от 4 февраля 2022 г. № 11-7/И/2-1631 «О методических рекомендациях по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования».
2. ESMO-MCBS (англ. European Society for Medical Oncology – Magnitude of Clinical Benefit Scale) – шкала величины клинической пользы Европейского общества медицинской онкологии.
Список литературы
1. Global oncology trends 2024: outlook to 2028. Annual trend report from the IQVIA Institute for Human Data Science. May 28, 2024. Available at: https://www.iqvia.com/insights/the-iqvia-institute/reports-andpublications/reports/global-oncology-trends-2024 (accessed 25.04.2025).
2. Schaft N., Dörrie J., Schuler G., et al. The future of affordable cancer immunotherapy. Front Immunol. 2023; 14: 1248867. https://doi.org/10.3389/fimmu.2023.1248867.
3. Naci H., Zhang Y., Woloshin S., et al. Overall survival benefits of cancer drugs initially approved by the US Food and Drug Administration on the basis of immature survival data: a retrospective analysis. Lancet Oncol. 2024; 25 (6): 760–9. https://doi.org/10.1016/S14702045(24)00152-9.
4. Del Paggio J.C., Sullivan R., Schrag D., et al. Delivery of meaningful cancer care: a retrospective cohort study assessing cost and benefit with the ASCO and ESMO frameworks. Lancet Oncol. 2017; 18 (7): 887–94. https://doi.org/10.1016/S1470-2045(17)30415-1.
5. Laviana A.A., Luckenbaugh A.N., Resnick M.J. Trends in the cost of cancer care: beyond drugs. J Clin Oncol. 2020; 38 (4): 316–22. https://doi.org/10.1200/JCO.19.01963.
6. Всемирная организация здравоохранения. Методы анализа использования лекарств и расходов на содействие осуществлению лекарственной политики. URL: https://iris.who.int/bitstream/handle/10665/342858/9789289055697-rus.pdf?sequence=1&isAllowed=y (дата обращения 25.0.2025).
7. Жукова О.В., Руина О.В., Хазов М.В. и др. Фармакоэпидемиологический анализ потребления лекарственных препаратов в многопрофильном стационаре – элемент управления качеством медицинской помощи и основа оценки импортозамещения. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2022; 15 (1): 51–8. https://doi.org/10.17749/2070-4909/farmakoekonomika.2022.046.
8. Pantziarka P., Capistrano I R., De Potter A., et al. An open access database of licensed cancer drugs. Front Pharmacol. 2021; 12: 627574. https://doi.org/10.3389/fphar.2021.627574.
9. World Health Organization. Model List of Essential Medicines. Available at: https://list.essentialmeds.org/ (accessed 25.04.2025).
10. Jenei K., Aziz Z., Booth C., et al. Cancer medicines on the WHO Model List of Essential Medicines: processes, challenges, and a way forward. Lancet Glob Health. 2022; 10 (12): e1860–6. https://doi.org/10.1016/S2214-109X(22)00376-X.
11. Коробейникова А.Н., Мальчикова С.В. ABC-, VEN- и частотный анализ терапии фибрилляции предсердий в условиях «типичной практики». ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2015; 8 (4): 28–31. https://doi.org/10.17749/2070-4909.2015.8.4.028-031.
12. Zhou Y., Naci H., Chen D., et al. Overall survival benefits of cancer drugs in the WHO Model List of Essential Medicines, 2015–2021. BMJ Glob Health. 2023; 8 (9): e012899. https://doi.org/10.1136/bmjgh-2023-012899.
13. Yang Y.T., Nagai S., Chen B.K., et al. Generic oncology drugs: are they all safe? Lancet Oncol. 2016; 17 (11): e493–501. https://doi.org/10.1016/S1470-2045(16)30384-9.
14. Cheung W.Y., Kornelsen E.A., Mittmann N., et al. The economic impact of the transition from branded to generic oncology drugs. Curr Oncol. 2019; 26 (2): 89–93. https://doi.org/10.3747/co.26.4395.
15. Yabroff K.R., Mariotto A., Tangka F., et al. Annual report to the nation on the status of cancer, Part 2: Patient economic burden associated with cancer care. J Natl Cancer Inst. 2021; 113 (19): 1670– 82. https://doi.org/10.1093/jnci/djab192.
16. Shin G., Kwon H.Y., Bae S. For whom the price escalates: high price and uncertain value of cancer drugs. Int J Environ Res Public Health. 2022; 19 (7): 4204. https://doi.org/10.3390/ijerph19074204.
Об авторе
Ю. А. АгафоноваРоссия
Агафонова Юлия Андреевна
Scopus Author ID: 57222346687
Покровский б-р, д. 6/20, стр. 2, Москва 109028
ул. Баррикадная, д. 2, стр. 1, Москва 123995
Что уже известно об этой теме?
► Стоимость противоопухолевой лекарственной терапии (ПОЛТ) создает беспрецедентное финансовое давление на системы здравоохранения во всем мире
► Современные исследования демонстрируют, что высокая стоимость инновационных противоопухолевых препаратов не всегда коррелирует с достижением значимых клинических результатов
► Комбинированный ABC/VEN-анализ как метод клинико-экономического анализа служит эффективным инструментом комплексной оценки финансовой нагрузки (ABC) и клинической значимости (VEN) схем ПОЛТ
Что нового дает статья?
► Выявлены диспропорции в структуре финансирования ПОЛТ, характерные для современных систем лекарственного обеспечения с акцентом на финансирование таргетных опций терапии
► Включение препаратов одного вида в разные категории при проведении ABC-анализа может свидетельствовать о существовании «бюджетных» аналогов и недостаточном использовании более доступных и эквивалентных препаратов при их наличии, в т.ч. дженериков и биосимиляров
► Примерный перечень ВОЗ для классификации препаратов по группам VEN включает только те средства, которые показали значительные преимущества в выживаемости или достигли установленного ВОЗ порога эффективности, что ограничило оценку препаратов, не продемонстрировавших такие приоритеты
Как это может повлиять на клиническую практику в обозримом будущем?
► Полученные результаты подчеркивают необходимость разработки адаптивной системы лекарственного обеспечения, которая учитывала бы как клиническую значимость препаратов, так и экономическую эффективность их применения
► Сохранение полного доступа пациентов к эффективному лечению является неоспоримым приоритетом онкологической практики, требующим при этом строгой оценки объективных показателей улучшения качества и продолжительности жизни
► Одним из возможных решений является мультикритериальная система оценки противоопухолевых препаратов с учетом клинической эффективности, социальной значимости, фармакоэкономических параметров и иных факторов, влияющих на систему здравоохранения в целом
Рецензия
Для цитирования:
Агафонова Ю.А. Фармакоэкономическое исследование пероральной противоопухолевой терапии: результаты комбинированного ABC/VEN- и частотного анализа. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2025;18(2):164–174. https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.318
For citation:
Agafonova J.A. Pharmacoeconomic study of oral anticancer therapy: results of combined ABC/VEN and frequency analysis. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2025;18(2):164–174. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2025.318

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.






































