Перейти к:
Оценка клинико-экономической целесообразности применения лекарственных препаратов эзетимиб, алирокумаб, эволокумаб и инклисиран в рамках программы льготного лекарственного обеспечения пациентов очень высокого сердечно-сосудистого риска
https://doi.org/10.17749/2070-4909/farmakoekonomika.2023.173
Аннотация
Цель: оценить клинико-экономическую целесообразность расширения программы льготного лекарственного обеспечения (ЛЛО) взрослых пациентов очень высокого сердечно-сосудистого (СС) риска, включая не достигших липидных целей на терапии статинами, за счет увеличения частоты использования лекарственных препаратов (ЛП) эзетимиб, алирокумаб, эволокумаб и инклисиран, применяемых в комбинации со статинами, по сравнению с текущей практикой ЛЛО (использование аторвастатина, симвастатина и минимальное применение других препаратов).
Материал и методы. Построена модель Маркова, характеризующая развитие атеросклеротической болезни сердца у пациентов очень высокого СС-риска и предполагающая последовательную смену гиполипидемической терапии при ее неэффективности. Модель учитывала приверженность пациентов лекарственной терапии во времени и фактор неназначения какого-либо лечения. Горизонт моделирования составил 30 лет, цикл модели – 1 год. В качестве исходов были использованы годы жизни с поправкой на качество (англ. quality-adjusted life year, QALY), добавленные годы жизни (англ. life years gained, LYG) без учета ее качества, а также вероятности наступления различных отдельных и комбинированных СС-событий. Базовый сценарий моделирования предполагал увеличение частоты назначения ингибиторов пропротеиновой конвертазы субтилизин-кексинового типа 9 (англ. рroprotein convertase subtilisin/kexin type 9, PCSK9), инклисирана и эзетимиба; дополнительно моделировались альтернативные сценарии расширения ЛЛО, включающие назначение высокоэффективной липидснижающей терапии всем пациентам, не достигшим целевых значений по холестерину липопротеинов низкой плотности (ХС-ЛПНП) на фоне приема статинов, и сценарий, подразумевающий 100% приверженность пациентов приему ЛП
Результаты. По сравнению с текущей практикой лечения пациентов очень высокого СС-риска клинико-экономическое моделирование продемонстрировало снижение частоты комбинированных исходов (комбинированное СС-событие – на 8%, расширенное комбинированное СС-событие – на 9%) и отдельных СС-событий (инфаркт – на 4%, инсульт – на 3%, нестабильная стенокардия – на 2%, реваскуляризация – на 3%) в базовом сценарии. При реализации сценариев назначения ингибиторов PCSK9 и инклисирана всем пациентам, не достигшим целевых значений ХС-ЛПНП на фоне приема статинов, снижение частоты отдельных СС-событий варьировало от 4% до 8%, а в сценарии, подразумевающем также 100% приверженность пациентов приему ЛП, снижение составило от 8% до 17% по сравнению с текущей практикой ведения пациентов, характеризующейся меньшей частотой назначения гиполипидемических ЛП, в т.ч. ЛП группы ингибиторов PCSK9 и инклисирана. Инкрементальный показатель «затраты–эффективность» (англ.
incremental cost-effectiveness ratio, ICER) за QALY в базовом сценарии составил 3 598 156 руб., ICER за LYG – 1 949 393 руб. При сопоставлении ICER c расчетным порогом готовности платить (ПГП) в Российской Федерации (рассчитанным как трехкратный размер валового внутреннего продукта на душу населения и в 2022 г. составившим 2,8 млн руб. за единицу эффекта) ICER за LYG не превышал ПГП во всех сценариях, в то время как ICER за QALY превышал ПГП на 29–44% в зависимости от реализуемого сценария.
Заключение. Расширение программы ЛЛО пациентов высокого СС-риска окажет позитивное влияние на качество и продолжительность их жизни, а также значительно снизит вероятность острых СС-событий. Сопоставление показателей ICER c расчетным ПГП позволяет заключить, что расширение программы ЛЛО является экономически эффективной организационной технологией по критерию LYG, но не является таковой по критерию QALY.
Ключевые слова
Для цитирования:
Бессонова Т.О., Мухортова П.А., Терян Р.А., Багдасаров А.Д., Мусина Н.З. Оценка клинико-экономической целесообразности применения лекарственных препаратов эзетимиб, алирокумаб, эволокумаб и инклисиран в рамках программы льготного лекарственного обеспечения пациентов очень высокого сердечно-сосудистого риска. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023;16(1):17-34. https://doi.org/10.17749/2070-4909/farmakoekonomika.2023.173
For citation:
Bessonova T.O., Mukhortova P.A., Teryan R.A., Bagdasarov A.D., Musina N.Z. Cost-effectiveness analysis of using atorvastatin, simvastatin, ezetimibe, alirocumab, evolocumab, inclisiran in adults with very high cardiovascular risk under the preferential drug provision program. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023;16(1):17-34. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2023.173
ВВЕДЕНИЕ / INTRODUCTION
Сердечно-сосудистые (СС) заболевания являются на сегодняшний день одной из основных причин инвалидизации и смертности в мире. Согласно данным Росстата, смертность от болезней системы кровообращения в Российской Федерации (РФ) в 2020 г. составила 938,5 тыс. человек, из них от ишемической болезни сердца – 508,7 тыс., в т.ч. от инфаркта миокарда – 58,1 тыс., от цереброваскулярных болезней (включая ишемический инсульт) – 278,6 тыс. [1], что демонстрирует необходимость проведения профилактических мероприятий, направленных на минимизацию частоты возникновения осложнений у пациентов с СС-заболеваниями. Одним из ключевых факторов риска развития СС-событий является атеросклероз [2].
Согласно клиническим рекомендациям для выбора тактики лечения пациента рекомендуется определение совокупного уровня СС-риска. Наиболее подвержены СС-событиям больные с высоким СС-риском: пациенты с атеросклерозом, перенесшие СС-события/вмешательства либо имеющие поражение периферических артерий или значимую атеросклеротическую бляшку, больные сахарным диабетом с поражением органов-мишеней или длительностью заболевания более 20 лет, пациенты с выраженной хронической болезнью почек, больные, имеющие риск по шкале оценки СС-риска (англ. Systematic Cоronary Risk Evaluation, SCORE) 10% и более, пациенты, имеющие семейную гиперхолестеринемию в сочетании с атеросклерозом или другими факторами риска [3].
Метод лечения атеросклеротической болезни, направленный на снижение уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП), зависит от уровня СС-риска и диапазона значений ХС-ЛПНП. Клинические рекомендации предписывают применение медикаментозной терапии для коррекции дислипидемии средними или высокими дозами статинов. При недостижении целевых значений ХС-ЛПНП показана терапия второй линии, в которой к высокодозным статинам добавляется эзетимиб, а при дальнейшем недостижении липидных целей – ингибиторы пропротеиновой конвертазы субтилизин-кексинового типа 9 (англ. рroprotein convertase subtilisin/kexin type 9, PCSK9): алирокумаб, эволокумаб или инклисиран [3].
Несмотря на то что медикаментозные методы гиполипидемической терапии доказали свою эффективность и широко применяются в мире как для первичной, так и для вторичной профилактики СС-событий, в РФ охват пациентов (даже с СС-заболеваниями, обусловленными атеросклерозом, в анамнезе) данными лекарственными препаратами (ЛП) все еще остается невысоким [4–6]. К тому же больные, которые получают гиполипидемические ЛП, часто не достигают целевых значений ХС-ЛПНП вследствие недостаточной интенсивности назначенной терапии или низкой приверженности [4].
Цель – оценка клинико-экономической целесообразности расширения программы льготного лекарственного обеспечения (ЛЛО) взрослых пациентов очень высокого СС-риска, включая не достигших липидных целей на терапии статинами, за счет увеличения частоты использования ЛП эзетимиб, алирокумаб, эволокумаб и инклисиран, применяемых в комбинации со статинами, по сравнению с текущей практикой ЛЛО (использование аторвастатина, симвастатина и минимальное применение других препаратов).
МАТЕРИАЛ И МЕТОДЫ / MATERIAL AND METHODS
С целью разработки клинико-экономической модели был проведен собственный систематический обзор для поиска исследований об эффективности рассматриваемых ЛП в моделируемой группе пациентов.
Варианты терапии / Therapy options
Модель предполагает сравнение комбинаций ЛП внутри рассматриваемой когорты пациентов до расширения программы ЛЛО и при увеличении финансирования всех рассматриваемых ЛП в рамках программы ЛЛО [7]. Возможно назначение следующих вариантов терапии:
- отсутствие терапии (нелекарственная терапия);
- статины в средней дозировке;
- статины в высокой дозировке;
- статины в высокой дозировке в комбинации с эзетимибом;
- статины в высокой дозировке в комбинации с алирокумабом;
- статины в высокой дозировке в комбинации с эволокумабом;
- статины в высокой дозировке в комбинации с инклисираном;
- статины в высокой дозировке в комбинации с эзетимибом и алирокумабом;
- статины в высокой дозировке в комбинации с эзетимибом и эволокумабом;
- статины в высокой дозировке в комбинации с эзетимибом и инклисираном.
Сценарии льготного лекарственного обеспечения / Preferential drug provision scenarios
От наполнения и уровня назначения ЛП в рамках ЛЛО зависит приверженность пациентов назначенной терапии, в то время как последняя напрямую влияет на вероятность достижения липидных целей и, соответственно, на переход пациентов на следующую линию терапии. Таким образом, возможность назначений высокоэффективной терапии влияет на СС-исходы как напрямую (ввиду более высокой эффективности данного вида терапии), так и опосредованно (путем повышения приверженности пациентов).
В рамках настоящего исследования был использован анализ «затраты–эффективность» и «затраты–полезность», который выполнялся с позиции системы здравоохранения РФ. В ходе анализа проведено сравнение различных сценариев назначения липидснижающей терапии в рамках программы ЛЛО с учетом приверженности пациентов назначенной терапии.
Текущий сценарий (сценарий А)
ЛЛО предполагает назначение статинов (в средних и высоких дозировках) или статинов в высокой дозировке в комбинации с эзетимибом. Ингибиторы PCSK9 доступны пациентам на текущем уровне назначения, рассчитанном как 3% от всех пациентов, не достигших липидных целей на терапии статинами или статинами в комбинации с эзетимибом. Данный сценарий является референтным для сравнения с другими моделируемыми сценариями.
Базовое расширение ЛЛО (сценарий Б)
Расширенное ЛЛО позволяет снизить долю пациентов, не достигших липидных целей на терапии статинами, которым не назначили ЛП группы ингибиторов PCSK9, инклисиран и эзетимиб, в 2, 2 и 1,5 раза соответственно. При этом предполагалось, что при внедрении расширенного ЛЛО приверженность пациентов терапии возрастает.
Максимальное назначение ЛП группы ингибиторов PSCK9 (сценарий В)
Расширенное ЛЛО предполагает назначение ингибиторов PCSK9 или инклисирана всем пациентам, которые не достигли целевых липидных показателей на статинах. Аналогично предыдущему сценарию предполагалось, что при внедрении расширенного ЛЛО приверженность пациентов терапии возрастает.
Максимальный прием всей терапии (сценарий Г)
Расширенное ЛЛО предполагает назначение всем пациентам всех видов липидснижающей терапии, требуемых в соответствии с клиническими рекомендациями (отсутствие нелекарственной терапии), при этом интенсивность назначаемой липидснижающией терапии определяется достигнутыми уровнями ХС-ЛПНП. Пациенты демонстрируют 100% приверженность к любой назначенной терапии [3].
Следует отметить, что применение ингибиторов PSCK9 и инклисирана в сценариях В и Г моделирования рассматривалось как терапия второй линии согласно клиническим рекомендациям [3] и инструкциям по медицинскому применению ингибиторов PCSK9 [8].
Описание математической модели / Mathematical model description
В рамках клинико-экономического исследования была разработана модель Маркова для оценки затратной эффективности расширения программы ЛЛО в соответствии с моделируемыми сценариями у взрослых пациентов очень высокого СС-риска (рис. 1). Разработанная модель структурно схожа с опубликованными зарубежными моделями течения атеросклеротической болезни [9–11]. Цикл модели равнялся 1 году. Горизонт моделирования составил 30 лет. Размер моделируемой когорты – 1000 человек.

Рисунок 1. Структура модели Маркова
Figure 1. Markov model structure
Модель включала семь состояний здоровья:
- живые пациенты высокого СС-риска без острых СС-событий;
- инфаркт миокарда (ИМ);
- ишемический инсульт (ИИ);
- постинфарктное состояние (пост-ИМ);
- постишемический инсульт (пост-ИИ);
- сердечно-сосудистая смерть (СС-смерть);
- смерть по другим причинам.
На начало моделирования все пациенты находились в состоянии «живые пациенты без острых СС-событий». Кроме того, в модель были включены два вида событий, которые могли случиться с живыми пациентами в любой цикл модели вне зависимости от их текущего состояния здоровья: реваскуляризация и нестабильная стенокардия (НС).
Модель прогнозировала развитие СС-событий (частота ИМ, ИИ, коронарной реваскуляризации, СС-смерти, НС, а также комбинированных СС-исходов) и общих исходов (добавленные годы жизни (англ. life years gained, LYG), годы жизни с поправкой на качество (англ. quality-adjusted life years, QALY)) в когорте пациентов. Вероятность развития исходов зависела от наблюдаемого в экспериментальных исследованиях снижения показателя ХС-ЛПНП на рассматриваемых видах терапии.
Для проверки устойчивости модели проведен однофакторный анализ чувствительности к показателям полезности состояний здоровья, а также к стоимости изучаемых ЛП.
Вероятности наступления сердечно-сосудистых событий / Probabilities of cardiovascular events occurrence
Вероятности наступления нефатальных ИМ и ИИ, а также СС-смерти были рассчитаны на основании модели REACH, которая позволяет спрогнозировать 20-месячный риск наступления СС-событий на основании характеристик пациентов [12]. При этом в литературе указано, что модель REACH систематически занижает прогноз по наступлению СС-событий [10][13], поэтому ее предсказания были скорректированы на фактор – частное предсказанного и наблюдаемого количеств исходов в популяции, на основании которой модель была построена [12].
Значения характеристик пациентов, использованные для моделирования российской популяции, были получены из четырех источников: российских исследований PROFILE (регистр ННИЦПМ) [14], АЙСБЕРГ [6], DYSIS [15] и Регион ИМ (предварительные данные из регистра острого инфаркта миокарда были предоставлены компанией-производителем). Доли отдельных СС-событий в комбинированном исходе были извлечены из исследования регистра M. Lindh et al. (2019 г.) [16], при этом эти доли специфичны для каждого из состояний. Каждый год средний возраст и половой состав моделируемой популяции менялись, поэтому в модели используются динамические вероятности переходов. Базовые характеристики моделируемой популяции представлены в таблице 1.
Таблица 1. Базовые характеристики моделируемой популяции
Table 1. Baseline characteristics of the populations modelled
|
Параметр / Parameter |
Значение / Value |
Источник / Source |
|
Мужской пол, % / Male gender, % |
69,5 |
Регион-ИМ* / Region-MI* |
|
Возраст, лет / Age, years |
63,1 |
Регион-ИМ* / Region-MI* |
|
Курение, % / Smoking, % |
38,9 |
Регион-MI* / Region-MI* |
|
Диабет, % / Diabetes, % |
29,3 |
[6] |
|
ИМТ меньше, чем 20 кг/м2 / BMI less than 20 kg/m2 |
0 |
[14] |
|
Число пораженных кровеносных русел, % / Number of affected bloodstreams, % |
[12] |
|
|
одно / one |
80,8 |
|
|
два / two |
17,2 |
|
|
три / three |
1,8 |
|
|
ИМ или ИИ за последний год / MI or IS in the last year |
1 – для острых состояний; 0 – для остальных / 1 – for acute conditions; 0 – for the rest |
– |
|
Хроническая сердечная недостаточность, % / Chronic heart failure, % |
24,1 |
Регион-ИМ* / Region-MI* |
|
Фибрилляция предсердий, % / Atrial fibrillation, % |
11,7 |
[12] |
|
Применение ацетилсалициловой кислоты, % / Acetylsalicylic acid use, % |
71,5 |
[12] |
|
Проживание в Восточной Европе или Средней Азии, % / Residence in Eastern Europe or Central Asia, % |
100 (российская популяция) / 100 (Russian population) |
– |
Примечание. ИМТ – индекс массы тела; ИМ – инфаркт миокарда; ИИ – ишемический инсульт. * Предварительные данные из регистра острого инфаркта миокарда Регион ИМ были предоставлены компанией-производителем.
Note. BMI – body mass index; MI – myocardial infarction; IS – ischemic stroke. * Preliminary data from the Region-MI acute myocardial infarction registry were provided by the manufacturing company.
Вероятность смерти по другим причинам была принята равной вероятности смерти по причинам, не связанным с CC-заболеваниями, в общей популяции населения РФ и рассчитана самостоятельно на основании отечественных данных [17]. Данные смерти включали все, кроме закодированных под номерами 121–155 российской номенклатуры причин смерти [18] (коды Международной классификации болезней I00–I99). Вероятность смерти по другим причинам также зависела от возраста и полового состава пациентов. Вероятности необходимости проведения реваскуляризации, а также наступления НС были извлечены из исследования регистра M. Lindh et al. (2019 г.) [16]. Данные вероятности были статичными на всем горизонте моделирования.
Следует отметить, что все математические действия с вероятностями переходов проводились по методике, описанной в публикации R. Fleurence и С. Hollenbeak (2007 г.) [19]. Все вероятности были пересчитаны на период в 1 год, соответствующий длительности цикла модели.
Назначение терапии и приверженность пациентов / Therapy appointment and patient compliance
При первичном посещении врача пациенту могла быть как назначена, так и не назначена лекарственная терапия. Доли пациентов, которым при первом визите к врачу не назначается лекарственная терапия, принимают значения соответствующих показателей из исследований АЙСБЕРГ [6] или РЕКВАЗА [5] (с возможностью выбора). Применяемая лекарственная терапия предполагала назначение: статинов в средней дозировке, статинов в высокой дозировке, статинов в высокой дозировке в комбинации с эзетимибом. Соотношение назначений статинов в средней и высокой дозировке получено из исследования EUROASPIRE IV для российской популяции [4]. Доля пациентов, получающих эзетимиб в комбинации со статинами, среди получающих статины в высоких дозах рассчитана на основании исследования N. Danchin et al. (2018 г.) [20].
В модели учитывалась приверженность терапии статинами на 1 год, которая была рассчитана на основании исследования I. Lin et al. (2016 г.) [21] и составляла 54% для статинов в средних дозах и 61,3% для статинов в высоких дозах, а также приверженность терапии ингибиторами PCSK9 и инклисираном. В базовом варианте делалось допущение, что приверженность данным опциям терапии составляет 80% и 95% соответственно. Часть пациентов, не достигших целевых показателей, начинала получать терапию ингибиторами PSCK9 и инклисираном, часть – продолжала принимать статины или статины в комбинации с эзетимибом. Установленная терапия повторно корректировалась на показатель приверженности: для статинов – на показатель приверженности, рассчитанный на основании кривой приверженности [21], для других видов терапии – на показатели приверженности терапии ингибиторами PCSK9 и инклисираном, устанавливаемые при моделировании самостоятельно.
Параметр достижения пациентами целевых показателей через 1 год после начала лечения учитывал только приверженных, при этом доли пациентов, не достигших целевых липидных показателей через 1 год лечения, были рассчитаны на основании результатов исследования DA VINCI, специфичных для популяции очень высокого СС-риска [22].
Таким образом, когорта пациентов, не получавших лечения, включала тех, которым при первом визите к врачу не назначается лекарственная терапия, а также тех, которые прекратили прием ЛП из-за низкой приверженности лечению. В когорту пациентов, принимающих любой вид лекарственной терапии, вошли продолжившие принимать все назначенные ЛП после 1 года лечения.
Критерии эффективности терапии / Criteria for therapy effectiveness
Модель воспроизводит влияние ЛП на конечные исходы (кроме смерти от прочих, не СС-причин) пациентов посредством влияния на унифицированный суррогатный исход (изменение ХС-ЛПНП). Начальные значения ХС-ЛПНП без лечения извлечены из литературы для популяции РФ [14], остальные начальные значения ХС-ЛПНП рассчитаны с учетом процента снижения показателя на рассматриваемой терапии. Абсолютные значения ХС-ЛПНП, а также процентные показатели снижения уровня ХС-ЛПНП при назначении различных ЛП по отношению к предыдущей линии терапии представлены в таблице 2 и на рисунке 2.
Таблица 2. Уровни холестерина липопротеинов низкой плотности (ХС-ЛПНП) и размер их снижения на различных вариантах гиполипидемической терапии
Table 2. Low density lipoprotein сholesterol (LDL-C) levels and their percentage change following different hypolipidemic therapy options
|
Вариант терапии / Therapy option |
Уровень ХС-ЛПНП, ммоль/л // LDL-C level, mmol/L |
Снижение*, % / Decrease*, % |
Источник / Source |
|
Нет лечения / No treatment |
3,89 |
– |
[14] |
|
Статины (средние дозы) / Statins (medium dose) |
2,77 |
–28,92 |
[23] |
|
Статины (высокие дозы) / Statins (high dose) |
2,21 |
–20,24 |
[23] |
|
Статины (высокие дозы) + эзетимиб / Statins (high dose) + ezetimibe |
1,90 |
–14,00 |
[24] |
|
Статины (высокие дозы) + алирокумаб / Statins (high dose) + alirocumab |
1,07 |
–51,29 |
[25] |
|
Статины (высокие дозы) + эволокумаб / Statins (high dose) + evolocumab |
1,02 |
–53,99 |
[25] |
|
Статины (высокие дозы) + инклисиран / Statins (high dose) + inclisiran |
1,09 |
–50,70 |
[26] |
|
Статины (высокие дозы) + эзетимиб + алирокумаб / Statins (high dose) + ezetimibe + alirocumab |
0,92 |
–51,29 |
[25] |
|
Статины (высокие дозы) + эзетимиб + эволокумаб / Statins (high dose) + ezetimibe + evolocumab |
0,87 |
–53,99 |
[25] |
|
Статины (высокие дозы) + эзетимиб + инклисиран / Statins (high dose) + ezetimibe + inclisiran |
0,94 |
–50,70 |
[26] |
Примечание. * Расчет снижения показателя ХС-ЛПНП как разницы средних значений ХС-ЛПНП рассматриваемой терапии по отношению к предшествующей терапии.
Note. * Calculation of LDL-C decrease as the difference of mean values of LDL-C of the considered therapy in relation to the previous therapy.
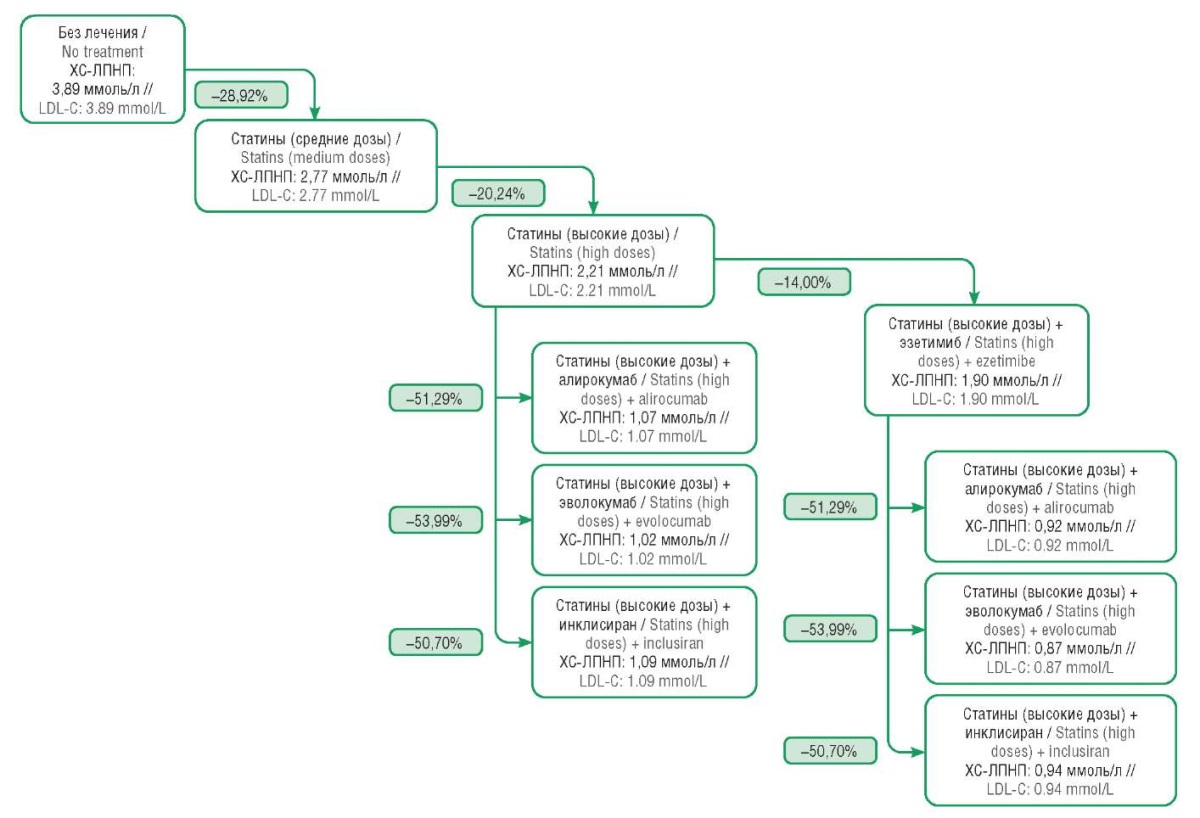
Рисунок 2. Эффективность назначаемой терапии в отношении снижения уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП) и среднего уровня ХС-ЛПНП в подгруппах пациентов в зависимости от назначенной терапии. Значения в процентах отражают размер падения ХС-ЛПНП на рассматриваемой терапии, абсолютные значения указывают на средний уровень ХС-ЛПНП в подгруппе пациентов, принимающих рассматриваемую опцию терапии
Figure 2. Effectiveness of prescribed therapy on the reduction in low-density lipoprotein cholesterol (LDL-C) and mean LDL-C levels in patient subgroups depending on prescribed therapy. Values in percent reflect the size of the drop in LDL-C on the considered therapy, absolute values indicate the average level of LDL-C in the subgroup of patients receiving the considered therapy
Влияние всех рассматриваемых вариантов терапии на конечные исходы отражено в виде изменения риска при падении ХС-ЛПНП на 1 ммоль/л (табл. 3) [23]. Следует отметить, что данный подход выбран для унификации эффектов моделируемых вариантов терапии, при этом значительных различий между рассчитанными и опубликованными показателями не выявлено.
Таблица 3. Отношения рисков наступления сердечно-сосудистых событий при снижении уровня холестерина липопротеинов низкой плотности на 1 ммоль/л
Table 3. Risk ratios of cardiovascular events per 1 mmol/L decrease in low density lipoprotein сholesterol level
|
СС-событие / CV event |
Отношение рисков / Risk ratio |
Источник / Source |
||
|
Статины в средних дозах / Medium dose statins |
Статины в высоких дозах / High dose statins |
Прочие виды терапии / Other types of therapy |
||
|
Нефатальный ИМ / Nonfatal MI |
0,74 |
0,71 |
0,80 |
[23] |
|
Нефатальный ИИ / Nonfatal IS |
0,80 |
0,69 |
0,71 |
[23] |
|
СС-смерть / CV death |
0,86 |
0,86 |
0,69* |
[23] |
|
Реваскуляризация / Revascularization |
0,76 |
0,66 |
0,86 |
[23] |
|
Нестабильная стенокардия / Unstable angina pectoris |
0,80 |
0,80 |
0,66 |
[27] |
Примечание. СС – сердечно-сосудистое; ИМ – инфаркт миокарда; ИИ – ишемический инсульт; СС-смерть – смерть ввиду сердечно-сосудистых причин.
* Показатель рассчитан на основании данных [23].
Note. CV – cardiovascular; MI – myocardial infarction; IS – ischemic stroke; CV-death – death due to cardiovascular causes. * The indicator is calculated based on the [23] data.
Комбинации способов терапии в моделируемых сценариях зависели от приверженности пациентов [4], достижения ими целевых липидных показателей [15], а также доступности ингибиторов PCSK9 в условиях отсутствия финансирования гиполипидемической терапии в амбулаторных условиях за счет средств бюджета. Более того, сценарии А, Б и В включали пациентов, не получавших лечения, в числе которых были как изначально не получавшие лечения после выписки, так и прекратившие терапию из-за низкой приверженности.
Доступность ингибиторов PCSK9 в условиях отсутствия финансирования гиполипидемической терапии (сценарий А) рассчитана на основании данных о среднемесячной реализации ингибиторов PCSK9 и высокоинтенсивных доз статинов по г. Москве и составила 3%. В остальных сценариях предполагалось, что финансирование гиполипидемической терапии за счет средств бюджета сократит число больных, прекращающих лечение [28], а также позволит части пациентов, которые не достигают липидных целей на терапии статинами, получать ингибиторы PCSK9 и инклисиран.
Исходы / Outcomes
Показатели полезности в каждом состоянии извлечены из литературного источника R. Ara et al. (2008 г.) [29], при этом дополнительно показатели полезности качества жизни (КЖ) были скорректированы на фактор убывания в соответствии с возрастом – согласно тренду, выявленному в исследовании P. Kind et al. (1998 г.) [30].
В связи с тем, что реваскуляризация является одним из методов лечения ишемической болезни сердца, полезность состояния «пост-реваскуляризация» была принята равной полезности состояния «стабильная стенокардия во второй и последующие годы» в исследовании R. Ara et al. (2008 г.) [29]. Данный показатель выбран для минимизации влияния острого состояния стабильной стенокардии в первый год наблюдения.
Показатели полезности КЖ при наступлении НС также скорректированы на фактор отношения полезности КЖ на первом году наблюдения у пациентов с НС к показателю полезности состояния «стабильная стенокардия во второй и последующие годы». Данный фактор составил 86% – таким образом, КЖ снижалось на 14% при развитии НС. Показатели полезности КЖ представлены в таблице 4.
Таблица 4. Показатели полезности качества жизни в различных состояниях модели [29]
Table 4. Health-related utility values in various health states of the model [29]
|
Состояние модели / Health state of the model |
Показатель / Utility value |
|
Высокий риск СС-событий / High risk of CV event |
0,90 |
|
Инфаркт миокарда / Myocardial infarction |
0,76 |
|
Постинфаркт миокарда / Post myocardial infarction |
0,80 |
|
Ишемический инсульт / Ischemic stroke |
0,63 |
|
Постишемический инсульт / Post ischemic stroke |
0,63 |
Примечание. СС – сердечно-сосудистое.
Note. CV – cardiovascular.
Затраты / Costs
При моделировании учитывались прямые медицинские затраты, которые рассчитаны с позиции системы здравоохранения РФ. Затраты на лекарственную терапию определены в соответствии с режимами дозирования ЛП, представленными в инструкциях по медицинскому применению в РФ [8] и медианой стоимости 1 мг действующего вещества.
Цены на ЛП, включенные в перечень жизненно необходимых и важнейших лекарственных препаратов (аторвастатин, симвастатин, алирокумаб, эволокумаб), учтены согласно зарегистрированным предельным отпускным ценам в РФ с учетом налога на добавленную стоимость (НДС) 10% [31]. Цены эзетимиба и инклисирана определены на основании данных государственных закупок за 2022 г. с учетом НДС 10% [32].
Для расчета стоимости статинов в средних дозировках использовались доли пациентов, получающих аторвастатин и симвастатин (50% и 50%). В расчете стоимости терапии высокими дозами статинов учитывался только аторвастатин для всей когорты согласно клиническим рекомендациям [3]. Информация о режиме дозирования и рассчитанной стоимости лекарственной терапии в год на 1 пациента представлена в таблице 5.
Таблица 5. Дозировки и стоимость применения рассматриваемых препаратов в год на 1 пациента
Table 5. Dosage and yearly costs for drugs modelled per 1 patient
|
МНН / INN |
Дозировка / Dose |
Стоимость, руб. / Cost, rub. |
|
Аторвастатин (средние дозы) / Atorvastatin (medium dose) |
40 мг ежедневно / 40 mg daily |
7106 |
|
Аторвастатин (высокие дозы) / Atorvastatin (high dose) |
80 мг ежедневно / 80 mg daily |
14 212 |
|
Симвастатин (средние дозы) / Simvastatin (medium dose) |
40 мг ежедневно / 40 mg daily |
4792 |
|
Эзетимиб / Ezetimibe |
10 мг ежедневно / 10 mg daily |
7891 |
|
Эволокумаб / Evolocumab |
280 мг 1 раз в 2 нед / 280 mg once every 2 weeks |
317 326 |
|
Алирокумаб, 1-й год / Alirocumab, Year 1 |
264,1 мг в месяц* / 264.1 mg per month* |
463 654 |
|
Алирокумаб, 2+ год / Alirocumab, Year 2+ |
246,15 мг в месяц* / 246.15 mg per month* |
432 141 |
|
Инклисиран, 1-й год / Inclisiran, Year 1 |
3 введения (852 мг) в год / 3 doses (852 mg) per year |
330 000 |
|
Инклисиран, 2+ год / Inclisiran, Year 2+ |
2 введения (568 мг) в год / 2 doses (568 mg) per year |
220 000 |
Примечание. МНН – международное непатентованное наименование. *Алирокумаб назначается в дозе 75 мг 1 раз в 2 нед, 150 мг 1 раз в 2 нед или 300 мг 1 раз в 4 нед.
Для определения долей пациентов, принимающих различные режимы дозирования было использовано исследование J. Jukema et al. (2019 г.): первые 4 мес пациенты принимают дозу 300 мг 1 раз в 4 нед, далее после 4-го месяца терапии 35,9% принимают сниженную дозу [33].
Note. INN – International nonproprietary name. * Alirocumab is prescribed at a dose of 75 mg once every 2 weeks, 150 mg once every 2 weeks, or 300 mg once every 4 weeks.
A study by J. Jukema et al. (2019) was used to determine the proportion of patients taking different dosing regimens: patients take a dose of 300 mg once every 4 weeks for the first 4 months, followed by 35.9% taking a reduced dose after the 4th month of therapy [33].
В модели учитывались посещения пациентами амбулаторных специалистов для контроля заболеваний, которые рассчитаны как произведения среднего норматива финансовых затрат на 1 посещение при оказании медицинской помощи в амбулаторных условиях за счет средств обязательного медицинского страхования (ОМС) в соответствии с Программой государственных гарантий бесплатного оказания гражданам медицинской помощи на 2022 г. (ПГГ-2022) [34] (329 руб.) и относительных коэффициентов стоимости посещения с учетом специальности различных врачей [35].
Для расчета объема амбулаторных посещений использованы усредненные показатели частоты предоставления и кратности посещения специалистов, извлеченные из стандартов оказания медицинской помощи. При отсутствии стандартов для рассматриваемых состояний здоровья был сделан ряд допущений о релевантности данных из прочих опубликованных стандартов медицинской помощи по СС-профилю [36–38]. Суммарная стоимость амбулаторных посещений равнялась сумме стоимости посещений всех специалистов для рассматриваемого состояния в модели. Результат расчетов стоимости амбулаторных посещений отражены в таблице 6.
Таблица 6. Стоимость амбулаторных посещений за год
Table 6. Cost of primary care visits per year
|
Состояние модели / Health state of the model |
Стоимость, руб. / Cost, rub. |
Источник / Source |
|
Постреваскуляризация / Postrevascularization |
3920 |
[38] |
|
ИМ и пост-ИМ / MI and post-IM |
3574 |
[36–38] |
|
ИИ и пост-ИИ / IS and post-IS |
4242 |
[36–38] |
Примечание. ИМ – инфаркт миокарда; ИИ – ишемический инсульт.
Note. MI – myocardial infarction; IS – ischemic stroke.
Стоимость стационарных услуг рассчитана в соответствии с ПГГ-2022 с учетом средних нормативов финансовых затрат на законченный случай лечения пациента в условиях круглосуточного стационара за счет средств ОМС (39 385 руб.) [34]. Минимальная базовая ставка определена как 65% от норматива стоимости 1 случая лечения в условиях круглосуточного стационара, что составило 25 600,25 руб. [39]. К рассчитанному тарифу стационара применялись коэффициенты затратоемкости для каждой причины госпитализации. При наличии в перечне коэффициентов затратоемкости нескольких подуровней рассматриваемой группы для расчета стоимости госпитализации использовалось среднее значение между всеми представленными подуровнями.
Кроме того, учитывался норматив стоимости вызова скорой помощи для каждой госпитализации: средний норматив согласно ПГГ-2022 составляет 2884,70 руб. [34]. Предполагалось, что в стоимость госпитализации пациентов, которым требуется реваскуляризация, входит процедура коронарографии. Доли пациентов, получающих разные виды реваскуляризации, рассчитаны исходя из отечественных статистических данных [40]: стентирование было проведено 87% пациентов, шунтирование – 13%.
Помимо госпитализаций ввиду неотложных состояний для всех пациентов учтены затраты на медицинскую реабилитацию после острых СС-событий. Результаты расчетов стоимости госпитализаций по причине СС-событий представлены в таблице 7.
Таблица 7. Стоимость госпитализаций по причине сердечно-сосудистых событий [39]
Table 7. Costs of hospitalizations for cardiovascular events [39]
|
Причина госпитализации / Reason for hospitalization |
Код КСГ / DRG code |
Наименование КСГ / Name of DRG |
КЗ / CIR |
Стоимость госпитализации, руб. / Cost of hospitalization, rub. |
|
Инфаркт миокарда / Myocardial infarction |
st13.008 |
Инфаркт миокарда, легочная эмболия, лечение с применением тромболитической терапии (уровень 1) / Myocardial infarction, pulmonary embolism, treatment with thrombolytic therapy (Level 1) |
1,61 |
72 346,71 |
|
st13.009 |
Инфаркт миокарда, легочная эмболия, лечение с применением тромболитической терапии (уровень 2) / Myocardial infarction, pulmonary embolism, treatment with thrombolytic therapy (level 2) |
2,99 |
||
|
st13.010 |
Инфаркт миокарда, легочная эмболия, лечение с применением тромболитической терапии (уровень 3) / Myocardial infarction, pulmonary embolism, treatment with thrombolytic therapy (Level 3) |
3,54 |
||
|
Ишемический инсульт / Ischemic stroke |
st15.014 |
Инфаркт мозга (уровень 1) / Cerebral infarction (Level 1) |
2,52 |
89 498,88 |
|
st15.015 |
Инфаркт мозга (уровень 2) / Cerebral infarction (Level 2) |
3,12 |
||
|
st15.016 |
Инфаркт мозга (уровень 3) / Cerebral infarction (Level 3) |
4,51 |
||
|
Нестабильная стенокардия / Unstable angina pectoris |
st13.001 |
Нестабильная стенокардия, инфаркт миокарда, легочная эмболия (уровень 1) ) / Unstable angina pectoris, myocardial infarction, pulmonary embolism (Level 1) |
1,42 |
57 029,23 |
|
st13.002 |
Нестабильная стенокардия, инфаркт миокарда, легочная эмболия (уровень 2) ) / Unstable angina pectoris, myocardial infarction, pulmonary embolism (Level 2) |
2,81 |
||
|
Аортокоронарное шунтирование / Coronary artery bypass grafting |
st25.007 |
Операции на сердце и коронарных сосудах (уровень 3) / Cardiac and coronary surgeries (Level 3) |
4,31 |
113 221,78 |
|
Ангиопластика коронарных артерий со стентированием / Coronary angioplasty with stenting |
st25.007 |
Операции на сердце и коронарных сосудах (уровень 3) / Cardiac and coronary surgeries (Level 3) |
4,31 |
113 221,78 |
|
Услуги по медицинской реабилитации пациента, перенесшего острый инфаркт миокарда / Medical rehabilitation of a patient who had an acute myocardial infarction |
st37.008 |
Медицинская кардиореабилитация (3 балла по ШРМ) / Medical cardiac rehabilitation (RRS Score 3) |
1,02 |
37 547,03 |
|
st37.009 |
Медицинская кардиореабилитация (4 балла по ШРМ) / Medical cardiac rehabilitation (RRS Score 4) |
1,38 |
||
|
st37.010 |
Медицинская кардиореабилитация (5 баллов по ШРМ) / Medical cardiac rehabilitation (RRS Score 5) |
2,00 |
||
|
Услуги по медицинской реабилитации пациента, перенесшего острое нарушение мозгового кровообращения / Medical rehabilitation of the patient, who had an acute impairment of cerebral circulation |
st37.001 |
Медицинская реабилитация пациентов с заболеваниями центральной нервной системы (3 балла по ШРМ) / Medical rehabilitation of patients with central nervous system diseases (RRS Score 3) |
1,53 |
99 264,97 |
|
st37.002 |
Медицинская реабилитация пациентов с заболеваниями центральной нервной системы (4 балла по ШРМ) / Medical rehabilitation of patients with central nervous system diseases (RRS Score 4) |
2,04 |
||
|
st37.003 |
Медицинская реабилитация пациентов с заболеваниями центральной нервной системы (5 баллов по ШРМ) / Medical rehabilitation of patients with central nervous system diseases (RRS Score 5) |
3,34 |
||
|
st37.004 |
Медицинская реабилитация пациентов с заболеваниями центральной нервной системы (6 баллов по ШРМ) / Medical rehabilitation of patients with central nervous system diseases (RRS Score 6) |
8,60 |
Примечание. КСГ – клинико-статистическая группа, КЗ – коэффициент затратоемкости; ШРМ – шкала реабилитационной маршрутизации.
Note. CRC – clinical and statistical group, CIR – cost-intensity ratio, RRS – Rehabilitation Routing Scale.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ / RESULTS AND DISCUSSION
Распределение пациентов / Patient distribution
В ходе моделирования проанализировано распределение пациентов по типам получаемой лекарственной терапии в рамках изучаемой когорты 1000 пациентов в течение первого года моделирования (рис. 3). К концу года получившееся распределение приняли как установившееся для дальнейшего моделирования (рис. 4).

Рисунок 3. Распределение пациентов по видам лекарственной терапии в моделируемых сценариях расширения программы льготного лекарственного обеспечения.
ХС-ЛПНП – холестерин липопротеинов низкой плотности; PCSK9 (англ. рroprotein convertase subtilisin/kexin type 9) – пропротеиновая конвертаза субтилизин-кексинового типа 9
Figure 3. Distribution of patients by drug therapy options in modelled scenarios of expansion of drug provision program
LDL-C – low-density lipoprotein cholesterol; PCSK9 – рroprotein convertase subtilisin/kexin type 9

Рисунок 4. Установившееся распределение когорты пациентов по типам схем лекарственных препаратов в моделируемых сценариях
Figure 4. Steady-state distribution of cohort of patients by type of drug regiment in modelled scenarios
Вероятность сердечно-сосудистых событий / Probability of cardiovascular events
Моделирование на 30-летнем горизонте (с учетом дисконтирования) продемонстрировало, что возмещение липидснижающей терапии нового поколения (эволокумаб, алирокумаб, инклисиран и эзетимиб в составе комбинированной терапии со статинами) у пациентов очень высокого СС-риска, не достигших целевых значений по липидам на терапии статинами, позволит значительно снизить вероятность отдельных СС-событий. Расширение ЛЛО приводит к снижению смертности ввиду СС-причин, при этом наблюдается увеличение смертности от прочих причин, т.к. у дополнительного числа выживших (не умерших от СС-причин) пациентов остается риск смерти от прочих причин. Однако совокупный эффект на общую смертность положительный.
Расширение ЛЛО оказывает выраженный эффект на количество случаев комбинированных СС-событий (в пересчете на 1 пациента), а также на показатели продолжительности и качества жизни (рис. 5, табл. 8). Так, при реализации базового сценария расширения ЛЛО (сценарий Б) количество случаев комбинированного СС-события (включающего ИМ, ИИ и СС-смерть) и расширенного комбинированного СС-события (включающего также НС и реваскуляризацию) по отношению к текущей практике в базовом сценарии (сценарий Б) снизилось на 8% и 9% соответственно, в сценарии максимального расширения ЛЛО (сценарий Г) – на 35% и 39% соответственно.
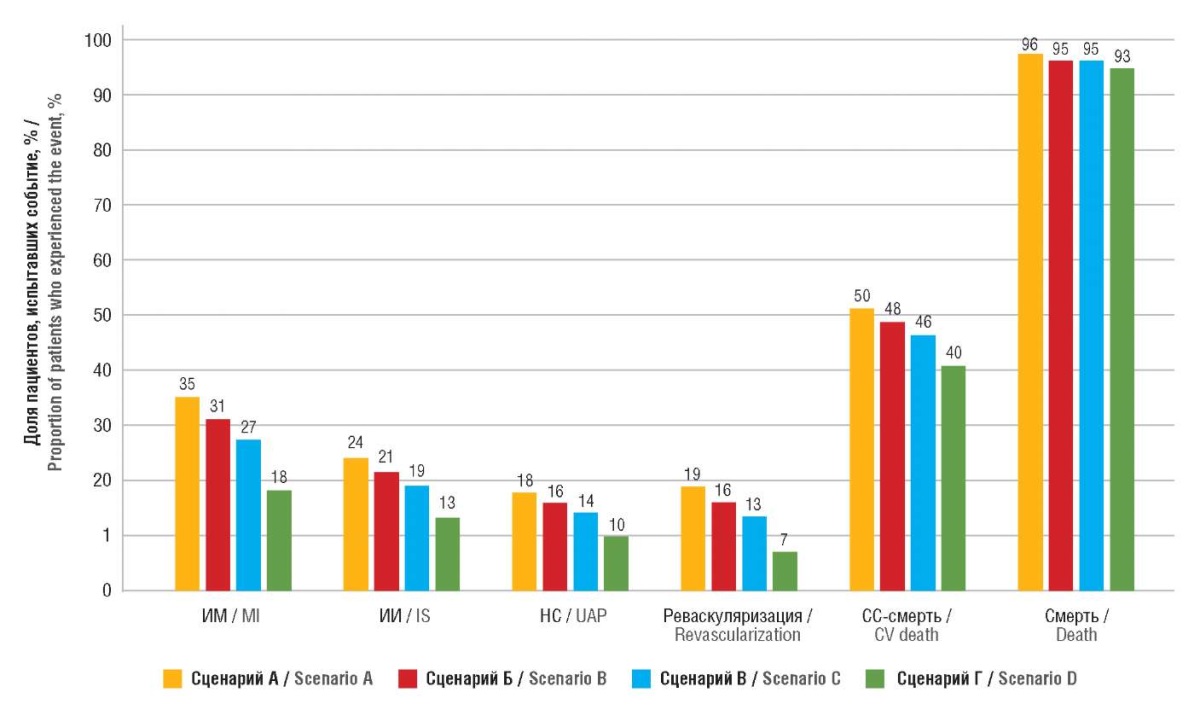
Рисунок 5. Распределение пациентов, испытавших сердечно-сосудистые исходы и смерть в моделируемых сценариях расширения программы льготного лекарственного обеспечения.
ИМ – инфаркт миокарда; ИИ – ишемический инсульт; НС – нестабильная стенокардия; СС-смерть – смерть ввиду сердечно-сосудистых причин
Figure 5. Distribution of patients who experienced cardiovascular events and death in modelled scenarios of expansion of drug provision program.
MI – myocardial infarction; IS – ischemic stroke; UAP – unstable angina pectoris; CV death – death due to cardiovascular causes
Таблица 8. Затраты и исходы на 1 пациента для сценариев расширения программы льготного лекарственного обеспечения за период моделирования 30 лет
Table 8. Costs and impacts per 1 patient for scenarios of expansion of drug provision program for 30 years modelling horizon
|
Параметр / Parameter |
Сценарий / Scenario |
|||
|
А / A |
Б / B |
В / C |
Г / D |
|
|
Затраты на 1 пациента, руб.* / Costs per 1 patient, rub.* |
||||
|
затраты на ЛП / costs of drugs |
38 757 |
716 502 |
1 508 543 |
2 995 015 |
|
затраты на статины / costs for statins |
15 359 |
43 599 |
68 959 |
134 207 |
|
затраты на прочие ЛП / costs of other drugs |
23 398 |
672 902 |
1 439 584 |
2 860 808 |
|
амбулаторные затраты / outpatient costs |
36 055 |
36 733 |
37 369 |
38 893 |
|
стационарные затраты / inpatient costs |
73 260 |
64 581 |
56 434 |
36 926 |
|
всего / total |
148 071 |
817 816 |
1 602 346 |
3 070 833 |
|
Исходы на 1 пациента / Outcomes per 1 patient |
||||
|
серьезные СС-события, n / major CV events, n |
1,09 |
1,00 |
0,91 |
0,71 |
|
расширенные серьезные СС-события, n / extended major CV events, n |
1,45 |
1,31 |
1,19 |
0,88 |
|
продолжительность жизни, лет / life expectancy, years |
13,56 |
13,90 |
14,23 |
15,00 |
|
QALY*, n |
7,90 |
8,08 |
8,26 |
8,68 |
|
ICER*, руб. / ICER*, rub. |
||||
|
за LYG / per LYG |
– |
1 949 393 |
2 180 784 |
2 032 444 |
|
за QALY / per QALY |
– |
3 598 156 |
4 017 636 |
3 749 261 |
Примечание. ЛП – лекарственные препараты; СС – сердечно-сосудистые; LYG (англ. life year gained) – добавленный год жизни; QALY (англ. quality-adjusted life year) – год жизни с поправкой на качество; ICER (англ. incremental cost-effectiveness ratio) – инкрементальный показатель «затраты–эффективность». * Дисконтированные значения.
Note. CV – cardiovascular; LYG – life year gained; QALY – quality-adjusted life year; ICER – incremental cost-effectiveness ratio. * Discounted values.
Максимальный эффект по показателю продолжительности жизни наблюдался в сценарии максимального расширения ЛЛО (сценарий Г). При моделировании данного сценария продолжительность жизни пациентов возрастала на 1,44 года по сравнению с текущей ситуацией (сценарий А), в то время как при реализации базового сценария расширения ЛЛО (сценарий Б) этот показатель увеличивался на 0,34 года. В результате проведенного моделирования эффект составил от 0,19 (сценарий Б) до 0,78 (сценарий Г) дополнительных QALY.
Анализ затрат / Cost analysis
Совокупные затраты на 1 пациента при расширении программы ЛЛО возрастают с каждым последующим сценарием. Таким образом, прирост общих затрат составляет от 669 745 до 2 922 762 руб. на пациента (рис. 6). Прирост затрат в первую очередь обусловлен ростом затрат на инновационные липидснижающие ЛП. При этом сумма амбулаторных затрат показывает незначительный рост (главным образом за счет дополнительных амбулаторных посещений выживших пациентов), а госпитальные затраты сокращаются в 1,13–1,98 раза в моделируемых сценариях. Снижение затрат на госпитализацию обусловлено значительным уменьшением количества острых СС-событий.
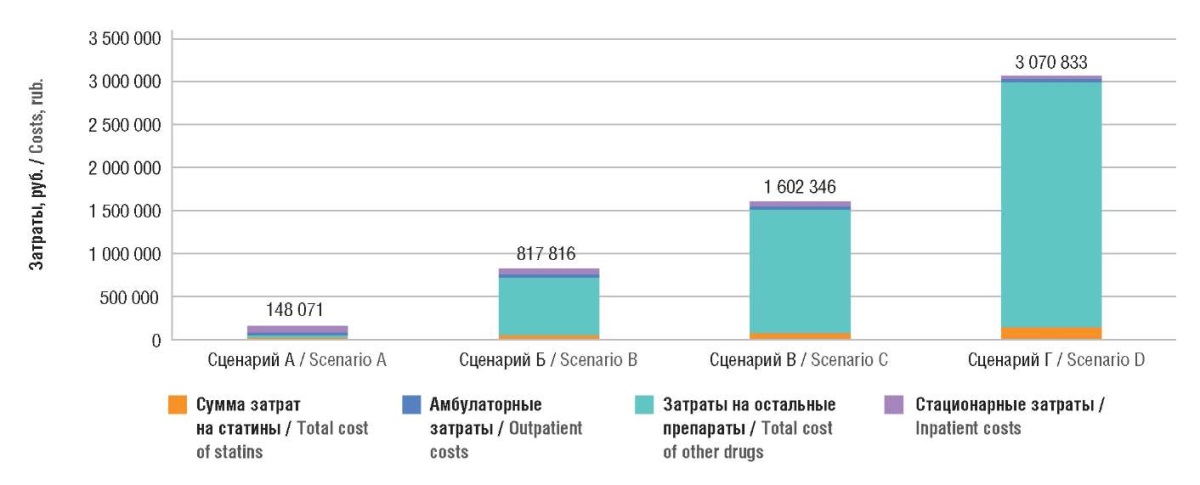
Рисунок 6. Затраты на сценарии расширения программы льготного лекарственного обеспечения
Figure 6. Costs associated with scenarios of expansion of drug provision program
При сопоставлении результатов различных моделируемых сценариев можно сделать вывод об увеличении затрат и эффекта от внедрения ЛЛО в каждом последующем сценарии. Однако рост затрат и эффекта не является пропорциональным, поэтому выбор наиболее затратно-эффективной стратегии должен базироваться на основании инкрементальных показателей «затраты–эффективность» (англ. incremental cost-effectiveness ratio, ICER), рассчитанных как разница затрат по отношению к разнице в эффекте между рассматриваемым сценарием и текущей практикой.
Стоимость дополнительного года жизни (ICER за LYG) варьировала от 1,95 до 2,18 млн руб., в то время как ICER за QALY составил от 3,6 до 4,02 млн руб. Следует отметить, что значения ICER за LYG и за QALY в сценарии В (максимальное назначение инновационных ЛП) превысили значения сценария Г (максимальное назначение всей терапии). Тотальное назначение статинов и своевременный перевод пациентов на инновационную терапию при недостижении липидных целей в начале модели на популяционном уровне помогает отсрочить или исключить необходимость назначения в будущем ингибиторов PCSK9 и инклисирана и дорогостоящей терапии для части пациентов. Более того, тотальная приверженность пациентов позволяет добиться максимально возможного эффекта на уровень ХС-ЛПНП для каждой назначенной линии терапии. Затраты и исходы на 1 пациента для сценариев расширения ЛЛО за период моделирования 30 лет в зависимости от моделируемого сценария представлены в таблице 8.
Вывод о целесообразности расширения программы ЛЛО можно сделать при сопоставлении ICER с порогом готовности платить (ПГП). Значение ПГП в РФ не установлено нормативными правовыми актами, поэтому ПГП рассчитывали самостоятельно на основании методики Всемирной организации здравоохранения как трехкратный размер валового внутреннего продукта (ВВП) на душу населения [41]. В 2022 г. 1 ВВП на душу населения составил 929 495 руб. (135 294 974 583 305 руб. ВВП / 145 557 576 жителей РФ) [42]. Таким образом, ПГП составляет 2 788 485 руб. за единицу эффекта.
Анализ эффективности / Effectiveness analysis
ICER за LYG во всех реализуемых сценариях не превышал значение ПГП, отклонение от ПГП составило от –22 до –30% в зависимости от реализуемого сценария. Можно заключить, что расширение ЛЛО по критерию LYG является затратно-эффективной (экономически эффективной) организационной медицинской технологией в контексте РФ. Однако ICER за QALY превышает рассчитанный ПГП от +29 до +44% в зависимости от сценария. Значимая разница в размере показателя ICER для двух оцениваемых исходов связана со значимым падением КЖ пациентов ввиду естественного старения когорты на длительном горизонте моделирования.
Анализ чувствительности / Sensitivity analysis
Для оценки устойчивости полученных результатов был проведен детерминистический анализ чувствительности. Наибольшее влияние на значение ICER за дополнительный QALY оказывает варьирование показателя КЖ в состоянии «высокий риск СС-событий»: при варьировании показателя на ±20%, значение ICER за QALY изменяется на +54/–26% в базовом сценарии (сценарий Б). Умеренное влияние на ICER за QALY оказывает варьирование показателей КЖ в состоянии «пост-ИМ», а также стоимости алирокумаба, эволокумаба и инклисирана. Варьирование прочих входных данных модели на ±20% оказывает влияние на ICER не более чем на ±5%.
Ограничения исследования / Study limitations
В связи с тем, что в открытом доступе отсутствуют данные, в достаточной мере описывающие течение атеросклеротической болезни, а также характеристики пациентов в РФ, моделирование проводилось методом комбинирования нескольких российских и зарубежных источников. Данные об эффективности применяемой терапии получены из метаанализов, популяция которых была неоднородна и включала как пациентов, уже перенесших СС-событие, так и пациентов с высоким СС-риском. Кроме того, пациенты во включенных исследованиях могли принимать сопутствующую терапию, эффективность и приверженность которой не изучались в данном клинико-экономическом исследовании. Сведения о приверженности пациентов и факторе сокращения неприверженных пациентов при внедрении расширенного ЛЛО получены из зарубежных источников и не учитывают российскую практику назначения гиполипидемической терапии.
Таким образом, реальные пациенты и течение их заболевания в РФ могут не вполне соответствовать таковым в представленной модели, что могло сместить результаты моделирования. Кроме того, расчет затрат на лекарственную терапию основывался на определении стоимости единицы действующего вещества. Для ЛП, имеющих несколько различных дозировок, расчеты выполнены исходя из медианной стоимости единицы действующего вещества по всем использующимся дозировкам. Таким образом, примененный в настоящем исследовании подход к определению стоимости 1 мг действующего вещества может смещать результаты исследования.
Результаты данного исследования следует трактовать с учетом указанных ограничений и допущений.
ЗАКЛЮЧЕНИЕ / CONCLUSION
Клинико-экономическая оценка продемонстрировала, что перевод пациентов высокого СС-риска, не достигших липидных целей на монотерапии статинами, на комбинированную терапию, включающую статины в высоких дозировках совместно с применением эзетимиба, эволокумаба, алирокумаба и инклисирана при реализации программы ЛЛО на горизонте моделирования 30 лет:
- позволяет значительно снизить количество серьезных СС-событий по отношению к текущей практике (на 8–35% для комбинированного СС-события и на 9–39% для расширенного комбинированного СС-события в зависимости от сценария);
- позволяет увеличить продолжительность жизни на 0,34–1,44 года и число QALY на 0,19–0,78 года в зависимости от сценария;
- увеличивает общие затраты в расчете на 1 пациента (разница составила от 670 тыс. руб. до 2,9 млн руб. в зависимости от сценария), при этом обеспечивая экономию затрат в части стационарных услуг;
- является затратно-эффективной (экономически эффективной) организационной технологией по критерию LYG, однако не затратно-эффективной по критерию QALY при текущем расчетном уровне ПГП в РФ;
- полное назначение всей доступной гиполипидемической терапии всем пациентам высокого СС-риска является более затратно-эффективной стратегий расширения ЛЛО по сравнению с тотальным назначением ЛП эволокумаб, алирокумаб и инклисиран.
Список литературы
1. Федеральная служба государственной статистики. Здравоохранение в России. Статистический сборник. М.; 2021. URL: https://rosstat.gov.ru/storage/mediabank/Zdravoohran-2021.pdf (дата обращения 07.02.2023).
2. Barquera S., Pedroza-Tobías A., Medina C., et al. Global overview of the epidemiology of atherosclerotic cardiovascular disease. Arch Med Res. 2015; 46 (5): 328–38. https://doi.org/10.1016/j.arcmed.2015.06.006.
3. Евразийская ассоциация кардиологов, Национальное общество по изучению атеросклероза (НОА). Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. М.; 2020. URL: https://cardio-eur.asia/media/files/clinical_recommendations/Diagnosis_and_correction_of_lipid_metabolism_disorders_for_the_prevention_and_treatment_of_atherosclerosis.pdf (дата обращения 07.02.2023).
4. Reiner Ž., De Backer G., Fras Z., et al. Lipid lowering drug therapy in patients with coronary heart disease from 24 European countries – Findings from the EUROASPIRE IV survey. Atherosclerosis. 2016; 246: 243–50. https://doi.org/10.1016/j.atherosclerosis.2016.01.018.
5. Бойцов С.А., Лукьянов М.М., Якушин С.С. и др. Регистр кардиоваскулярных заболеваний (РЕКВАЗА): диагностика, сочетанная сердечно-сосудистая патология, сопутствующие заболевания и лечение в условиях реальной амбулаторно-поликлинической практики. Кардиоваскулярная терапия и профилактика. 2014; 13 (6): 44–50. https://doi.org/10.15829/1728-8800-2014-6-3-8.
6. Ежов М.В., Близнюк С.А., Алексеева И.А., Выгодин В.А. Распространенность гиперхолестеринемии и применения статинов в амбулаторной практике в Российской Федерации. Исследование АЙСБЕРГ – диагностирование пациентов с гиперхолестеринемией в условиях амбулаторной практики на раннем этапе с целью улучшения. Атеросклероз и дислипидемии. 2017; 4: 5–17.
7. Приказ Минздрава России от 29.09.2022 № 639н «Об утверждении перечня лекарственных препаратов для медицинского применения в целях обеспечения в амбулаторных условиях лиц, находящихся под диспансерным наблюдением, которые перенесли острое нарушение мозгового кровообращения, инфаркт миокарда, а также которым выполнены аортокоронарное шунтирование, ангиопластика коронарных артерий со стентированием и катетерная абляция по поводу сердечно-сосудистых заболеваний, в течение 2 лет с даты постановки диагноза и (или) выполнения хирургического вмешательства». URL: https://www.garant.ru/products/ipo/prime/doc/405467511/ (дата обращения 07.02.2023).
8. Государственный реестр лекарственных средств. URL: https://grls.rosminzdrav.ru/Default.aspx (дата обращения 15.07.2022).
9. Toth P.P., Danese M., Villa G., et al. Estimated burden of cardiovascular disease and value-based price range for evolocumab in a highrisk, secondary-prevention population in the US payer context. J Med Econ. 2017; 20 (6): 555–64. https://doi.org/10.1080/13696998.2017.1284078.
10. Gandra S.R., Villa G., Fonarow G.C., et al. Cost-effectiveness of LDL-C lowering with evolocumab in patients with high cardiovascular risk in the United States. Clin Cardiol. 2016; 39 (6): 313–20. https://doi.org/10.1002/clc.22535.
11. Liang Z., Chen Q., Yang F., et al. Cost-effectiveness of evolocumab therapy for myocardial infarction: the Chinese healthcare perspective. Cardiovasc Drugs Ther. 2021; 35 (4): 775–85. https://doi.org/10.1007/s10557-020-07079-6.
12. Wilson P.W.F., D'Agostino R. Sr., Bhatt D.L., et al. An international model to predict recurrent cardiovascular disease. Am J Med. 2012; 125 (7): 695–703.e1. https://doi.org/10.1016/j.amjmed.2012.01.014.
13. Taylor B., Lothgren M., Villa G., et al. Abstract 18114: Differences between observed and predicted cardiovascular event rates using the Framingham and REACH equations: the case of high-intensity statin users in the United Kingdom. Circulation. 2015; 132 (Suppl. 3): A18114. https://doi.org/10.1161/circ.132.suppl_3.18114.
14. Gaisenok O., Martsevich S., Tripkosh S., Lukina Y. Analysis of lipidlowering therapy and factors affecting regularity of statin intake in patients with cardiovascular disease enrolled in the PROFILE registry. Rev Port Cardiol. 2015; 34 (2): 111–6. https://doi.org/10.1016/j.repc.2014.08.021.
15. Оганов Р.Г., Кухарчук В.В., Арутюнов Г.П. и др. Сохраняющиеся нарушения показателей липидного спектра у пациентов с дислипидемией, получающих статины, в реальной клинической практике в Российской Федерации (Российская часть исследования DYSIS). Кардиоваскулярная терапия и профилактика. 2012; 11 (4): 70–8. https://doi.org/10.15829/1728-8800-2012-4-70-78.
16. Lindh M., Banefelt J., Fox K.M., et al. Cardiovascular event rates in a high atherosclerotic cardiovascular disease risk population: estimates from Swedish population-based register data. Eur Heart J Qual Care Clin Outcomes. 2019; 5 (3): 225–32. https://doi.org/10.1093/ehjqcco/qcy058.
17. Центр демографических исследований Российской экономической школы. Данные. URL: http://demogr.nes.ru/ (дата обращения 07.02.2023).
18. Краткая российская номенклатура причин смерти, основанная на ICD10. URL: http://demogr.nes.ru/images/uploads/Приложение%204_190814.pdf (дата обращения 07.02.2023).
19. Fleurence R.L., Hollenbeak C.S. Rates and probabilities in economic modelling: transformation, translation and appropriate application. Pharmacoeconomics. 2007; 25 (1): 3–6. https://doi.org/10.2165/00019053-200725010-00002.
20. Danchin N., Almahmeed W., Al-Rasadi K., et al. Achievement of low-density lipoprotein cholesterol goals in 18 countries outside Western Europe: The International ChoLesterol management Practice Study (ICLPS). Eur J Prev Cardiol. 2018; 25 (10): 1087–94. https://doi.org/10.1177/2047487318777079.
21. Lin I., Sung J., Sanchez R.J., et al. Patterns of statin use in a realworld population of patients at high cardiovascular risk. J Manag Care Spec Pharm. 2016; 22 (6): 685–98. https://doi.org/10.18553/jmcp.2016.22.6.685.
22. Ray K.K., Molemans B., Schoonen W.M., et al. EU-wide crosssectional observational study of lipid-modifying therapy use in secondary and primary care: the DA VINCI study. Eur J Prev Cardiol. 2021; 28 (11): 1279–89. https://doi.org/10.1093/eurjpc/zwaa047.
23. Baigent C., Blackwell L., Emberson J., et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010; 376 (9753) 1670–81. https://doi.org/10.1016/S0140-6736(10)61350-5.
24. Lee J., Egolum U., Parihar H., et al. Effect of ezetimibe added to high-intensity statin therapy on low-density lipoprotein cholesterol levels: a meta-analysis. Cardiol Res. 2021; 12 (2): 98–108. https://doi.org/10.14740/cr1224.
25. Geng Q., Li X., Sun Q., Wang Z. Efficacy and safety of PCSK9 inhibition in cardiovascular disease: a meta-analysis of 45 randomized controlled trials. Cardiol J. 2022; 29 (4): 574–81. https://doi.org/10.5603/CJ.a2021.0110.
26. Wright R.S., Ray K.K., Raal F.J., et al. Pooled patient-level analysis of inclisiran trials in patients with familial hypercholesterolemia or atherosclerosis. J Am Coll Cardiol. 2021; 77 (9): 1182–93. https://doi.org/10.1016/j.jacc.2020.12.058.
27. Briel M., Schwartz G.G., Thompson P.L., et al. Effects of early treatment with statins on short-term clinical outcomes. JAMA. 2006; 295 (17): 2046–56. https://doi.org/10.1001/jama.295.17.2046.
28. Choudhry N.K., Avorn J., Glynn R.J., et al. Full coverage for preventive medications after myocardial infarction. New Engl J Med. 2011; 365 (22): 2088–97. https://doi.org/10.1056/NEJMsa1107913.
29. Ara R., Pandor A., Tumur I., et al. Cost effectiveness of ezetimibe in patients with cardiovascular disease and statin intolerance or contraindications: a Markov model. Am J Cardiovasc Drugs. 2008; 8 (6): 419–27. https://doi.org/10.2165/0129784-200808060-00005.
30. Kind P., Dolan P., Gudex C., Williams A. Variations in population health status: results from a United Kingdom national questionnaire survey. BMJ. 1998; 316 (7133): 736–41. https://doi.org/10.1136/bmj.316.7133.736.
31. Государственный реестр предельных отпускных цен производителей на лекарственные препараты, включенные в перечень жизненно необходимых и важнейших лекарственных препаратов. URL: https://minzdrav.gov.ru/opendata/7707778246-gosreestrpredelnyhotpusknyhcen/visual (дата обращения 07.02.2023).
32. Единая информационная система в сфере закупок. URL: https://zakupki.gov.ru/epz/main/public/home.html (дата обращения 07.02.2023).
33. Jukema J.W., Zijlstra L.E., Bhatt D.L., et al. Effect of Alirocumab on stroke in ODYSSEY OUTCOMES. Circulation. 2019; 140 (25): 2054–62. https://doi.org/10.1161/CIRCULATIONAHA.119.043826.
34. Постановление Правительства РФ от 28.12.2021 № 2505 «О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2022 год и на плановый период 2023 и 2024 годов» (с изменениями и дополнениями). URL: https://base.garant.ru/403335795/ (дата обращения 07.02.2023).
35. Письмо Министерства здравоохранения РФ от 24.12.2019 г. № 11-7/И/2-12330 «О направлении разъяснений по вопросам формирования и экономического обоснования территориальных программ государственных гарантий бесплатного оказания гражданам медицинской помощи». URL: https://www.garant.ru/products/ipo/prime/doc/73283735/ (дата обращения 07.02.2023).
36. Приказ Министерства здравоохранения РФ от 10.06.2021 г. № 612н «Об утверждении стандарта медицинской помощи взрослым при остром инфаркте миокарда с подъемом сегмента ST электрокардиограммы (диагностика, лечение и диспансерное наблюдение)». URL: https://www.garant.ru/products/ipo/prime/doc/401354840/ (дата обращения 07.02.2023).
37. Приказ Министерства здравоохранения РФ от 02.03.2021 г. № 158н «Об утверждении стандарта медицинской помощи взрослым при остром коронарном синдроме без подъема сегмента ST электрокардиограммы (диагностика, лечение и диспансерное наблюдение)». URL: https://base.garant.ru/400577761/ (дата обращения 07.02.2023).
38. Приказ Министерства здравоохранения РФ от 28.04.2021 г. № 410н «Об утверждении стандарта медицинской помощи взрослым при стабильной ишемической болезни сердца (диагностика, лечение и диспансерное наблюдение)». URL: https://base.garant.ru/400802511/ (дата обращения 07.02.2023).
39. Методические рекомендации по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования на 2022 год (утв. Министерством здравоохранения РФ и Федеральным фондом обязательного медицинского страхования 2 февраля 2022 г. №№ 11-7/И/2-1619, 00-10-26-2-06/750). URL: https://www.garant.ru/products/ipo/prime/doc/403402448/ (дата обращения 07.02.2023).
40. Бокерия Л.А., Милиевская Е.Б., Кудзоева З.Ф. и др. Сердечно-сосудистая хирургия – 2018. Болезни и врожденные аномалии системы кровообращения. М.: НМИЦССХ им. А.Н. Бакулева МЗ РФ; 2019: 270 c.
41. Marseille E., Larson B., Kazi D.S., et al. Thresholds for the costeffectiveness of interventions: alternative approaches. Bull World Health Organ. 2015; 93 (2): 118–24. https://doi.org/10.2471/BLT.14.138206.
42. Федеральная служба государственной статистики. Национальные счета. Валовой внутренний продукт. URL: https://rosstat.gov.ru/statistics/accounts (дата обращения 24.01.2023)
Об авторах
Т. О. БессоноваРоссия
Бессонова Татьяна Олеговна – главный специалист отдела методологического обеспечения проведения комплексной оценки технологий в здравоохранении; старший преподаватель кафедры организации здравоохранения и общественного здоровья
Хохловский пер., д. 10/5, Москва 109028
ул. Стасова, д. 8А, Пенза 440060
П. А. Мухортова
Россия
Мухортова Полина Алексеевна – ведущий специалист отдела методологического обеспечения проведения комплексной оценки технологий в здравоохранении
Хохловский пер., д. 10/5, Москва 109028
Р. А. Терян
Россия
Терян Рози Артемовна – к.м.н., главный специалист отдела методологии разработки и экспертной оценки клинических рекомендаций
Хохловский пер., д. 10/5, Москва 109028
А. Д. Багдасаров
Россия
Багдасаров Арсен Дмитриевич – специалист отдела методического обеспечения стандартизации; аспирант кафедры управления и экономики фармации
Хохловский пер., д. 10/5, Москва 109028
ул. Профессора Попова, д. 14, лит. А, Санкт-Петербург 197022
Н. З. Мусина
Россия
Мусина Нурия Загитовна – к.фарм.н., доцент кафедры управления и экономики фармации; начальник Управления международной деятельности
ул. Профессора Попова, д. 14, лит. А, Санкт-Петербург 197022
ул. Добролюбова, д. 11, Москва 127254
WoS ResearcherID: C-8075-2018; Scopus AuthorID: 56526954600
Рецензия
Для цитирования:
Бессонова Т.О., Мухортова П.А., Терян Р.А., Багдасаров А.Д., Мусина Н.З. Оценка клинико-экономической целесообразности применения лекарственных препаратов эзетимиб, алирокумаб, эволокумаб и инклисиран в рамках программы льготного лекарственного обеспечения пациентов очень высокого сердечно-сосудистого риска. ФАРМАКОЭКОНОМИКА. Современная фармакоэкономика и фармакоэпидемиология. 2023;16(1):17-34. https://doi.org/10.17749/2070-4909/farmakoekonomika.2023.173
For citation:
Bessonova T.O., Mukhortova P.A., Teryan R.A., Bagdasarov A.D., Musina N.Z. Cost-effectiveness analysis of using atorvastatin, simvastatin, ezetimibe, alirocumab, evolocumab, inclisiran in adults with very high cardiovascular risk under the preferential drug provision program. FARMAKOEKONOMIKA. Modern Pharmacoeconomics and Pharmacoepidemiology. 2023;16(1):17-34. (In Russ.) https://doi.org/10.17749/2070-4909/farmakoekonomika.2023.173

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.






































